某实验小组为探究CO与CuO的反应,设计了如下实验方案。
Ⅰ.CO的制备:甲同学设计了利用如下装置制备纯净的CO,并将其收集到储气罐中备用。
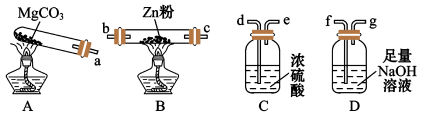
(1)各装置接口的连接顺序为__________ ,D装置的作用为____________ 。
(2)乙同学认为甲同学设计的装置过于复杂,他提出可以在A装置的试管中放入一定质量比的MgCO3和锌粉的混合物,加热后即可得到纯净的CO,则MgCO3与Zn粉的质量比最好为__________ 。
Ⅱ.CO还原CuO反应产物的探究:丙同学设计的实验装置如下图所示。
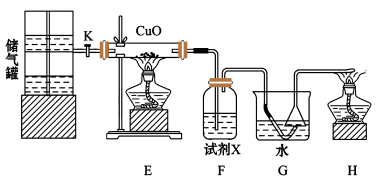
(3)实验开始时应先打开开关K,立即点燃________ (填“E处”或“H处”)的酒精灯,发现G处倒置于水中的漏斗轻轻向上弹起,过一小会儿又会落下,产生该实验现象的原因为________________________ 。
(4)F处的试剂X为________ ,反应开始一段时间后F处的实验现象为_______________________ 。
(5)CO在空气中燃烧产生淡蓝色火焰,但本实验却看到从H处玻璃管尖嘴处点燃的CO的火焰颜色呈黄色,火焰呈黄色的原因是______________________ 。
(6)反应结束后,E处硬质玻璃管中的CuO粉末全部变红,丁同学认为该红色物质全部为Cu,乙同学认为其中还可能含有Cu2O,因为Cu2O也是红色物质。请设计实验探究该红色粉末中是否含有Cu2O:____________ (已知:Cu2O+H2SO4=Cu+CuSO4+H2O)。
Ⅰ.CO的制备:甲同学设计了利用如下装置制备纯净的CO,并将其收集到储气罐中备用。

(1)各装置接口的连接顺序为
(2)乙同学认为甲同学设计的装置过于复杂,他提出可以在A装置的试管中放入一定质量比的MgCO3和锌粉的混合物,加热后即可得到纯净的CO,则MgCO3与Zn粉的质量比最好为
Ⅱ.CO还原CuO反应产物的探究:丙同学设计的实验装置如下图所示。

(3)实验开始时应先打开开关K,立即点燃
(4)F处的试剂X为
(5)CO在空气中燃烧产生淡蓝色火焰,但本实验却看到从H处玻璃管尖嘴处点燃的CO的火焰颜色呈黄色,火焰呈黄色的原因是
(6)反应结束后,E处硬质玻璃管中的CuO粉末全部变红,丁同学认为该红色物质全部为Cu,乙同学认为其中还可能含有Cu2O,因为Cu2O也是红色物质。请设计实验探究该红色粉末中是否含有Cu2O:
2020高三·全国·专题练习 查看更多[1]
(已下线)第5单元 常见的金属元素(A卷 基础过关检测)-2021年高考化学一轮复习单元滚动双测卷
更新时间:2020-08-23 09:47:16
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】I.回答下列问题:
(1)下列实验装置与实验操作正确的是_______

II.实验室里需要纯净的氯化钠溶液,但现在只有混有硫酸钠、碳酸氢铵的氯化钠。某学生设计了如下方案:

如果此方案正确,那么
(2)操作①加热可选择_______ 仪器,加热后产生的气体有刺激气味,写出反应的化学方程式_______
(3)操作②BaCl2溶液是否可改为加硝酸钡溶液?为什么?_______
(4)操作③加Na2CO3的目的是_______
(5)操作④加热煮沸的目的是_______ 。
(6)纯净的NaCl溶液通过_______ (操作)得到NaCl固体。用NaCl固体配制0.1 mol·L-1的NaCl溶液,实验中造成所配溶液浓度偏低的原因可能是_______ 。
A.容量瓶中原来含有少量蒸馏水
B.定容摇匀后少量溶液外流
C.向容量瓶中加水定容时眼睛一直仰视刻度线
(1)下列实验装置与实验操作正确的是

II.实验室里需要纯净的氯化钠溶液,但现在只有混有硫酸钠、碳酸氢铵的氯化钠。某学生设计了如下方案:

如果此方案正确,那么
(2)操作①加热可选择
(3)操作②BaCl2溶液是否可改为加硝酸钡溶液?为什么?
(4)操作③加Na2CO3的目的是
(5)操作④加热煮沸的目的是
(6)纯净的NaCl溶液通过
A.容量瓶中原来含有少量蒸馏水
B.定容摇匀后少量溶液外流
C.向容量瓶中加水定容时眼睛一直仰视刻度线
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】某科学小组利用工业锌渣(主要成分是ZnO、还含有少量的PbO、FeO、Fe2O3、CuO、MnO、SiO2)制取活性ZnO的工艺流程如下图所示:
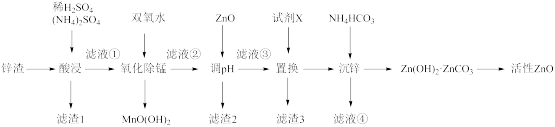
相关金属离子[C0(Mn+)=0.1mol/L]形成氢氧化物沉淀的pH范围如下:
请回答下列问题:
(1)为了提高锌渣的浸出率,可采取的措施有___________ (列举1点)。
(2)滤渣1的主要成分有___________ 和___________ (填化学式)。
(3)写出生成MnO(OH)2的离子方程式:___________ 。
(4)为了检验滤液②中是否含有Fe2+,可选用的试剂是___________ (填序号)。
a.氯水 b.KSCN溶液 c. K3[Fe(CN)6]溶液
(5)若滤渣2只含有一种成分,则加入ZnO调节pH的范围为___________ 。
(6)试剂X是___________ (填化学式)。
(7)NH4HCO3“沉锌”的离子方程式为___________ 。
(8)滤液④可循环利用,其主要成分的化学式为___________ 。

相关金属离子[C0(Mn+)=0.1mol/L]形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Fe3+ | Fe2+ | Zn2+ | Mn2+ | Cu2+ | Pb2+ |
| 开始沉淀的pH | 1.5 | 6.3 | 6.2 | 8.1 | 4.7 | 7.1 |
| 沉淀完全的pH | 2.8 | 8.3 | 8.2 | 10.1 | 6.7 | 10.5 |
请回答下列问题:
(1)为了提高锌渣的浸出率,可采取的措施有
(2)滤渣1的主要成分有
(3)写出生成MnO(OH)2的离子方程式:
(4)为了检验滤液②中是否含有Fe2+,可选用的试剂是
a.氯水 b.KSCN溶液 c. K3[Fe(CN)6]溶液
(5)若滤渣2只含有一种成分,则加入ZnO调节pH的范围为
(6)试剂X是
(7)NH4HCO3“沉锌”的离子方程式为
(8)滤液④可循环利用,其主要成分的化学式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】环境问题是广大群众关注的热点话题之一,化工厂排放的废水、废渣一般利用化学原理可以进行排放物达标检测与无害化处理。某皮革厂对制革工业污泥中Cr(Ⅲ)的处理工艺流程如图:

已知:①酸浸后的溶液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如表:
(1)如需配制480mL酸浸环节所需的硫酸,需要用量筒量取18.4mol·L-1的浓硫酸__________ mL;配制时所用玻璃仪器除量筒、烧杯和玻璃棒外,还需哪些仪器:__________ 。
(2)经氧化环节滤液I中的Cr3+转化为Cr2O ,写出此反应的离子方程式:
,写出此反应的离子方程式:__________ 。
(3)调pH=8环节,既可以将溶液中某些杂质离子转化为沉淀,同时又可以将Cr2O 转化为某种含铬元素微粒,溶液颜色由橙色变为黄色,请解释该颜色变化的原因
转化为某种含铬元素微粒,溶液颜色由橙色变为黄色,请解释该颜色变化的原因__________ 。
(4)钠离子交换树脂的反应原理为Mn++nNaR⇌MRn+nNa+,则利用钠离子交换树脂可除去滤液Ⅱ中的金属阳离子有__________ 。
(5)请写出流程中用SO2进行还原时发生反应的离子方程式:__________ 。
(6)沉淀滴定法是测定粒子浓度的方法之一,为了测定某废水中SCN—的浓度,可用标准AgNO3溶液滴定待测液,已知:
滴定时可选为滴定指示剂的是_____ (填编号),
A.NaCl B.K2CrO4 C.KI D.NaCN
如何确定该滴定过程的终点:__________ 。

已知:①酸浸后的溶液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如表:
| 阳离子 | Fe3+ | Mg2+ | Аl3+ | Cr3+ |
| 沉淀完全时的pH | 3.7 | 11.1 | 5.4 | 9 |
| 沉淀溶解时的pH | — | — | >8溶解 | >9溶解 |
(1)如需配制480mL酸浸环节所需的硫酸,需要用量筒量取18.4mol·L-1的浓硫酸
(2)经氧化环节滤液I中的Cr3+转化为Cr2O
 ,写出此反应的离子方程式:
,写出此反应的离子方程式:(3)调pH=8环节,既可以将溶液中某些杂质离子转化为沉淀,同时又可以将Cr2O
 转化为某种含铬元素微粒,溶液颜色由橙色变为黄色,请解释该颜色变化的原因
转化为某种含铬元素微粒,溶液颜色由橙色变为黄色,请解释该颜色变化的原因(4)钠离子交换树脂的反应原理为Mn++nNaR⇌MRn+nNa+,则利用钠离子交换树脂可除去滤液Ⅱ中的金属阳离子有
(5)请写出流程中用SO2进行还原时发生反应的离子方程式:
(6)沉淀滴定法是测定粒子浓度的方法之一,为了测定某废水中SCN—的浓度,可用标准AgNO3溶液滴定待测液,已知:
| 银盐性质 | AgCl | AgI | AgCN | Ag2CrO4 | AgSCN |
| 颜色 | 白 | 黄 | 白 | 砖红 | 白 |
| Ksp | 1.8×10-10 | 8.3×10-17 | 1.2×10-16 | 3.5×10-11 | 1.0×10-12 |
滴定时可选为滴定指示剂的是
A.NaCl B.K2CrO4 C.KI D.NaCN
如何确定该滴定过程的终点:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】“索尔维制碱法”工艺流程如图所示,请回答下列问题:
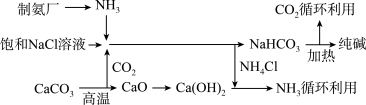
(1)向饱和氯化钠溶液中先通入___ ,效果更好。反应制得NaHCO3沉淀和NH4Cl溶液的化学方程式为____ 。
(2)索尔维制碱法除了得到纯碱外,还会产生一种废渣___ 。侯氏制碱法在此工艺上改进,不再使用碳酸钙制备CO2,而是在制备NH3的过程中制得CO2,则侯氏制碱法在得到纯碱的同时还制得了___ ,此物质在农业上的用途是___ 。

(1)向饱和氯化钠溶液中先通入
(2)索尔维制碱法除了得到纯碱外,还会产生一种废渣
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】氯气是一种重要的化工原料,呈黄绿色,有毒,能与多种物质反应。用图所示装置1可制取氯气,并对其性质进行一系列的实验探究。
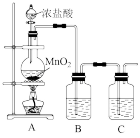
回答下列问题:
(1)①装置1中盛装浓盐酸的仪器名称是_______ 。
②实验室利用装置A制氯气,反应的离子方程式是_______ 。
(2)将装置1与装置2连接起来探究氯气的漂白性及氧化性。
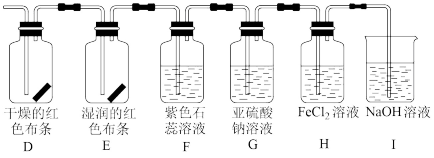
①D、E通入Cl2后,观察到的现象是_______ ,根据现象可得出结论:Cl2无漂白性,Cl2与水反应生成的HClO有漂白性。
②实验开始后,观察到洗气瓶F中的现象是_______ 。
③请设计一个实验,证明洗气瓶H中的FeCl2已被氧化(简述实验操作):_______ 。
④装置I中氢氧化钠的作用是(用离子方程式表示)_______ 。

回答下列问题:
(1)①装置1中盛装浓盐酸的仪器名称是
②实验室利用装置A制氯气,反应的离子方程式是
(2)将装置1与装置2连接起来探究氯气的漂白性及氧化性。

①D、E通入Cl2后,观察到的现象是
②实验开始后,观察到洗气瓶F中的现象是
③请设计一个实验,证明洗气瓶H中的FeCl2已被氧化(简述实验操作):
④装置I中氢氧化钠的作用是(用离子方程式表示)
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】高纯碳酸锰广泛应用于电子工业,是制造高性能磁性材料的主要原料。新工艺采用工业冶铜后的废气SO2进行湿法浸取软锰矿(主要含MnO2,同时含有少量SiO2、Fe2O3、Al2O3)来制备。(已知亚硫酸酸性强于碳酸)
①将过量的SO2气体通入软锰矿浆中进行“浸锰”操作,并控制温度加热反应;
②向浸锰结束后的滤液中加入MnO2、同时通入空气,再用Na2CO3溶液调节pH为3.7后
过滤分离;
③调节滤液pH为6.5~7.2 ,然后加入NH4HCO3 ,有浅红色的沉淀生成,过滤洗涤干燥后就可以得到高纯碳酸锰。
工业流程图如下:
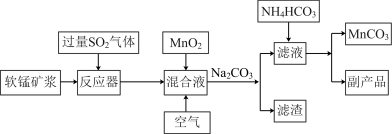
已知生成氢氧化物的pH如下表:
请根据题中有关信息回答问题:
(1)“浸锰”后所得混合液中主要存在的金属阳离子有____________________ 。
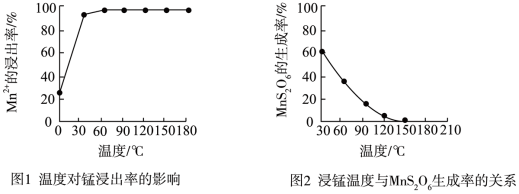
(2)由图可知,副反应MnSO4+ SO2 MnS2O6的△H
MnS2O6的△H_______ 0(填>、<或=),为减少MnS2O6的生成,“浸锰”的适宜温度是__________________________________ 。
(3)步骤②中加入MnO2和通入空气的作用___________________________________ 。
(4)③中控制温度为60~70℃,温度不宜太高的原因是_________________________ 。
(5)与传统的电解法制MnCO3工艺相比较,新工艺的优点是____________ (写两点)。
①将过量的SO2气体通入软锰矿浆中进行“浸锰”操作,并控制温度加热反应;
②向浸锰结束后的滤液中加入MnO2、同时通入空气,再用Na2CO3溶液调节pH为3.7后
过滤分离;
③调节滤液pH为6.5~7.2 ,然后加入NH4HCO3 ,有浅红色的沉淀生成,过滤洗涤干燥后就可以得到高纯碳酸锰。
工业流程图如下:


已知生成氢氧化物的pH如下表:
| 物质 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 8.3 |
| 完全沉淀pH | 3.7 | 9.6 | 9.8 |
请根据题中有关信息回答问题:
(1)“浸锰”后所得混合液中主要存在的金属阳离子有
(2)由图可知,副反应MnSO4+ SO2
 MnS2O6的△H
MnS2O6的△H(3)步骤②中加入MnO2和通入空气的作用
(4)③中控制温度为60~70℃,温度不宜太高的原因是
(5)与传统的电解法制MnCO3工艺相比较,新工艺的优点是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某校化学小组学生利用下图所列装置进行“铁与水反应”的实验。(图中夹持及尾气处理装置均已略去)
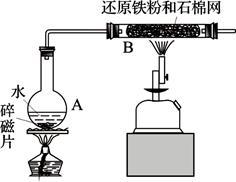
(1)烧瓶底部放置了几片碎瓷片,碎瓷片的作用是_____________ 。装置B中发生反应的化学方程式是_______________ 。
(2)停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤。简述检验滤液中Fe3+的操作方法__________ 。
(3)若(2)实验中未检验到Fe3+的存在,则可能的原因是__________ (用离子方程式表示)。

(1)烧瓶底部放置了几片碎瓷片,碎瓷片的作用是
(2)停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤。简述检验滤液中Fe3+的操作方法
(3)若(2)实验中未检验到Fe3+的存在,则可能的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某课外活动小组的同学在实验室做锌与浓硫酸反应的实验中,甲同学认为产生的气体是二氧化硫,而乙同学认为除二氧化硫气体外,还可能产生氢气。为了验证哪位同学的判断正确,丙同学设计了图中的实验装置(锌与浓硫酸共热时产生的气体为X,且该反应加热装置略去)。
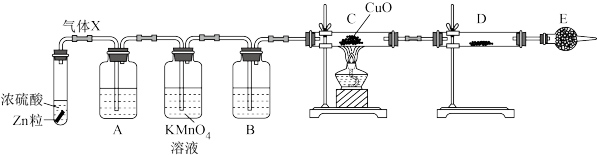
试回答下列问题:
(1)上述反应中生成二氧化硫的化学方程式为_______ 。
(2)乙同学认为还可能产生氢气的理由是_______ 。
(3)A中加入的试剂可能是_______ ,作用是_______ ;E中加入的试剂可能是_______ ,作用是_______ 。
(4)可以证明气体X中含有氢气的实验现象:C中_______ ,D中_______ 。

试回答下列问题:
(1)上述反应中生成二氧化硫的化学方程式为
(2)乙同学认为还可能产生氢气的理由是
(3)A中加入的试剂可能是
(4)可以证明气体X中含有氢气的实验现象:C中
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】实验室利用下图装置制备KClO,并探究其性质。据图回答下列问题:___________ ,A中发生反应的离子方程式为___________ 。
(2)B中盛放的试剂是___________ ,其作用是___________ 。
(3)制备KClO的反应是放热反应,反应温度较高时有副反应发生,改进该实验装置以减少副反应发生的方法是___________ 。
(4)E的作用是___________ ,下列不能代替E中NaOH溶液的是___________ (填正确答案标号)。
A. 溶液 B.NaCl溶液
溶液 B.NaCl溶液
C. 溶液 D.KI溶液
溶液 D.KI溶液
(5)在一支试管中依次加入氢氧化铁和氢氧化钾溶液,再加入KClO溶液,有紫红色的高铁酸钾( )生成,由此可知KClO具有
)生成,由此可知KClO具有___________ 性(填“氧化”或“还原”),完成并配平该反应的离子方程式:
___________

(2)B中盛放的试剂是
(3)制备KClO的反应是放热反应,反应温度较高时有副反应发生,改进该实验装置以减少副反应发生的方法是
(4)E的作用是
A.
 溶液 B.NaCl溶液
溶液 B.NaCl溶液C.
 溶液 D.KI溶液
溶液 D.KI溶液(5)在一支试管中依次加入氢氧化铁和氢氧化钾溶液,再加入KClO溶液,有紫红色的高铁酸钾(
 )生成,由此可知KClO具有
)生成,由此可知KClO具有
您最近一年使用:0次



