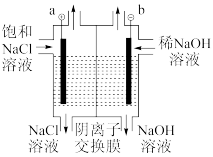
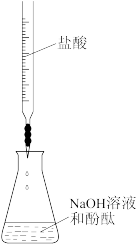
下列操作能达到实验目的的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 验证SO2的漂白性 | 将SO2通入溴水,观察溴水是否褪色 |
| B | 提纯含有少量乙酸的乙酸乙酯 | 向含有少量乙酸的乙酸乙酯中加入过量NaOH溶液,振荡后静置分液,并除去有机相中的水 |
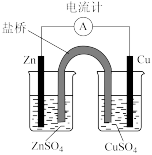
| C | 比较铁和锌的金属性强弱 | 将铁和锌置于稀硫酸中构成原电池 |
| D | 证明增大反应物浓度,能加快 化学反应速率 | 将两块表面积相同的锌粒分别放入稀硫酸和浓硫酸中 |
| A.A | B.B | C.C | D.D |
更新时间:2020/08/24 17:04:48
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】(原创)下列现象或事实可用同一原理解释的是
| A.氯水和二氧化硫使品红溶液褪色 |
| B.亚硫酸钠和水玻璃长期暴露在空气中变质 |
| C.稀硝酸和三氯化铁溶液使KI-淀粉试纸变蓝 |
| D.浓盐酸和浓硫酸长期暴露在空气中浓度变小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】X、Y、Z、W四种元素的原子序数依次增大,它们离子的电子层结构相同。X原子的L层电子数与K、M层电子数之和相等,W原子的K、L层电子数之和等于其电子总数的一半。下列说法错误的是
| A.四种元素中原子半径最大的是W |
| B.四种元素对应的单质氧化性最强的是Y |
| C.X的一种氧化物具有漂白性 |
| D.Y的最高正价与最低负价的代数和为6 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】氧、硫及其化合物应用广泛。O2可用作燃料电池的氧化剂。S8在液态SO2中被AsF5氧化成S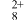 ,反应方程式为S8+3AsF5
,反应方程式为S8+3AsF5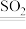 S8(AsF6)2+AsF3。氧能形成H2O、H2O2、Na2O2、SO2、V2O5等重要氧化物。SO2是一种重要的工业原料,可通过煅烧黄铁矿或加热无水硫酸钙、焦炭及二氧化硅的混合物(CaSO4+C+SiO2
S8(AsF6)2+AsF3。氧能形成H2O、H2O2、Na2O2、SO2、V2O5等重要氧化物。SO2是一种重要的工业原料,可通过煅烧黄铁矿或加热无水硫酸钙、焦炭及二氧化硅的混合物(CaSO4+C+SiO2 SO2↑+CO↑+CaSiO3)等方法来制取。SO2在V2O5催化作用下与O2反应生成SO3。下列关于物质结构与性质或物质性质与用途具有对应关系说法正确的是
SO2↑+CO↑+CaSiO3)等方法来制取。SO2在V2O5催化作用下与O2反应生成SO3。下列关于物质结构与性质或物质性质与用途具有对应关系说法正确的是
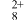 ,反应方程式为S8+3AsF5
,反应方程式为S8+3AsF5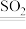 S8(AsF6)2+AsF3。氧能形成H2O、H2O2、Na2O2、SO2、V2O5等重要氧化物。SO2是一种重要的工业原料,可通过煅烧黄铁矿或加热无水硫酸钙、焦炭及二氧化硅的混合物(CaSO4+C+SiO2
S8(AsF6)2+AsF3。氧能形成H2O、H2O2、Na2O2、SO2、V2O5等重要氧化物。SO2是一种重要的工业原料,可通过煅烧黄铁矿或加热无水硫酸钙、焦炭及二氧化硅的混合物(CaSO4+C+SiO2 SO2↑+CO↑+CaSiO3)等方法来制取。SO2在V2O5催化作用下与O2反应生成SO3。下列关于物质结构与性质或物质性质与用途具有对应关系说法正确的是
SO2↑+CO↑+CaSiO3)等方法来制取。SO2在V2O5催化作用下与O2反应生成SO3。下列关于物质结构与性质或物质性质与用途具有对应关系说法正确的是| A.Na2O2具有较高的熔点,可用于潜艇的供氧剂 |
| B.SO2易溶于水,可用于漂白羽毛 |
| C.H2O2具有强氧化性,可用KMnO4溶液通过滴定法测定其浓度 |
| D.焦炭具有还原性,可用于制备晶体硅 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列描述正确的是
| A.电解AlCl3饱和溶液,可制得金属铝 |
| B.用惰性电极电解足量CuSO4溶液,一段时间后,阴极和阳极析出产物的质量之比为4∶1 |
| C.将等体积不同浓度的酸性高锰酸钾溶液分别滴入等浓度等体积的草酸溶液中,依据褪色快慢,比较浓度对反应速率的影响 |
| D.新制氯水中存在两种电离平衡,且2c(Cl2) =c (Cl-) +c (ClO-) +c (HClO) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知Fe3+和I-在水溶液中的反应为2I-+2Fe3+ I2+2Fe2+。某温度下该反应的正反应速率和I-、Fe3+浓度的关系为v=kcm(I-)·cn(Fe3+)(k为常数)。
I2+2Fe2+。某温度下该反应的正反应速率和I-、Fe3+浓度的关系为v=kcm(I-)·cn(Fe3+)(k为常数)。
由此推知,有关Fe3+、I-的浓度对反应速率影响的判断正确的是
 I2+2Fe2+。某温度下该反应的正反应速率和I-、Fe3+浓度的关系为v=kcm(I-)·cn(Fe3+)(k为常数)。
I2+2Fe2+。某温度下该反应的正反应速率和I-、Fe3+浓度的关系为v=kcm(I-)·cn(Fe3+)(k为常数)。c(I-)/mol·L-1 | c(Fe3+)/mol·L-1 | v/mol·L-1·s-1 | |
① | 0.20 | 0.80 | 0.032k |
② | 0.60 | 0.40 | 0.144k |
③ | 0.80 | 0.20 | 0.128k |
| A.Fe3+浓度对正反应速率的影响程度大于I-浓度的影响程度 |
| B.Fe3+浓度对正反应速率的影响程度小于I-浓度的影响程度 |
| C.Fe3+浓度对正反应速率的影响程度等于I-浓度的影响程度 |
| D.无法比较 |
您最近一年使用:0次
单选题-单题
|
适中
(0.65)
解题方法
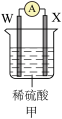
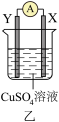
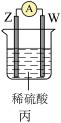
【推荐1】有W、X、Y、Z四种金属,按下列装置进行实验,电流表指针均发生偏转,下列说法正确的是
| 实验装置 |
|
|
|
| 现象 | W不断溶解 | Y的质量增加 | W上有气泡产生 |
| A.装置甲中W作原电池负极,电子的流动方向:W→电解质溶液→X |
B.装置乙中Y电极上的电极反应式为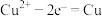 |
| C.装置丙中Z电极不断溶解,发生还原反应 |
| D.四种金属的活动性强弱顺序为Z>W>X>Y |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验方案的设计能达到相应实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 验证Cl2的氧化性强于Br2 | 向FeBr2溶液中通入少量Cl2 |
| B | 比较HF与HClO的酸性强弱 | 常温下,用pH计分别测定浓度为0.1 mol/L的NaF溶液和NaClO溶液的pH |
| C | 验证FeCl3与KI的反应是可逆反应 | 向1 mL0.1 mol/L FeCl3的溶液中滴加5 mL0.1mol/LKI溶液,充分反应后,取少量混合液滴加淀粉溶液 |
| D | 比较Fe与Cu的金属活动性 | 常温下,将Fe、Cu与浓硝酸组成原电池 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】除去下列物质中混入的少量杂质(括号内物质为杂质),能达到实验目的的是( )
| A.乙醇(水):加足量生石灰,过滤 |
| B.溴苯(溴):加入足量的Na2SO3溶液,充分振荡、静置、分液 |
| C.乙酸乙酯(乙酸):加入足量的NaOH溶液,充分振荡、静置、分液 |
| D.苯酚(甲苯):加入足量的酸性KMnO4溶液,充分振荡、静置、分液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
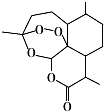
【推荐2】阿司匹林具有解热镇痛作用,科研工作者在一定条件下合成长效缓释阿司匹林,从而减少了对肠胃的刺激和每天吃药次数。下列说法正确的是
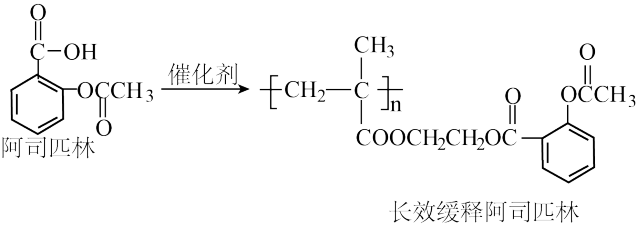
A. 阿司匹林与足量的 阿司匹林与足量的 反应,最多消耗 反应,最多消耗  |
| B.阿司匹林与长效缓释阿司匹林可通过红外光谱区别 |
| C.阿司匹林和长效缓释阿司匹林中碳原子的杂化方式不同 |
D. 长效缓释阿司匹林与 长效缓释阿司匹林与 溶液反应,最多消耗 溶液反应,最多消耗  |
您最近一年使用:0次

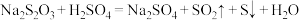 的速率影响因素,某实验小组利用
的速率影响因素,某实验小组利用 溶液与
溶液与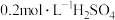 溶液设计和探究实验如下表:
溶液设计和探究实验如下表: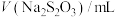
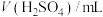
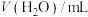


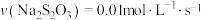
 的体积变化来判断反应速率的快慢
的体积变化来判断反应速率的快慢