如图为原电池装置示意图。
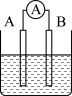
(1)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,作负极的分别是_____ (填字母)。
A.铝片、铜片B.铜片、铝片
C.铝片、铝片D.铜片、铜片
写出插入烧碱溶液中形成的原电池的负极反应式_____ ;
(2)若A为Pb,B为PbO2,电解质为H2SO4溶液,工作时的总反应为Pb+PbO2+2H2SO4===2PbSO4+2H2O。写出B电极反应式_____ ,该电池在工作时,A电极的质量将___ (填“增加”“减小”或“不变”)。若该电池反应消耗了0.1molH2SO4,则转移电子的数目为_____ 。
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入CH4和O2,该电池即为甲烷燃料电池,写出A电极反应式:_____ ;该电池在工作一段时间后,溶液的pH将_____ (填“增大”“减小”或“不变”)。

(1)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,作负极的分别是
A.铝片、铜片B.铜片、铝片
C.铝片、铝片D.铜片、铜片
写出插入烧碱溶液中形成的原电池的负极反应式
(2)若A为Pb,B为PbO2,电解质为H2SO4溶液,工作时的总反应为Pb+PbO2+2H2SO4===2PbSO4+2H2O。写出B电极反应式
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入CH4和O2,该电池即为甲烷燃料电池,写出A电极反应式:
更新时间:2020-08-24 22:05:13
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】回答下列问题:
(1)某温度下,在1 L恒容密闭容器中A、B、C三种气体物质的浓度随时间变化曲线如图所示,t是到达平衡状态的时间。试回答:
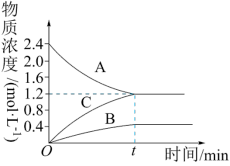
①该反应的反应物是_______ 。
②该反应的化学反应方程式为_______ 。
③若达到平衡状态的时间是2 min,B物质的平均反应速率为_______ mol/(L•min)。
(2)观察图,回答问题。
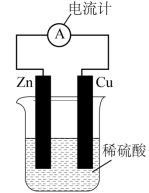
①该装置叫_______ 装置,可以将化学能转化为电能。
②负极是_______ ,总反应的化学方程式为_______ 。
(1)某温度下,在1 L恒容密闭容器中A、B、C三种气体物质的浓度随时间变化曲线如图所示,t是到达平衡状态的时间。试回答:

①该反应的反应物是
②该反应的化学反应方程式为
③若达到平衡状态的时间是2 min,B物质的平均反应速率为
(2)观察图,回答问题。

①该装置叫
②负极是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】化学反应中的物质变化和能量变化与化学键密切相关。依据所学知识回答下列问题:
1.(1)将装有二氧化氮和四氧化二氮混合气体的烧瓶分别侵入冷水和热水中,观察到的现象是______________________ ,由此得出的结论是_______________________________________ 。
2.(2)某同学根据原电池原理。将离子反应Cu+2Fe3+=Cu2++2Fe2+设计成原电池,在该原电池中,以FeCl3 为电解质溶液,以石墨为正极材料,负极材料应选用_______________ ,负极上发生________ 反应(填写“氧化“或“还原”)。当反应进行一段时间,测得负极电极质量减轻了6.4g,原电池的电路中转移电子的物质的量是____________________________ 。
3.(3)从能量角度看,断裂化学键吸收能量,形成化学键释放能量。
已知:断裂1molH-H键吸收的能量为436kJ,断裂气态ImolI-I键吸收的能量为151kJ,形成lmolH-I键放出的能量为299kJ。
则由氢气和碘蒸气反应生成1molHI需要________ (填“放出“或“吸收”)_______ kJ的热量
1.(1)将装有二氧化氮和四氧化二氮混合气体的烧瓶分别侵入冷水和热水中,观察到的现象是
2.(2)某同学根据原电池原理。将离子反应Cu+2Fe3+=Cu2++2Fe2+设计成原电池,在该原电池中,以FeCl3 为电解质溶液,以石墨为正极材料,负极材料应选用
3.(3)从能量角度看,断裂化学键吸收能量,形成化学键释放能量。
已知:断裂1molH-H键吸收的能量为436kJ,断裂气态ImolI-I键吸收的能量为151kJ,形成lmolH-I键放出的能量为299kJ。
则由氢气和碘蒸气反应生成1molHI需要
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】锌铜原电池的工作原理
(1)ZnZnSO4半电池:在ZnSO4溶液中,锌片逐渐溶解,即Zn被_______ ,锌原子失去电子,形成Zn2+进入溶液,即Zn-2e-=Zn2+;从锌片上释放出的_______ ,经过导线流向铜片。
(2)CuCuSO4半电池:CuSO4溶液中的Cu2+从铜片上得到_______ ,_______ 为铜单质并沉积在铜片上,即Cu2++2e-=Cu。
(3)盐桥的作用:电池工作时,盐桥中的_______ 会移向ZnSO4溶液,_______ 移向CuSO4溶液,使两溶液均保持电中性。当取出盐桥后,形成断路,反应停止。
| 装置示意图 | 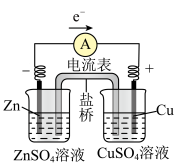 注:盐桥中装有含KCl饱和溶液的琼胶 |
| 现象 | 锌片 |
| 能量转换 | |
| 微观探析 | 在硫酸锌溶液中,负极一端的 在硫酸铜溶液中,正极一端的 |
| 电子或离子移动方向 | 电子: 盐桥: |
| 工作原理,电极反应式 | 负极:Zn-2e-=Zn2+( 正极:Cu2++2e-=Cu( |
| 总反应:Zn+Cu2+=Zn2++Cu |
(2)CuCuSO4半电池:CuSO4溶液中的Cu2+从铜片上得到
(3)盐桥的作用:电池工作时,盐桥中的
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】能源是现代文明的原动力,电池与我们的生活和生产密切相关。
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是___ (填字母)。
A.C(s)+H2O(g)=CO(g)+H2(g)
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)
C.2CO(g)+O2=2CO2(l)
(2)如图为原电池装置示意图:___ ,反应过程中溶液的酸性___ (填“变大”变小“或”不变“)。一段时间后,当在电池中放出1.68L(标准状况)气体时,电路中有___ 个电子通过了导线(设NA为阿伏加德罗常数的值)。
②若电池的总反应为2Fe3++Cu=2Fe2++Cu2+,负极材料是___ ,负极的电极反应式为___ 。
③若A为镁片,B为铝片,电解质为NaOH溶液,则铝片为___ 极(填正或负);写出该电极电极反应式:__ 。
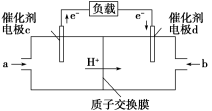
④燃料电池是一种具有应用前景的绿色电源,H2和O2组合形成的燃料电池的结构如图(电解液是稀硫酸):___ (填“正极”或“负极”),电极d的电极反应式为_____ 。若线路中转移2mol电子,则该燃科电池理论上消耗的O2在标准状况下的体积为___ L。
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是
A.C(s)+H2O(g)=CO(g)+H2(g)
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)
C.2CO(g)+O2=2CO2(l)
(2)如图为原电池装置示意图:
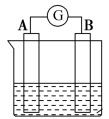
②若电池的总反应为2Fe3++Cu=2Fe2++Cu2+,负极材料是
③若A为镁片,B为铝片,电解质为NaOH溶液,则铝片为
④燃料电池是一种具有应用前景的绿色电源,H2和O2组合形成的燃料电池的结构如图(电解液是稀硫酸):
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】某化学兴趣小组进行如图所示实验,以检验化学反应中的能量变化。
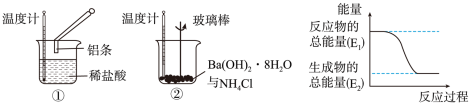
请回答下列问题:
(1)反应①的离子方程式是___________ ;反应②的化学方程式___________ 。
(2)②中的温度___________ (填“升高”或“降低”)。反应___________ (填“①”或“②”)的能量变化可用图表示。
(3)现有如下两个反应:
A.
B.
①A反应不能设计成原电池的原因是___________ 。
②利用B反应可设计成原电池,该电池负极的电极反应式为___________ ,可用作该电池正极材料的是___________ (填字母)。
a.碳棒 b.铁片 c.铜片 d.铂棒
(4)用 和
和 组合形成的质子交换膜燃料电池的结构如图:
组合形成的质子交换膜燃料电池的结构如图:
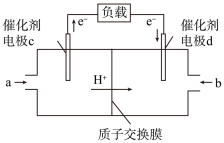
则d电极是燃料电池的___________ (填“正极”或“负极”),此电极的电极反应式为___________ 。

请回答下列问题:
(1)反应①的离子方程式是
(2)②中的温度
(3)现有如下两个反应:
A.

B.

①A反应不能设计成原电池的原因是
②利用B反应可设计成原电池,该电池负极的电极反应式为
a.碳棒 b.铁片 c.铜片 d.铂棒
(4)用
 和
和 组合形成的质子交换膜燃料电池的结构如图:
组合形成的质子交换膜燃料电池的结构如图:
则d电极是燃料电池的
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】化学反应的过程不仅包括物质变化,还包括能量变化。研究化学能与其他形式能量之间的转化具有重要意义。
I.化学能转化为热能
(1)氢气在氯气中燃烧时产生苍白色火焰,并释放大量的热。若破坏1molH2中的化学键吸收的能量为Q1 kJ,破坏1mol Cl2中的化学键吸收的能量为O2 kJ,形成1mol HCl中的化学键释放的能量为Q3 kJ。则由H2和Cl2反应生成1mol HCl时,释放的能量为______ kJ(用含Q1、Q2、Q3的代数式表示)。
Ⅱ.化学能转化为电能
原电池是将化学能转化为电能的装置,其构成要素可用图1来表示:

(2)氢氧燃料电池(如图2)中,正极材料和负极材料均可选用______ ;正极的电极反应式为______ ;电池工作时,溶液中的OH—移向______ 极(填“正”或“负”)。
(3)如果将反应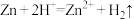 设计成原电池,则负极材料为
设计成原电池,则负极材料为______ (填化学式,下同)正极反应产物为______ ;离子导体为______ 。
(4)如果以Mg、Al为电极材料,NaOH溶液为离子导体,设计成原电池,则Al电极上的电极反应式为______ 。
I.化学能转化为热能
(1)氢气在氯气中燃烧时产生苍白色火焰,并释放大量的热。若破坏1molH2中的化学键吸收的能量为Q1 kJ,破坏1mol Cl2中的化学键吸收的能量为O2 kJ,形成1mol HCl中的化学键释放的能量为Q3 kJ。则由H2和Cl2反应生成1mol HCl时,释放的能量为
Ⅱ.化学能转化为电能
原电池是将化学能转化为电能的装置,其构成要素可用图1来表示:

(2)氢氧燃料电池(如图2)中,正极材料和负极材料均可选用
(3)如果将反应
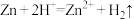 设计成原电池,则负极材料为
设计成原电池,则负极材料为(4)如果以Mg、Al为电极材料,NaOH溶液为离子导体,设计成原电池,则Al电极上的电极反应式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】新一代锂二次电池体系和全固态锂二次电池体系是化学、物理等学科的基础理论研究与应用技术的前沿。
(1)Li-CuO二次电池的比能量高、工作温度宽。Li-CuO二次电池中,金属锂作___ 极。比能量是指消耗单位质量的电极所释放的电量,用来衡量电池的优劣,则Li、Na、Al分别作为电极时比能量由大到小的顺序为___ 。
(2)通过如下过程制备CuO:

“过程II”产生Cu2(OH)2CO3的离子方程式为____ 。
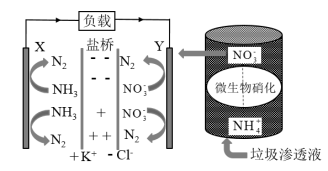
(3)某种利用垃圾渗透液实现发电装置示意图如下,当该装置工作时,Y极发生的电极反应式为___ 。
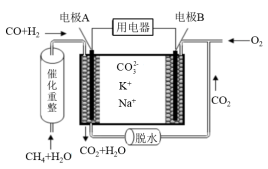
(4)一种熔融碳酸盐燃料电池原理示意如图所示。电极A上CO参与的电极反应式为_______ 。
(5)某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。
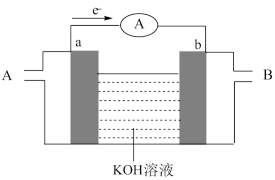
①假设使用的“燃料”是氢气(H2),则b极的电极反应式为_______ 。
②假设使用的“燃料”是甲醇(CH3OH),则a极的电极反应式为_______ 。
如果消耗甲醇160g,假设化学能完全转化为电能,则转移电子的数目为___ (用NA表示)。
(1)Li-CuO二次电池的比能量高、工作温度宽。Li-CuO二次电池中,金属锂作
(2)通过如下过程制备CuO:

“过程II”产生Cu2(OH)2CO3的离子方程式为
(3)某种利用垃圾渗透液实现发电装置示意图如下,当该装置工作时,Y极发生的电极反应式为

(4)一种熔融碳酸盐燃料电池原理示意如图所示。电极A上CO参与的电极反应式为

(5)某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。

①假设使用的“燃料”是氢气(H2),则b极的电极反应式为
②假设使用的“燃料”是甲醇(CH3OH),则a极的电极反应式为
如果消耗甲醇160g,假设化学能完全转化为电能,则转移电子的数目为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】将锌片和铜片用导线连接后插入稀硫酸中,并在中间串联一个电流表,装置如图所示。
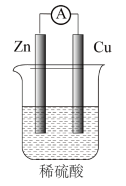
(1)该装置可以将_______ 能转化为_______ 能。
(2)装置中的负极材料是_______ 。
(3)铜片上的电极反应式是_______ ,该电极上发生了_______ (填“氧化”或“还原”)反应。
(4)稀硫酸中的SO 向
向_______ 片移动。导线中电子流向_______ 片。
(5)若将电解质溶液换成CuSO4溶液,则正极上的实验现象为_______ 。

(1)该装置可以将
(2)装置中的负极材料是
(3)铜片上的电极反应式是
(4)稀硫酸中的SO
 向
向(5)若将电解质溶液换成CuSO4溶液,则正极上的实验现象为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】(1)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,作负极的分别是____ (填字母)。
A. 铝片、铜片 B. 铜片、铝片 C. 铝片、铝片 D. 铜片、铜片
写出插入烧碱溶液中形成的原电池的负极反应式:______ 。
(2)若A为Pb,B为PbO2,电解质为H2SO4溶液,工作时的总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O。写出A电极反应式:______ ;该电池在工作时,A电极的质量将____ (填“增加”“减小”或“不变”)。若该电池反应消耗了0.1 mol H2SO4,则转移电子的数目为____ 。
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为氢氧燃料电池,写出B电极反应式:____ ;该电池在工作一段时间后,溶液的碱性将______ (填“增强”“减弱”或“不变”)。
(4)若A、B均为铂片,电解质为H2SO4溶液,分别从A、B两极通入CH4和O2,该电池即为甲烷燃料电池,写出A电极反应式:_______ ;若该电池反应消耗了6.4gCH4,则转移电子的数目为_____ 。
A. 铝片、铜片 B. 铜片、铝片 C. 铝片、铝片 D. 铜片、铜片
写出插入烧碱溶液中形成的原电池的负极反应式:
(2)若A为Pb,B为PbO2,电解质为H2SO4溶液,工作时的总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O。写出A电极反应式:
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为氢氧燃料电池,写出B电极反应式:
(4)若A、B均为铂片,电解质为H2SO4溶液,分别从A、B两极通入CH4和O2,该电池即为甲烷燃料电池,写出A电极反应式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】某化学兴趣小组为了探究铝电极在原电池中的作用,设计并进行了下列实验,实验结果记录如下:
根据上表中的实验现象完成下列问题:
(1)实验1、2中Al的电极名称分别是___________ 。
(2)指出实验3中铝和石墨的电极名称,并写出相应的电极反应和电池总反应。
铝为___________ ,电极反应式为___________ ;
石墨为___________ ,电极反应式为___________ 。
电池总反应式为___________ 。
(3)实验4中的铝作___________ (填“正极”或“负极”),理由为___________ 。
(4)请解释实验5中检流计指针偏向铝电极的原因:___________ 。
| 实验编号 | 电极材料 | 电解质溶液 | 检流计指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al电极 |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu电极 |
| 3 | Al、石墨 | 稀盐酸 | 偏向石墨电极 |
| 4 | Mg、Al | NaOH溶液 | 偏向Mg电极 |
| 5 | Al、Zn | 浓硝酸 | 偏向Al电极 |
(1)实验1、2中Al的电极名称分别是
(2)指出实验3中铝和石墨的电极名称,并写出相应的电极反应和电池总反应。
铝为
石墨为
电池总反应式为
(3)实验4中的铝作
(4)请解释实验5中检流计指针偏向铝电极的原因:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】根据化学能转化电能的相关知识,回答下列问题:
Ⅰ.理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“ ”设计一个化学电池(正极材料用碳棒),回答下列问题:
”设计一个化学电池(正极材料用碳棒),回答下列问题:
(1)该电池的负极材料是___________ ,发生___________ (填“氧化”或“还原”)反应,电解质溶液是___________ 。
(2)正极上出现的现象是___________ 。
(3)若导线上转移电子 ,则消耗铜
,则消耗铜___________  。
。
Ⅱ. 有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入 的
的 溶液中,乙同学将电极放入
溶液中,乙同学将电极放入 的
的 溶液中,如图所示。
溶液中,如图所示。
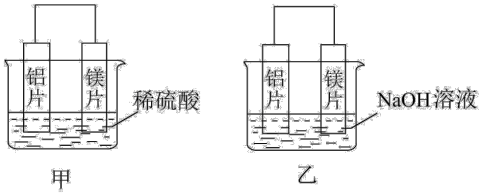
(4)写出甲中正极的电极反应式:___________ 。
(5)写出乙中总反应的离子方程式:___________ 。
Ⅰ.理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“
 ”设计一个化学电池(正极材料用碳棒),回答下列问题:
”设计一个化学电池(正极材料用碳棒),回答下列问题:(1)该电池的负极材料是
(2)正极上出现的现象是
(3)若导线上转移电子
 ,则消耗铜
,则消耗铜 。
。Ⅱ. 有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入
 的
的 溶液中,乙同学将电极放入
溶液中,乙同学将电极放入 的
的 溶液中,如图所示。
溶液中,如图所示。
(4)写出甲中正极的电极反应式:
(5)写出乙中总反应的离子方程式:
您最近一年使用:0次




