为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施。化学反应的焓变通常用实验进行测定,也可进行理论推算。
(1)实验测得 甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出
甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出 的热量,试写出甲醇燃烧的热化学方程式:
的热量,试写出甲醇燃烧的热化学方程式:__________ 。
(2)由气态基态原子形成 化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键被破坏和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。
化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键被破坏和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。
已知反应: 。试根据表中所列键能数据估算
。试根据表中所列键能数据估算 的值为
的值为__________ 。
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。已知:25℃、 时:
时:
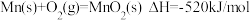


 与
与 反应生成无水
反应生成无水 的热化方程式是:
的热化方程式是:___________ 。
(1)实验测得
 甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出
甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出 的热量,试写出甲醇燃烧的热化学方程式:
的热量,试写出甲醇燃烧的热化学方程式:(2)由气态基态原子形成
 化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键被破坏和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。
化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键被破坏和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。| 化学键 | H-H | N-H | N≡N |
| 键能/(kJ·mol-1) | 436 | 391 | 945 |
已知反应:
 。试根据表中所列键能数据估算
。试根据表中所列键能数据估算 的值为
的值为(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。已知:25℃、
 时:
时: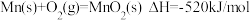


 与
与 反应生成无水
反应生成无水 的热化方程式是:
的热化方程式是:
更新时间:2020-08-26 18:07:16
|
相似题推荐
计算题
|
较易
(0.85)
名校
解题方法
【推荐1】填空
(1)已知C(s,石墨)=C(s,金刚石) ΔH>0,则稳定性:金刚石___ (填“>”或“<”)石墨。
(2)已知:2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2;则ΔH1____ (填“>”或“<”)ΔH2。
(3)“嫦娥五号”发射时,用肼(N2H4)作燃料,四氧化二氮作氧化剂,二者反应生成氮气和气态水。已知:
①N2(g)+2O2(g)=N2O4(g) ΔH=+10.7 kJ·mol-1;
②N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-543 kJ·mol-1
写出气态肼和N2O4反应的热化学方程式:________ 。
(4)25 ℃、101 kPa时,14 g CO在足量的O2中充分燃烧,放出141.3 kJ热量,则CO的燃烧热ΔH=____ 。
(5)0.50 L 2.00 mol·L-1H2SO4溶液与2.10 L 1.00 mol·L-1 KOH溶液完全反应,放出114.6 kJ热量,该反应的中和热ΔH=______ 。
(6)已知断开1 mol H-H键、1 mol N-H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式是________ 。
(1)已知C(s,石墨)=C(s,金刚石) ΔH>0,则稳定性:金刚石
(2)已知:2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2;则ΔH1
(3)“嫦娥五号”发射时,用肼(N2H4)作燃料,四氧化二氮作氧化剂,二者反应生成氮气和气态水。已知:
①N2(g)+2O2(g)=N2O4(g) ΔH=+10.7 kJ·mol-1;
②N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-543 kJ·mol-1
写出气态肼和N2O4反应的热化学方程式:
(4)25 ℃、101 kPa时,14 g CO在足量的O2中充分燃烧,放出141.3 kJ热量,则CO的燃烧热ΔH=
(5)0.50 L 2.00 mol·L-1H2SO4溶液与2.10 L 1.00 mol·L-1 KOH溶液完全反应,放出114.6 kJ热量,该反应的中和热ΔH=
(6)已知断开1 mol H-H键、1 mol N-H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式是
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
解题方法
【推荐2】Ⅰ、某实验小组用100mL0.55mol·L NaOH溶液与100mL0.5mol·L
NaOH溶液与100mL0.5mol·L 盐酸进行中和热的测定,装置如图所示。
盐酸进行中和热的测定,装置如图所示。
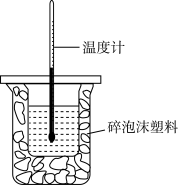
(1)回答下列问题:
①图中装置缺少的仪器是___________ 。
②若将盐酸改为相同体积、相同浓度的醋酸,测得中和热为ΔH1,NaOH溶液与盐酸反应中和热为ΔH,则ΔH1___________ ΔH (填写<、>、=);若测得该反应放出的热量为2.84kJ,请写出盐酸与NaOH溶液反应的中和热的热化学方程式:___________
Ⅱ、已知1g的甲烷完全燃烧生成液态水放出akJ的热量。
(2)写出表示甲烷燃烧热的热化学方程式为___________ 。
Ⅲ、发射卫星可用肼做燃料,二氧化氮做氧化剂,两者反应生成氮气和水蒸气。已知:

 kJ·mol
kJ·mol

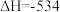 kJ·mol
kJ·mol
(3)写出肼和二氧化氮反应的热化学方程式为:___________ 。
(4)有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。若1mol氢气完全燃烧生成1mol气态水放出241kJ的热量,已知H-O键能为463kJ·mol ,O=O键能为498kJ·mol
,O=O键能为498kJ·mol ,计算H-H键能为
,计算H-H键能为___________ kJ·mol 。
。
 NaOH溶液与100mL0.5mol·L
NaOH溶液与100mL0.5mol·L 盐酸进行中和热的测定,装置如图所示。
盐酸进行中和热的测定,装置如图所示。
(1)回答下列问题:
①图中装置缺少的仪器是
②若将盐酸改为相同体积、相同浓度的醋酸,测得中和热为ΔH1,NaOH溶液与盐酸反应中和热为ΔH,则ΔH1
Ⅱ、已知1g的甲烷完全燃烧生成液态水放出akJ的热量。
(2)写出表示甲烷燃烧热的热化学方程式为
Ⅲ、发射卫星可用肼做燃料,二氧化氮做氧化剂,两者反应生成氮气和水蒸气。已知:

 kJ·mol
kJ·mol

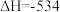 kJ·mol
kJ·mol
(3)写出肼和二氧化氮反应的热化学方程式为:
(4)有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。若1mol氢气完全燃烧生成1mol气态水放出241kJ的热量,已知H-O键能为463kJ·mol
 ,O=O键能为498kJ·mol
,O=O键能为498kJ·mol ,计算H-H键能为
,计算H-H键能为 。
。
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
解题方法
【推荐3】(1)由N2和H2合成1 mol NH3时可放出46.2 kJ/mol的热量。从手册上查出N≡N键的键能是948.9 kJ/mol,H-H键的键能是436.0 kJ/mol,则N-H键的键能是_______ kJ/mol。
(2)黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:S(s)+2KNO3(s)+3C(s)=K2S(s)+N2(g)+3CO2(g) ΔH=x kJ•mol-1
已知:碳的燃烧热ΔH1=a kJ•mol-1
S(s)+2K(s)=K2S(s) ΔH2=b kJ•mol-1
2K(s)+N2(g)+3O2(g)=2KNO3(s) ΔH 3=c kJ•mol-1,则x为_____ kJ/mol
(3)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态过氧化氢。当把0.4 mol液态肼和0.8 mol H2O2混合反应,生成氮气和水蒸气,放出256.7 kJ的热量(相当于25℃、101kPa下测得的热量)。反应的热化学方程式为_______ 。
(2)黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:S(s)+2KNO3(s)+3C(s)=K2S(s)+N2(g)+3CO2(g) ΔH=x kJ•mol-1
已知:碳的燃烧热ΔH1=a kJ•mol-1
S(s)+2K(s)=K2S(s) ΔH2=b kJ•mol-1
2K(s)+N2(g)+3O2(g)=2KNO3(s) ΔH 3=c kJ•mol-1,则x为
(3)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态过氧化氢。当把0.4 mol液态肼和0.8 mol H2O2混合反应,生成氮气和水蒸气,放出256.7 kJ的热量(相当于25℃、101kPa下测得的热量)。反应的热化学方程式为
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐1】(1)肼(N2H4)又称联氨,在常温下是一种可燃性的液体,可用作火箭燃料。已知在101 kPa时,1 g N2H4在氧气中完全燃烧生成氮气和H2O,放出19.5 kJ热量(25℃时),表示N2H4燃烧的热化学方程式是:______________________________ 。
(2)在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(H2O2),当它们混合时,即产生大量的N2和水蒸气,并放出大量热。已知0.4 mol液态肼和足量液态H2O2反应,生成氮气和液态水,放出327.05 kJ的热量。写出该反应的热化学方程式:____________________________ 。
(2)在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(H2O2),当它们混合时,即产生大量的N2和水蒸气,并放出大量热。已知0.4 mol液态肼和足量液态H2O2反应,生成氮气和液态水,放出327.05 kJ的热量。写出该反应的热化学方程式:
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐2】计算题
(1)硅粉与HCl在300 ℃时反应生成1 mol SiHCl3气体和H2,放出225 kJ热量,该反应的热化学方程式为:_______ 。
(2)将SiCl4氢化为SiHCl3有三种方法,对应的反应依次为:
①SiCl4(g)+H2(g) SiHCl(g)+HCl(g) ΔH1>0
SiHCl(g)+HCl(g) ΔH1>0
②3SiCl4(g)+2H2(g)+Si(s) 4SiHCl3(g) ΔH2<0
4SiHCl3(g) ΔH2<0
③2SiCl4(g)+H2(g)+Si(s)+HCl(g) 3SiHCl3(g) ΔH3
3SiHCl3(g) ΔH3
反应③的ΔH3=_______ (用ΔH1、ΔH2表示)。
(3)实现反应 对减少温室气体排放和减缓燃料危机具有重要意义。
对减少温室气体排放和减缓燃料危机具有重要意义。
已知:

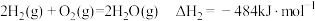

则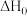 =
=_______  。
。
(4)我国是个钢铁大国,钢铁产量为世界第一,高炉炼铁是最为普遍的炼铁方法高炉内可能发生的反应:
①C(s) +O2(g)=CO2(g) △H1=-393.5kJ/mol
②C(s) + CO2(g)= 2CO(g) △H2=+172.5 kJ/mol
③4CO(g) + Fe3O4(s)=4CO2(g)+3Fe(s) △H3=-13.7 kJ/mol
则:3Fe(s)+2O2(g)= Fe3O4(s) △H=_______ 。
(1)硅粉与HCl在300 ℃时反应生成1 mol SiHCl3气体和H2,放出225 kJ热量,该反应的热化学方程式为:
(2)将SiCl4氢化为SiHCl3有三种方法,对应的反应依次为:
①SiCl4(g)+H2(g)
 SiHCl(g)+HCl(g) ΔH1>0
SiHCl(g)+HCl(g) ΔH1>0②3SiCl4(g)+2H2(g)+Si(s)
 4SiHCl3(g) ΔH2<0
4SiHCl3(g) ΔH2<0③2SiCl4(g)+H2(g)+Si(s)+HCl(g)
 3SiHCl3(g) ΔH3
3SiHCl3(g) ΔH3反应③的ΔH3=
(3)实现反应
 对减少温室气体排放和减缓燃料危机具有重要意义。
对减少温室气体排放和减缓燃料危机具有重要意义。已知:

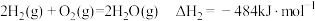

则
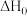 =
= 。
。(4)我国是个钢铁大国,钢铁产量为世界第一,高炉炼铁是最为普遍的炼铁方法高炉内可能发生的反应:
①C(s) +O2(g)=CO2(g) △H1=-393.5kJ/mol
②C(s) + CO2(g)= 2CO(g) △H2=+172.5 kJ/mol
③4CO(g) + Fe3O4(s)=4CO2(g)+3Fe(s) △H3=-13.7 kJ/mol
则:3Fe(s)+2O2(g)= Fe3O4(s) △H=
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
解题方法
【推荐3】(1)已知常温下, 乙醇
乙醇 和一定量的氧气混合后点燃,恰好完全燃烧,放出
和一定量的氧气混合后点燃,恰好完全燃烧,放出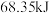 热量,则该反应的热化学方程式为
热量,则该反应的热化学方程式为________ 。
(2)已知:
硅晶体中每个硅原子和其他4个硅原子形成4个共价键,工业上制取高纯硅的反应方程式为
 ,该反应的反应热为
,该反应的反应热为________  。
。
(3)已知水的比热容为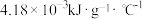 。
。 硫黄在
硫黄在 中完全燃烧生成气态
中完全燃烧生成气态 时放出的热量能使
时放出的热量能使 的温度由18℃升高至62.4℃,则硫黄的燃烧热为
的温度由18℃升高至62.4℃,则硫黄的燃烧热为________ (保留三位有效数字),热化学方程式为________ 。
 乙醇
乙醇 和一定量的氧气混合后点燃,恰好完全燃烧,放出
和一定量的氧气混合后点燃,恰好完全燃烧,放出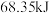 热量,则该反应的热化学方程式为
热量,则该反应的热化学方程式为(2)已知:
| 化学键 |  |  |  |  |
键能/ | 360 | 436 | 431 | 176 |
硅晶体中每个硅原子和其他4个硅原子形成4个共价键,工业上制取高纯硅的反应方程式为
 ,该反应的反应热为
,该反应的反应热为 。
。(3)已知水的比热容为
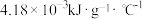 。
。 硫黄在
硫黄在 中完全燃烧生成气态
中完全燃烧生成气态 时放出的热量能使
时放出的热量能使 的温度由18℃升高至62.4℃,则硫黄的燃烧热为
的温度由18℃升高至62.4℃,则硫黄的燃烧热为
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐1】随着化石能源的减少,新能源的开发利用需求日益迫切。Bunsen热化学循环制氢工艺由下列三个反应组成:
SO2(g)+I2(g)+2H2O(g)=2HI(g)+H2SO4(l) △H=a kJ·mol-1
2H2SO4(l)=2H2O(g)+2SO2(g)+O2(g) △H=b kJ·mol-1
2HI(g)=H2(g)+I2(g) △H=c kJ·mol-1则:2H2O(g)=2H2(g)+O2(g) △H=__________
SO2(g)+I2(g)+2H2O(g)=2HI(g)+H2SO4(l) △H=a kJ·mol-1
2H2SO4(l)=2H2O(g)+2SO2(g)+O2(g) △H=b kJ·mol-1
2HI(g)=H2(g)+I2(g) △H=c kJ·mol-1则:2H2O(g)=2H2(g)+O2(g) △H=
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐2】在25 ℃、101 kPa时,C8H18在12.5 mol O2中完全燃烧生成CO2和 H2O(l)放出5518 kJ的热量。
(1)C8H18的燃烧热为__________ ,表示C8H18燃烧热的热化学方程式为_________________ 。
(2)若1 g水蒸气转化为液态水放热2.444 kJ,则 1molC8H18完全燃烧生成气态水时,放出的热量为______________ 。
(1)C8H18的燃烧热为
(2)若1 g水蒸气转化为液态水放热2.444 kJ,则 1molC8H18完全燃烧生成气态水时,放出的热量为
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐1】(1)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为____________________ 。
(2)已知: 2Fe(s)+O2(g)=2FeO(s) ΔH=-544.0kJ·mol-1
4Al(s)+3O2(g)=2Al2O3(s) ΔH=-3351.4kJ·mol-1
则Al和FeO发生铝热反应的热化学方程式为:_______________________ 。
(2)已知: 2Fe(s)+O2(g)=2FeO(s) ΔH=-544.0kJ·mol-1
4Al(s)+3O2(g)=2Al2O3(s) ΔH=-3351.4kJ·mol-1
则Al和FeO发生铝热反应的热化学方程式为:
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐2】氮的固定一直是科学家研究的重要课题,合成氨是人工固氮比较成熟的技术,其原理为 。已知破坏
。已知破坏 有关化学键需要的能量如表所示:
有关化学键需要的能量如表所示:
则反应生成
 所释放出的热量为
所释放出的热量为________  。
。
 。已知破坏
。已知破坏 有关化学键需要的能量如表所示:
有关化学键需要的能量如表所示: |  |  |  |
 |  |  |  |
则反应生成

 所释放出的热量为
所释放出的热量为 。
。
您最近一年使用:0次

 键的键能为
键的键能为 ,
, 键的键能为
键的键能为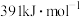 ,根据热化学方程式:
,根据热化学方程式: ,则
,则

