A、B、C、D、E五种物质中均含有同一种非金属元素,它们能发生如图所示的转化关系,该元素(用R)表示)的单质能与NaOH溶液反应生成盐(Na2RO3)和氢气.

(1)写出各物质的化学式:A____ ;C____ .
(2)写出反应①的化学方程式___ 该反应中氧化剂与还原剂的物质的量之比为___ .
(3)写出反应④的离子方程式:_____ .
(4)写出反应⑤的离子方程式_____ .
(5)H2CO3的酸性强于E的酸性,请用离子方程式予以证明:____ .

(1)写出各物质的化学式:A
(2)写出反应①的化学方程式
(3)写出反应④的离子方程式:
(4)写出反应⑤的离子方程式
(5)H2CO3的酸性强于E的酸性,请用离子方程式予以证明:
更新时间:2020-08-28 09:35:33
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】现有A、B、C、D四种不相同的化合物,已知它们均能溶于水,所得溶液中的阳离子含有 、
、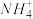 、
、 、
、 、
、 ,阴离子含有
,阴离子含有 、
、 、
、 。现将它们分别配成0.1mol/L的溶液,常温下进行如下实验:
。现将它们分别配成0.1mol/L的溶液,常温下进行如下实验:
①做焰色试验时,透过蓝色钻玻璃观察只有溶液B和溶液D的火焰为紫色;
②测得溶液A显碱性,溶液B显酸性;
③溶液A和溶液B混合,只有白色沉淀生成,且沉淀不溶解;
④向溶液C中滴加溶液A,先出现白色絮状沉淀,后变为灰绿色,最终变为红褐色;同时产生刺激性气味的气体;
⑤溶液B和溶液C混合无明显现象:
⑥向溶液D中滴加溶液B,只产生无色无味的气体。根据上述实验现象。
回答下列问题:
(1)写出下列物质的化学式:A_______ ,C_______ 。
(2)溶液B的pH=_______ 。
(3)实验③中,溶液A和溶液B混合显中性时,反应的离子方程式为_______ 。
(4)实验④中,向溶液C中滴加过量溶液A时,反应的离子方程式为_______ 。
(5)溶液B和溶液D反应的离子方程式为_______ 。
(6)溶液C在空气中长时间露置会变质,检验其是否变质的方法是_______ 。
 、
、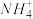 、
、 、
、 、
、 ,阴离子含有
,阴离子含有 、
、 、
、 。现将它们分别配成0.1mol/L的溶液,常温下进行如下实验:
。现将它们分别配成0.1mol/L的溶液,常温下进行如下实验:①做焰色试验时,透过蓝色钻玻璃观察只有溶液B和溶液D的火焰为紫色;
②测得溶液A显碱性,溶液B显酸性;
③溶液A和溶液B混合,只有白色沉淀生成,且沉淀不溶解;
④向溶液C中滴加溶液A,先出现白色絮状沉淀,后变为灰绿色,最终变为红褐色;同时产生刺激性气味的气体;
⑤溶液B和溶液C混合无明显现象:
⑥向溶液D中滴加溶液B,只产生无色无味的气体。根据上述实验现象。
回答下列问题:
(1)写出下列物质的化学式:A
(2)溶液B的pH=
(3)实验③中,溶液A和溶液B混合显中性时,反应的离子方程式为
(4)实验④中,向溶液C中滴加过量溶液A时,反应的离子方程式为
(5)溶液B和溶液D反应的离子方程式为
(6)溶液C在空气中长时间露置会变质,检验其是否变质的方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】硫酸亚铁(FeSO4)是中学化学常用试剂,可用于治疗缺铁性贫血症。
(1)实验室配备FeSO4溶液时为防止硫酸亚铁变质,常采用的措施是_______ (填一种)。
(2)以FeSO4为原料可制备碱式硫酸铁 、铁红、硫酸亚铁铵[
、铁红、硫酸亚铁铵[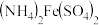 ,俗名摩尔盐],转化关系如图1所示。
,俗名摩尔盐],转化关系如图1所示。

①制备 时,若pH过高会导致碱式硫酸铁的产率偏低,其原因是
时,若pH过高会导致碱式硫酸铁的产率偏低,其原因是_______ 。
②制备 时,向FeSO4溶液中加入过量的
时,向FeSO4溶液中加入过量的 溶液,该反应的离子方程式为
溶液,该反应的离子方程式为_______ ;铁红的化学式为_______ 。
③制备摩尔盐时将反应物混合,经蒸发浓缩、冷却结晶、_______ 、洗涤、干燥得到产品。
(3)隔绝空气条件下,FeSO4分解时的物质转化关系如图2。

①关于M的成分提出三种猜想:
猜想1:M是 ;
;
猜想2:M是_______ ;
猜想3:M是 和
和 。
。
②已知三种气体的部分性质如表所示:
利用图3装置探究硫酸亚铁部分分解产物。能否将低温浴槽A的温度控制在 ?
?_______ (填“能”或“否”)。C中试剂可能是_______ 。

(1)实验室配备FeSO4溶液时为防止硫酸亚铁变质,常采用的措施是
(2)以FeSO4为原料可制备碱式硫酸铁
 、铁红、硫酸亚铁铵[
、铁红、硫酸亚铁铵[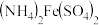 ,俗名摩尔盐],转化关系如图1所示。
,俗名摩尔盐],转化关系如图1所示。
①制备
 时,若pH过高会导致碱式硫酸铁的产率偏低,其原因是
时,若pH过高会导致碱式硫酸铁的产率偏低,其原因是②制备
 时,向FeSO4溶液中加入过量的
时,向FeSO4溶液中加入过量的 溶液,该反应的离子方程式为
溶液,该反应的离子方程式为③制备摩尔盐时将反应物混合,经蒸发浓缩、冷却结晶、
(3)隔绝空气条件下,FeSO4分解时的物质转化关系如图2。

①关于M的成分提出三种猜想:
猜想1:M是
 ;
;猜想2:M是
猜想3:M是
 和
和 。
。②已知三种气体的部分性质如表所示:
| 物质 |  |  |  |
| 熔点/℃ | 16.8 |  |  |
| 沸点/℃ | 44.8 |  |  |
 ?
?
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某同学称取一定质量的 固体配成溶液,在该溶液中加入50mL 0.1 mol/L的盐酸,然后向此混合溶液中逐滴加入0.2 mol/L的NaOH溶液(如图甲所示)。滴加过程中产生的沉淀的质量与加入的NaOH溶液体积的关系如图乙所示。
固体配成溶液,在该溶液中加入50mL 0.1 mol/L的盐酸,然后向此混合溶液中逐滴加入0.2 mol/L的NaOH溶液(如图甲所示)。滴加过程中产生的沉淀的质量与加入的NaOH溶液体积的关系如图乙所示。

请回答下列问题:
(1)溶解 固体所用的玻璃仪器有
固体所用的玻璃仪器有___________ (填字母)。
a.天平 b.烧杯 c.漏斗 d.玻璃棒
(2)OA段反应的离子方程式为___________ 。
(3)AB段反应的离子方程式为___________ 。
(4)B点的数值是___________ 。
 固体配成溶液,在该溶液中加入50mL 0.1 mol/L的盐酸,然后向此混合溶液中逐滴加入0.2 mol/L的NaOH溶液(如图甲所示)。滴加过程中产生的沉淀的质量与加入的NaOH溶液体积的关系如图乙所示。
固体配成溶液,在该溶液中加入50mL 0.1 mol/L的盐酸,然后向此混合溶液中逐滴加入0.2 mol/L的NaOH溶液(如图甲所示)。滴加过程中产生的沉淀的质量与加入的NaOH溶液体积的关系如图乙所示。
请回答下列问题:
(1)溶解
 固体所用的玻璃仪器有
固体所用的玻璃仪器有a.天平 b.烧杯 c.漏斗 d.玻璃棒
(2)OA段反应的离子方程式为
(3)AB段反应的离子方程式为
(4)B点的数值是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】为探究矿物(含三种常见元素)的组成和性质,某兴趣小组设计了如下实验:

已知实验中所用试剂均足量,请回答如下问题:
(1)X所含的元素为___________ 。
(2)气体A与溴水反应的离子方程式是___________ 。
(3)X在高温下与氧气充分反应的化学方程式是___________ 。
(4)检验溶液G中的金属阳离子的实验方案是___________ 。

已知实验中所用试剂均足量,请回答如下问题:
(1)X所含的元素为
(2)气体A与溴水反应的离子方程式是
(3)X在高温下与氧气充分反应的化学方程式是
(4)检验溶液G中的金属阳离子的实验方案是
您最近一年使用:0次
【推荐2】为探究无水盐X(仅含5种元素)的组成和性质,设计并完成如下实验:

请回答:
(1)组成X的5种元素符号是H、N___________ ;X的化学式是___________ 。
(2)写出向X溶液中加入足量的浓Ba(OH)2溶液并微热的离子方程式___________ 。
(3)写出检验X中金属阳离子的实验操作和现象:___________ 。

请回答:
(1)组成X的5种元素符号是H、N
(2)写出向X溶液中加入足量的浓Ba(OH)2溶液并微热的离子方程式
(3)写出检验X中金属阳离子的实验操作和现象:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】下图为各单质与化合物之间的转化关系,单质及化合物的组成元素均为常见的短周期元素。请回答:

(1)若沉淀丁不溶于过量的盐酸,单质A为_______ 。若沉淀丁能溶于过量的盐酸,化合物甲为_______ 。
(2)单质B的化学式为_______ ,丙的电子式为_______ 。
(3)若沉淀丁不溶于过量的盐酸,写出A和NaOH溶液反应的化学方程式:_______ 。
(4)KMnO4是重要的氧化剂,在双氧水中滴加少量用稀硫酸酸化的KMnO4溶液,溶液迅速变为无色,同时生成单质B。写出该反应的离子方程式_______ 。
(5)单质B的同素异体与Na2FeO4同是良好的消毒剂,在新冠疫情防控中作用巨大。在碱性条件下,利用NaClO氧化硝酸铁,制得Na2FeO4,该反应的离子反应方程式为_______ 。

(1)若沉淀丁不溶于过量的盐酸,单质A为
(2)单质B的化学式为
(3)若沉淀丁不溶于过量的盐酸,写出A和NaOH溶液反应的化学方程式:
(4)KMnO4是重要的氧化剂,在双氧水中滴加少量用稀硫酸酸化的KMnO4溶液,溶液迅速变为无色,同时生成单质B。写出该反应的离子方程式
(5)单质B的同素异体与Na2FeO4同是良好的消毒剂,在新冠疫情防控中作用巨大。在碱性条件下,利用NaClO氧化硝酸铁,制得Na2FeO4,该反应的离子反应方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系:

(1)若B是气态氢化物。C、D是氧化物且会造成光化学烟雾污染。写③反应的化学方程式_________ 。
(2)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体。写④反应离子方程式_________________________________ 。
(3)若A是太阳能电池用的光伏材料。C、D为钠盐,两种物质中除钠、氧外的元素均为同一主族,且溶液均显碱性。写出②反应的化学方程式_____________________________ 。
(4)若A是当今应用最广泛的金属。④反应用到A,②⑤反应均用到同一种非金属单质。C的溶液用于蚀刻印刷铜电路板,写出该反应的离子方程式____________________________________ 。

(1)若B是气态氢化物。C、D是氧化物且会造成光化学烟雾污染。写③反应的化学方程式
(2)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体。写④反应离子方程式
(3)若A是太阳能电池用的光伏材料。C、D为钠盐,两种物质中除钠、氧外的元素均为同一主族,且溶液均显碱性。写出②反应的化学方程式
(4)若A是当今应用最广泛的金属。④反应用到A,②⑤反应均用到同一种非金属单质。C的溶液用于蚀刻印刷铜电路板,写出该反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】含A元素的一种单质是一种重要的半导体材料,含 A元素的一种化合物C可用于制造高性能的现代通讯材料——光导纤维,C与烧碱反应生成含A元素的化合物D。
(1)在元素周期表中,A位于________ 族,与A同族但相对原子质量比A小的元素B的原子结构示意图为________ ,A与B在原子的电子层结构上的相同点是______________________________________ 。
(2)易与C发生化学反应的酸是________ (写名称),反应的化学方程式是__________________________ 。
(3)将C与纯碱混合高温熔融时也发生化学反应生成D,同时还生成B的最高价氧化物E;将全部的E与全部的D在足量的水中混合后,又发生化学反应生成含A的化合物F。
①写出生成D和F的化学反应方程式:______________________________________________ 。
②要将纯碱高温熔化,下列坩埚中可选用的是________ 。
A.普通玻璃坩埚 B.石英玻璃坩埚
C.氧化铝坩埚 D.铁坩埚
(4)100 g C与石灰石的混合物充分反应后,生成的气体在标准状况下的体积为11.2 L,100 g混合物中石灰石的质量分数是________ 。
(1)在元素周期表中,A位于
(2)易与C发生化学反应的酸是
(3)将C与纯碱混合高温熔融时也发生化学反应生成D,同时还生成B的最高价氧化物E;将全部的E与全部的D在足量的水中混合后,又发生化学反应生成含A的化合物F。
①写出生成D和F的化学反应方程式:
②要将纯碱高温熔化,下列坩埚中可选用的是
A.普通玻璃坩埚 B.石英玻璃坩埚
C.氧化铝坩埚 D.铁坩埚
(4)100 g C与石灰石的混合物充分反应后,生成的气体在标准状况下的体积为11.2 L,100 g混合物中石灰石的质量分数是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】下图所示转化关系中涉及到的物质均由主族元素组成(部分产物已略去),其中C、D为单质,A、B、E、F、G为化合物,除C与D的反应外,其它反应均在溶液中进行。请填写下列空白。
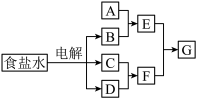
(1) 若A是常见的金属或金属氧化物,当F过量时,G为可溶性盐,则A的化学式为_________ 或_________ 。
(2) 若A是一种常见氧化物,不管F过量与否,G为同一种难溶性物质,则A的名称是________ ,晶体类型是_______ ,A的用途是_________ 。
(3) 若A是一种具有漂白性的气态氧化物,A是___ ;若A是一种无味的气态氧化物,A的电子式为______ 。
(4) 若A为有机化合物,如果A与G为同一物质,请写出两种A(不同类别物质)的结构简式:_____ ;_____ 。

(1) 若A是常见的金属或金属氧化物,当F过量时,G为可溶性盐,则A的化学式为
(2) 若A是一种常见氧化物,不管F过量与否,G为同一种难溶性物质,则A的名称是
(3) 若A是一种具有漂白性的气态氧化物,A是
(4) 若A为有机化合物,如果A与G为同一物质,请写出两种A(不同类别物质)的结构简式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E、F六种短周期元素,原子序数依次增大。A是地壳中含量最高的元素,C是地壳中含量最高的金属元素,A、E同主族。D元素原子最外层电子数是次外层电子数的一半。B、C两元素原子的最外层电子数之和等于D元素原子的最外层电子数,C、D两元素原子最外层电子数之和等于F元素原子的最外层电子数。回答下列问题:
(1)元素A在元素周期表中的位置是______ 。
(2)写出B、E两元素形成化合物的电子式:______ ,所含化学键类型______ ;
(3)A、D、E、F的气态氢化物的稳定性顺序______ (用化学式表示);
(4)写出C、E对应的最高价氧化物的水化物相互反应的化学方程式为:______ ;
(5)C、D的氧化物与分别与B的氢氧化物反应的离子方程式:______ 、______ 。
(1)元素A在元素周期表中的位置是
(2)写出B、E两元素形成化合物的电子式:
(3)A、D、E、F的气态氢化物的稳定性顺序
(4)写出C、E对应的最高价氧化物的水化物相互反应的化学方程式为:
(5)C、D的氧化物与分别与B的氢氧化物反应的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】镓是我国战略储备金属之一,在电子通信、新能源、芯片、军工等领域有着重要应用。某废渣粉煤灰主要含有Al2O3、SiO2,还有少量的Fe2O3、Ga2O3,一种从中提取镓的工艺流程如图:

样已知:①碱浸液中铝、镓元素分别以AlO 、GaO
、GaO 形式存在;
形式存在;
②常温下Al(OH)3(s)+OH-(aq) AlO
AlO (aq)+2H2O(l),平衡常数K=100.63。回答下列问题:
(aq)+2H2O(l),平衡常数K=100.63。回答下列问题:
(1)粉煤灰需“球磨”至40目筛子(孔径为0.425mm的漏筛)漏出再焙烧,目的是_____ 。
(2)“焙烧”时碳酸钠与SiO2反应的化学方程式为_____ 。
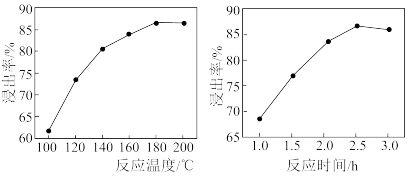
(3)“碱浸”时镓的浸出率随温度、时间变化如图所示,反应适宜的温度为_____ ,时间为____ 。
(4)“沉铝”时,物质X是_____ (填名称),过程中若要使铝元素在常温下恰好沉淀完全(含Al物质浓度恰好为10-5mol/L),计算此时溶液的c(OH-)=_____ (写出计算过程)。
(5)写出解析过程中GaO 被H2SO4解析为Ga3+的离子方程式:
被H2SO4解析为Ga3+的离子方程式:_____ 。

样已知:①碱浸液中铝、镓元素分别以AlO
 、GaO
、GaO 形式存在;
形式存在;②常温下Al(OH)3(s)+OH-(aq)
 AlO
AlO (aq)+2H2O(l),平衡常数K=100.63。回答下列问题:
(aq)+2H2O(l),平衡常数K=100.63。回答下列问题:(1)粉煤灰需“球磨”至40目筛子(孔径为0.425mm的漏筛)漏出再焙烧,目的是
(2)“焙烧”时碳酸钠与SiO2反应的化学方程式为
(3)“碱浸”时镓的浸出率随温度、时间变化如图所示,反应适宜的温度为

(4)“沉铝”时,物质X是
(5)写出解析过程中GaO
 被H2SO4解析为Ga3+的离子方程式:
被H2SO4解析为Ga3+的离子方程式:
您最近一年使用:0次




