铜是生活中常见的金属,请回答下列问题:
(1)Cu不活泼,通常情况下不与稀硫酸反应,但向Cu和稀硫酸的混合物中滴入H2O2溶液后,溶液很快变蓝色,试写出该反应的离子方程式:__________ 。
(2)将硫酸铜溶液和碳酸钠溶液混合,会析出Cu2(OH)2CO3绿色固体,试写出该反应的离子方程式:_________ 。
(3)火法炼铜的原理为Cu2S+O2 2Cu+SO2,在该反应中每生成1 mol Cu,转移
2Cu+SO2,在该反应中每生成1 mol Cu,转移________ mol e-。
(4)据报道,有一种叫Thibacillus Ferroxidans的细菌在有氧气存在的酸性溶液中,可将黄铜矿CuFeS2氧化成硫酸盐:4CuFeS2+2H2SO4+17O2=4CuSO4+2Fe2(SO4)3+2H2O。利用反应后的溶液,按如下流程可制备胆矾(CuSO4·5H2O):
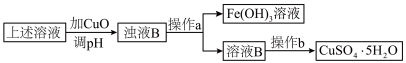
①检验溶液B中Fe3+是否被除尽的实验方法:__________ 。
②在实验室中,设计两个原理不同的方案,从溶液B中提炼金属铜(要求:一种方案只用一个反应来完成)。写出两种方案中涉及的化学方程式:
方案一_________ ;方案二_________ 。
(1)Cu不活泼,通常情况下不与稀硫酸反应,但向Cu和稀硫酸的混合物中滴入H2O2溶液后,溶液很快变蓝色,试写出该反应的离子方程式:
(2)将硫酸铜溶液和碳酸钠溶液混合,会析出Cu2(OH)2CO3绿色固体,试写出该反应的离子方程式:
(3)火法炼铜的原理为Cu2S+O2
 2Cu+SO2,在该反应中每生成1 mol Cu,转移
2Cu+SO2,在该反应中每生成1 mol Cu,转移(4)据报道,有一种叫Thibacillus Ferroxidans的细菌在有氧气存在的酸性溶液中,可将黄铜矿CuFeS2氧化成硫酸盐:4CuFeS2+2H2SO4+17O2=4CuSO4+2Fe2(SO4)3+2H2O。利用反应后的溶液,按如下流程可制备胆矾(CuSO4·5H2O):

①检验溶液B中Fe3+是否被除尽的实验方法:
②在实验室中,设计两个原理不同的方案,从溶液B中提炼金属铜(要求:一种方案只用一个反应来完成)。写出两种方案中涉及的化学方程式:
方案一
2020高三·全国·专题练习 查看更多[1]
(已下线)第12讲 镁、铝、铜及其化合物 金属冶炼(精练)——2021年高考化学一轮复习讲练测
更新时间:2020-08-28 10:45:04
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】AgNO3为中学常用化学试剂,某学习小组研究其性质。
(1)测量 0.1 mol/LAgNO3溶液pH值为4,用离子方程式解释其原因___________ 。
(2)AgSCN为白色沉淀,设计实验证明Ksp(AgSCN)>Ksp(AgI),完善以下实验步骤:
取0.1 mL1 mol/L AgNO3溶液于洁净的试管中,加入___________ ,振荡,再加入___________ ,振荡,观察到白色沉淀变成黄色,则证明上述结论。
探究一:证明AgNO3具有氧化性
(3)往4 mL0.1 mol/L(NH4)2Fe(SO4)2 [pH≈2]溶液中滴加几滴___________ ,把混合溶液均分到加a、b两支试管中。同学甲往a试管中滴加少量0.1 mol/L AgNO3溶液,观察到产生少量白色沉淀和___________ (填实验现象),证明AgNO3具有氧化性。
(4)同学乙认为:氧化Fe2+的,可能是Ag+,也可能是 。若向b试管中滴加少量“检测试剂”,无明显现象,则证明氧化剂为Ag+。写出这种“检测试剂”的配方:
。若向b试管中滴加少量“检测试剂”,无明显现象,则证明氧化剂为Ag+。写出这种“检测试剂”的配方:___________ 。
探究二:AgNO3溶液与过量 铁粉的反应
向酸化的0.1 mol/L AgNO3溶液[pH≈2]中加入过量铁粉,搅拌后静置,随着反应进行,在不同时间取上层清液,滴加KSCN溶液,溶液变红,同时有白色沉淀生成,且溶液颜色深浅、沉淀量多少与取样时间有关,对比实验记录如下:
(5)用离子方程式解释实验中①出现红色的原因: ,
,___________ ,___________ 。
(6)解释实验②的现象:___________ 。
(7)用离子方程式解释实验③中红色变浅的原因:___________ 。
(1)测量 0.1 mol/LAgNO3溶液pH值为4,用离子方程式解释其原因
(2)AgSCN为白色沉淀,设计实验证明Ksp(AgSCN)>Ksp(AgI),完善以下实验步骤:
取0.1 mL1 mol/L AgNO3溶液于洁净的试管中,加入
探究一:证明AgNO3具有氧化性
(3)往4 mL0.1 mol/L(NH4)2Fe(SO4)2 [pH≈2]溶液中滴加几滴
(4)同学乙认为:氧化Fe2+的,可能是Ag+,也可能是
 。若向b试管中滴加少量“检测试剂”,无明显现象,则证明氧化剂为Ag+。写出这种“检测试剂”的配方:
。若向b试管中滴加少量“检测试剂”,无明显现象,则证明氧化剂为Ag+。写出这种“检测试剂”的配方:探究二:AgNO3溶液与
向酸化的0.1 mol/L AgNO3溶液[pH≈2]中加入过量铁粉,搅拌后静置,随着反应进行,在不同时间取上层清液,滴加KSCN溶液,溶液变红,同时有白色沉淀生成,且溶液颜色深浅、沉淀量多少与取样时间有关,对比实验记录如下:
| 序号 | 取样时间/min | 现象 |
| ① | 3 | 产生大量白色沉淀;溶液呈红色 |
| ② | 30 | 产生白色沉淀,较3 min时量少;溶液红色较3 min时加深 |
| ③ | 120 | 产生白色沉淀,较30 min时量少;溶液红色较30 min时变浅 |
 ,
,(6)解释实验②的现象:
(7)用离子方程式解释实验③中红色变浅的原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】生铁中含有一种铁碳化合物 X(Fe3C)。X 在足量的空气中高温煅烧,生成有磁性的固体Y,回答下列问题:
(1)将 Y 溶于过量盐酸,写出离子方程式_____ 。
(2)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等四种离子,向其中加入过量的NaOH 溶液后,过滤,将滤渣高温灼烧并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是_____ 。
(3)设计实验,鉴别固体Y 中既有 Fe2+ ,又有 Fe3+________________
(1)将 Y 溶于过量盐酸,写出离子方程式
(2)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等四种离子,向其中加入过量的NaOH 溶液后,过滤,将滤渣高温灼烧并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是
(3)设计实验,鉴别固体Y 中既有 Fe2+ ,又有 Fe3+
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】铁及其化合物在生产生活中有极其重要的用途,请回答下列问题:
(1) 溶液可用于刻蚀铜制电路板,该反应的离子方程式为
溶液可用于刻蚀铜制电路板,该反应的离子方程式为________ 。
(2)要实现 转化为
转化为 ,可选用足量的
,可选用足量的________ (填字母)。
①亚硫酸钠溶液 ②稀盐酸 ③酸性 溶液 ④铁粉 ⑤碘化钾溶液 ⑥过氧化氢溶液
溶液 ④铁粉 ⑤碘化钾溶液 ⑥过氧化氢溶液
(3)某补铁口服液中含有 ,为检验其是否被氧化变质,可取少量该口服液,向其中滴加
,为检验其是否被氧化变质,可取少量该口服液,向其中滴加________ ,若溶液变为_____ 色,则说明其已变质。向该口服液中加入维生素C可防止其被氧化变质,利用了维生素C的_____ 性。
(4)激光打印机的墨粉中含有 。
。 溶于过量的稀盐酸,反应的离子方程式为
溶于过量的稀盐酸,反应的离子方程式为___________ 。往反应后的溶液中滴加少量酸性 溶液,酸性
溶液,酸性 溶液褪色,
溶液褪色,_____ (填“能或不能”)说明反应后的溶液中含 。若不能,请说明原因:
。若不能,请说明原因:___________ 。
(5)高铁酸盐可作为饮用水的消毒剂和净水剂,工业上以 、
、 、
、 为原料制备高铁酸钾。
为原料制备高铁酸钾。
①高铁酸钠 中Fe的化合价为
中Fe的化合价为_____ 。
②配平制备 的离子方程式:
的离子方程式:______
__ +__
+__ +__=__
+__=__ +__
+__ +__
+__
每生成39.6g ,转移电子的数目为
,转移电子的数目为_____ 。
③已知 ,说明高铁酸盐既可作饮用水的消毒剂又可作净水剂的原因
,说明高铁酸盐既可作饮用水的消毒剂又可作净水剂的原因___________ 。
(1)
 溶液可用于刻蚀铜制电路板,该反应的离子方程式为
溶液可用于刻蚀铜制电路板,该反应的离子方程式为(2)要实现
 转化为
转化为 ,可选用足量的
,可选用足量的①亚硫酸钠溶液 ②稀盐酸 ③酸性
 溶液 ④铁粉 ⑤碘化钾溶液 ⑥过氧化氢溶液
溶液 ④铁粉 ⑤碘化钾溶液 ⑥过氧化氢溶液(3)某补铁口服液中含有
 ,为检验其是否被氧化变质,可取少量该口服液,向其中滴加
,为检验其是否被氧化变质,可取少量该口服液,向其中滴加(4)激光打印机的墨粉中含有
 。
。 溶于过量的稀盐酸,反应的离子方程式为
溶于过量的稀盐酸,反应的离子方程式为 溶液,酸性
溶液,酸性 溶液褪色,
溶液褪色, 。若不能,请说明原因:
。若不能,请说明原因:(5)高铁酸盐可作为饮用水的消毒剂和净水剂,工业上以
 、
、 、
、 为原料制备高铁酸钾。
为原料制备高铁酸钾。①高铁酸钠
 中Fe的化合价为
中Fe的化合价为②配平制备
 的离子方程式:
的离子方程式:__
 +__
+__ +__=__
+__=__ +__
+__ +__
+__
每生成39.6g
 ,转移电子的数目为
,转移电子的数目为③已知
 ,说明高铁酸盐既可作饮用水的消毒剂又可作净水剂的原因
,说明高铁酸盐既可作饮用水的消毒剂又可作净水剂的原因
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】不法商人,常以假乱真,市场上出现了假金(含有Cu),检验假金可选用的试剂是_________ (填 “HCl” 或 “HNO3”);碳酸氢钠(NaHCO3)俗名为____________ (填 “苏打” 或 “小苏打”)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,反应方程式可为:Cu+HNO3→Cu(NO3)2+NO↑+NO2↑+H2O(不考虑2NO2 N2O4)。
N2O4)。
(1)硝酸在该反应中的作用是___________ ,该反应的还原产物是___________ 。
(2)0.3mol Cu被硝酸完全溶解后,Cu失去的电子数是___________ ,如果到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是___________ ,若用排水法收集这些气体,可得标准状况下的气体___________ L。
(3)如果参加反应的Cu和HNO3的物质的量之比是3:10,写出该反应的离子方程式,同时标出电子转移的方向和数量___________
(4)将32.0g Cu投入50mL 12mol/L的浓硝酸中,充分反应后,收集到4.48L(标准状况)NO和NO2的混合气体。判断Cu和硝酸反应后何者有剩余?___________ ,剩余___________ mol。
 N2O4)。
N2O4)。(1)硝酸在该反应中的作用是
(2)0.3mol Cu被硝酸完全溶解后,Cu失去的电子数是
(3)如果参加反应的Cu和HNO3的物质的量之比是3:10,写出该反应的离子方程式,同时标出电子转移的方向和数量
(4)将32.0g Cu投入50mL 12mol/L的浓硝酸中,充分反应后,收集到4.48L(标准状况)NO和NO2的混合气体。判断Cu和硝酸反应后何者有剩余?
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】I.硝酸被称为“国防工业之母”是因为它是制取炸药的重要原料,可以氨气为原料,经一系列反应制得。
NH3 NO
NO NO2
NO2 HNO3。
HNO3。
(1)实验室可用加热浓氨水制备NH3,该反应的化学方程式为____ 。
(2)NH3与O2催化氧化反应中会得到副产物N2O,写出NH3与O2在加热和催化剂作用下生成N2O的化学方程式:____ 。
(3)NO2通入水中制备硝酸时,通常会通入适量的氧气,目的是___ 。
(4)工业生产中为了盛装大量浓硝酸,可选择___ 作为罐体材料。
(5)将12.8gCu与200mL一定浓度的硝酸反应,铜完全溶解,产生的混合气体(设产生的气体只有NO和NO2)在标准状况下的体积为4.48L,待产生的气体全部释放后,向溶液中加入100mL5mol·L-1氢氧化钠溶液,恰好使溶液中的铜离子全部转化成沉淀,原硝酸溶液的物质的量浓度为____ mol·L-1。
II.硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。甲、乙两位同学用铜和硫酸作原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即Cu→CuSO4
方案乙:Cu→CuO→CuSO4
(6)方案甲中,铜和浓硫酸发生反应的化学方程式是____ 。
(7)这两种方案,你认为哪一种方案更合理?____ 。理由是____ 。
NH3
 NO
NO NO2
NO2 HNO3。
HNO3。(1)实验室可用加热浓氨水制备NH3,该反应的化学方程式为
(2)NH3与O2催化氧化反应中会得到副产物N2O,写出NH3与O2在加热和催化剂作用下生成N2O的化学方程式:
(3)NO2通入水中制备硝酸时,通常会通入适量的氧气,目的是
(4)工业生产中为了盛装大量浓硝酸,可选择
| A.铜 | B.铂 | C.铝 | D.镁 |
II.硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。甲、乙两位同学用铜和硫酸作原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即Cu→CuSO4
方案乙:Cu→CuO→CuSO4
(6)方案甲中,铜和浓硫酸发生反应的化学方程式是
(7)这两种方案,你认为哪一种方案更合理?
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)铜器表面有时会生成铜绿[Cu2(OH)2CO3],这层铜绿可用化学方法除去。试写出除去铜绿而不损伤器物的化学方程式 _________________________ 。
(2)工业上常用铝热反应产生的“铁水”来焊接铁轨,请写出铝热反应的化学方程式_________ 。
(3)冶金工业中,常用焦炭来冶炼铁。写出赤铁矿(Fe2O3)被CO还原成铁的化学方程式_____ 。
(2)工业上常用铝热反应产生的“铁水”来焊接铁轨,请写出铝热反应的化学方程式
(3)冶金工业中,常用焦炭来冶炼铁。写出赤铁矿(Fe2O3)被CO还原成铁的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】2023年10月央视的节目《只此青绿》,提到了颜料石绿{铜绿,又名孔雀石,主要成分是碱式碳酸铜[Cu2(OH)2CO3]}。某同学利用下述反应实现了“铜→铜绿→……→Cu”的转化。回答下列问题:
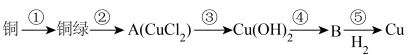
(1)铜在潮湿的空气中容易产生铜绿,写出此反应的化学方程式:______
(2)A、B在无色火焰上灼烧时,其焰色______ (填“相同”或“不相同”),该原理是______ (填“物理”或“化学”)变化。
(3)完成步骤②和③可选用的试剂分别为______ 、______ 。(填标号)
a.HCl溶液 b.NaCl溶液 c.NaOH溶液 d.KNO3溶液
(4)若在该转化过程中有2mol氧化铜生成,则该氧化铜的质量为多少______ ?(写出计算过程)
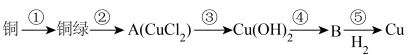
(1)铜在潮湿的空气中容易产生铜绿,写出此反应的化学方程式:
(2)A、B在无色火焰上灼烧时,其焰色
(3)完成步骤②和③可选用的试剂分别为
a.HCl溶液 b.NaCl溶液 c.NaOH溶液 d.KNO3溶液
(4)若在该转化过程中有2mol氧化铜生成,则该氧化铜的质量为多少
您最近一年使用:0次



