下列说法正确的是( )
A.若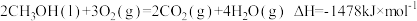 ,则CH3OH(l)的燃烧热为739kJ·mol-1 ,则CH3OH(l)的燃烧热为739kJ·mol-1 |
B.已知25℃、101KPa 下,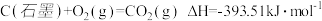 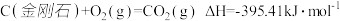 ,则石墨比金刚石更稳定 ,则石墨比金刚石更稳定 |
C.已知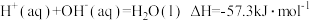 ,则20.0gNaOH固体与稀盐酸完全中和,放出28.65kJ的热量 ,则20.0gNaOH固体与稀盐酸完全中和,放出28.65kJ的热量 |
| D.中和热测定实验中,不可用环形铜质搅拌棒代替环形玻璃搅拌棒,实验至少需测3次温度 |
更新时间:2020-09-01 10:13:59
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】探究钠及其化合物的性质,下列方案设计、现象和结论都正确的是
| 实验方案 | 现象 | 结论 | |
| A | 将金属钠置于坩埚中燃烧,取燃烧后的少量固体粉末于试管中,加入 蒸馏水 蒸馏水 | 有气体生成 | 该固体粉末一定为 |
| B | 将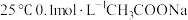 溶液加热到40℃,用传感器监测溶液 溶液加热到40℃,用传感器监测溶液 变化 变化 | 溶液的 逐渐减小 逐渐减小 | 随温度升高, 逐渐增大, 逐渐增大, 溶液中 溶液中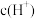 增大, 增大,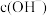 减小 减小 |
| C | 向 溶液中加入等体积等浓度的 溶液中加入等体积等浓度的 溶液 溶液 | 有白色沉淀生成 |  结合 结合 的能力强于 的能力强于 |
| D | 测定中和热时,将稀 溶液缓慢倒入到盛有稀 溶液缓慢倒入到盛有稀 的内筒,搅拌使其充分混合,再盖上杯盖 的内筒,搅拌使其充分混合,再盖上杯盖 | 温度差为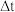 | 中和反应放热,将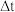 代入公式算得中和热( 代入公式算得中和热( ) ) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列关于中和热测定实验的说法不正确的是
| A.简易量热计的隔热层是为了减少实验过程中的热量损失 |
| B.使用玻璃搅拌器既可以搅拌又避免损坏温度计 |
| C.向盛装酸的烧杯中加碱时要小心缓慢 |
| D.测酸液温度后的温度计要用水清洗后再测碱液的温度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是( )
| A.甲烷的燃烧热为ΔH=-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1 |
| B.NaOH(aq)+CH3COOH(aq)===CH3COONa(aq)+H2O(l) ΔH=-57.3 kJ·mol-1(中和热) |
| C.测定盐酸和NaOH溶液反应的中和热时,每次实验均应测量3个温度,即盐酸起始温度、NaOH溶液起始温度和反应后终止温度 |
| D.2H2(g)+O2(g)===2H2O(l)ΔH=-571.6 kJ·mol-1(燃烧热) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某实验小组学生按照课本实验要求,用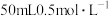 的盐酸与50mL
的盐酸与50mL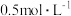 的NaOH溶液在右图所示的装置中进行中和反应通过测定反应
的NaOH溶液在右图所示的装置中进行中和反应通过测定反应
过程中所放出的热量,从而计算中和热。下列说法正确的是
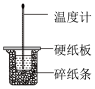
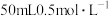 的盐酸与50mL
的盐酸与50mL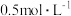 的NaOH溶液在右图所示的装置中进行中和反应通过测定反应
的NaOH溶液在右图所示的装置中进行中和反应通过测定反应过程中所放出的热量,从而计算中和热。下列说法正确的是

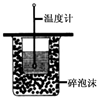
| A.实验过程中没有热量损失 |
| B.图中实验装置缺少环形玻璃搅拌棒 |
| C.烧杯间填满碎纸条的作用只是固定小烧杯 |
D.若改用 盐酸跟 盐酸跟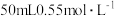 的NaOH溶液进行反应,从理论上来说,所求中和热不相等。 的NaOH溶液进行反应,从理论上来说,所求中和热不相等。 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列说法正确的是
| A.已知NaOH(aq)+HCl(aq) = NaCl(aq)+H2O(l) ΔH = - 57.3 kJ/mol ,则含有40.0g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3kJ的热量。 |
| B.已知2C(s)+2O2(g)=2CO2(g) ΔH=akJ/mol,2C(s)+2O2(g)=2CO (g) ΔH =b kJ/mol,则a>b。 |
| C.取50mL 0.55mol/LNaOH(aq)和50mL 0.50mol/L HCl(aq)进行中和热的测定实验,用温度计测定HCl(aq)起始温度后,直接测定NaOH(aq)的温度,会使中和热ΔH偏小 |
| D.已知P(白磷,s)=P(红磷,s) ΔH<0,则白磷比红磷稳定。 |
您最近一年使用:0次
【推荐1】下列根据方程式得出的结论正确的是
| A.将Cu 置于双氧水和过量氨水中,其反应的离子方程式为:Cu+H2O2+4NH3·H2O=[Cu(NH3)]2++2OH-+4H2O |
B.已知S(s)+ O2(g)=SO3(g) ΔH=-395.7 kJ/mol,则硫磺的燃烧热为395.7 kJ/mol O2(g)=SO3(g) ΔH=-395.7 kJ/mol,则硫磺的燃烧热为395.7 kJ/mol |
| C.已知4P (红磷,s)=P4(白磷,s) ΔH=+29.2 kJ/mol,则白磷更稳定 |
| D.已知H+(aq)+OH-(aq)=HO(l) ΔH=-57.3 kJ/mol,则稀H2C2O4和稀NaOH反应生成2 molH2O的反应热ΔH<-2×57.3 kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列关于热化学反应的描述中正确 的是
| A.HCl与NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和氨水反应的中和热△H=2×(-57.3)kJ/mol |
| B.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g)的反应热△H=+566.0kJ/mol |
| C.需要加热才能发生的反应一定是吸热反应 |
| D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
您最近一年使用:0次
【推荐1】已知NaHCO3溶液与盐酸反应生成CO2吸热,Na2CO3溶液与盐酸反应生成CO2 放热。关于下列ΔH的判断正确的是
CO (aq)+H+(aq)
(aq)+H+(aq) HCO
HCO (aq) ΔH1
(aq) ΔH1
HCO (aq)+H+(aq)
(aq)+H+(aq)  H2CO3(aq) ΔH2
H2CO3(aq) ΔH2
H2CO3(aq) H2O(l)+CO2(g) ΔH3
H2O(l)+CO2(g) ΔH3
OH-(aq)+H+(aq) H2O(l) ΔH4
H2O(l) ΔH4
CO
 (aq)+H+(aq)
(aq)+H+(aq) HCO
HCO (aq) ΔH1
(aq) ΔH1HCO
 (aq)+H+(aq)
(aq)+H+(aq)  H2CO3(aq) ΔH2
H2CO3(aq) ΔH2H2CO3(aq)
 H2O(l)+CO2(g) ΔH3
H2O(l)+CO2(g) ΔH3OH-(aq)+H+(aq)
 H2O(l) ΔH4
H2O(l) ΔH4| A.ΔH1<0 ΔH2>0 | B.ΔH1+ΔH2>0 |
| C.ΔH1+ΔH2+ΔH3>0 | D.ΔH2<ΔH4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】工业生产甲醇的常用方法是:CO(g)+2H2(g)=CH3OH(g) △H1=-90.8 kJ/mol。
已知:2H2(g)+O2(g)=2H2O(1) △H2=-571.6 kJ/mol
H2(g)+ O2(g)=H2O(g) △H3=-241.8 kJ/mol
O2(g)=H2O(g) △H3=-241.8 kJ/mol
下列有关说法正确的是
已知:2H2(g)+O2(g)=2H2O(1) △H2=-571.6 kJ/mol
H2(g)+
 O2(g)=H2O(g) △H3=-241.8 kJ/mol
O2(g)=H2O(g) △H3=-241.8 kJ/mol下列有关说法正确的是
| A.H2的燃烧热为241. 8 kJ/mol |
| B.CH3OH(g)+O2(g)=CO(g)+2H2O(g) △H=-392. 8 kJ/mol |
C.“ ”既表示分子个数也能表示物质的量 ”既表示分子个数也能表示物质的量 |
| D.未注明温度和压强时,△H表示标准状况下的数据 |
您最近一年使用:0次

 的燃烧热是890.3kJ/mol,则表示
的燃烧热是890.3kJ/mol,则表示

 常温下不能自发进行,则该反应的
常温下不能自发进行,则该反应的 和1.5mol
和1.5mol  置于密闭容器中充分反应生成
置于密闭容器中充分反应生成 (g),放热19.3kJ,其热化学方程式为:
(g),放热19.3kJ,其热化学方程式为:
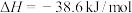
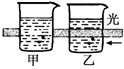
 的玻璃球浸到热水中,气体颜色加深:
的玻璃球浸到热水中,气体颜色加深:


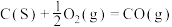
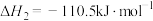
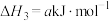
 和1mol
和1mol 的能量之和小于1mol
的能量之和小于1mol 的能量
的能量


