下列不能说明氯元素的非金属性比硫元素强的事实是( )
①HCl比H2S稳定②HClO氧化性比H2SO4强③HClO4酸性比H2SO4强④Cl2能与H2S反应生成S⑤Cl原子最外层有7个电子,S原子最外层有6个电子⑥Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS
①HCl比H2S稳定②HClO氧化性比H2SO4强③HClO4酸性比H2SO4强④Cl2能与H2S反应生成S⑤Cl原子最外层有7个电子,S原子最外层有6个电子⑥Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS
| A.②⑤ | B.①② | C.①②④ | D.①③⑤ |
更新时间:2020-09-02 16:51:25
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】短周期主族元素X、Y、Z、W的原子序数依次增大,最外层电子数之和为16。Y的原子半径在同周期元素中最大(除稀有气体外),Z所在周期与族序数相同,W与X属于同一主族。下列说法正确的是
A.原子半径: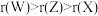 |
| B.由X、Y组成的化合物中均不含共价键 |
| C.Y的最高价氧化物的水化物的碱性比Z的弱 |
| D.X的简单气态氢化物的热稳定性比W的强 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】短周期主族元素X、Y、Z、W原子序数依次增大。W元素的气体单质呈黄绿色,此气体同冷烧碱溶液作用可得到化合物ZWX的溶液。下列说法正确的是
| A.W的氢化物稳定性强于Y的氢化物 |
| B.Z与Y形成的化合物为离子化合物 |
| C.Z与X形成的化合物中只含有离子键 |
| D.对应的简单离子半径大小为W>Z>X>Y |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】有 、
、 、
、 、
、 四种金属,最高价氧化物对应水化物的碱性:
四种金属,最高价氧化物对应水化物的碱性: 。将
。将 、
、 分别投入等浓度的盐酸中,
分别投入等浓度的盐酸中, 比
比 反应剧烈。将
反应剧烈。将 浸入
浸入 的盐溶液里,无明显变化。如果把
的盐溶液里,无明显变化。如果把 浸入
浸入 的盐溶液里,有
的盐溶液里,有 的单质析出。据此判断它们的金属活动性由强到弱的顺序是( )
的单质析出。据此判断它们的金属活动性由强到弱的顺序是( )
 、
、 、
、 、
、 四种金属,最高价氧化物对应水化物的碱性:
四种金属,最高价氧化物对应水化物的碱性: 。将
。将 、
、 分别投入等浓度的盐酸中,
分别投入等浓度的盐酸中, 比
比 反应剧烈。将
反应剧烈。将 浸入
浸入 的盐溶液里,无明显变化。如果把
的盐溶液里,无明显变化。如果把 浸入
浸入 的盐溶液里,有
的盐溶液里,有 的单质析出。据此判断它们的金属活动性由强到弱的顺序是( )
的单质析出。据此判断它们的金属活动性由强到弱的顺序是( )A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列正确的是( )。
| A.碱性:Al(OH)3>NaOH |
| B.原子半径:Cl>S |
| C.第一电离能:Mg>Al |
| D.沸点:H2S>H2O |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下面的排序不正确的是:
| A.晶体熔点:F2<Cl2 | B.稳定性:HF<HCl |
| C.硬度:金刚石>碳化硅>晶体硅 | D.熔点:H2O>HCl |
您最近一年使用:0次
【推荐2】下列比较不正确的是
| A.第一电离能:Be>B | B.热稳定性;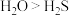 |
C.原子半径: | D.酸性: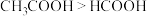 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐3】化合物M(结构式如图)是最常用的还原剂,由H·C·Brown和Schlesinger于1942年在芝加哥大学发现,其中X、Y、Z是原子序数依次减小的不同短周期主族元素,X与W、Z与W均能形成原子个数比为1:1和2:1的化合物,W原子的最外层电子数是电子层数的3倍,下列叙述正确的是


| A.Y的最高价氧化物对应的水化物是一种一元弱酸 |
| B.Z元素位于第3周期第ⅦA族 |
| C.X和Z形成的化合物的水溶液呈酸性 |
| D.化合物M不能与Z2W2反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列有关性质比较不能用元素周期律解释的是
A.向 溶液中加盐酸,有气泡产生 溶液中加盐酸,有气泡产生 |
B. 能溶于NaOH溶液, 能溶于NaOH溶液, 不能溶解于NaOH 不能溶解于NaOH |
C.酸性: |
| D.F2在暗处遇H2爆炸,I2在暗处遇H2几乎不反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】将一小块钠投入盛20 mL硫酸铜溶液的烧杯里,不可能观察到的现象是
| A.钠熔成小球、四处游动 | B.钠浮在液面上 |
| C.溶液底部有红色固体生成 | D.钠游过的下方有蓝色浑浊物质生成 |
您最近一年使用:0次

 沸点比
沸点比 低,所以O的非金属性比S强
低,所以O的非金属性比S强 的酸性比
的酸性比 的酸性强,所以S的非金属性比
的酸性强,所以S的非金属性比 强
强 三种元素对应离子半径的顺序为:
三种元素对应离子半径的顺序为:
 Si+2CO,该反应说明碳非金属性强于硅
Si+2CO,该反应说明碳非金属性强于硅

