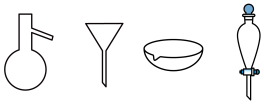
以电石渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的流程如图,氯化过程控制电石渣过量,在75℃左右进行。氯化时存在Cl2与Ca(OH)2作用生成Ca(ClO)2的反应,Ca(ClO)2进一步转化为Ca(ClO3)2,少量Ca(ClO)2分解为CaCl2和O2。生成Ca(ClO)2的化学方程式为___ 。



2020高三·全国·专题练习 查看更多[1]
(已下线)易错06 陌生化学方程式书写-备战2021年高考化学一轮复习易错题
更新时间:2020-09-03 11:10:35
|
相似题推荐
填空题
|
容易
(0.94)
【推荐1】根据信息书写指定反应的方程式。
(1)请从下列溶液中选择合适的溶液完成指定转化(试剂可以重复选择)。溶液:NH3·H2O、FeSO4、Fe2(SO4)3、HCl、NaCl
①写出SO2→H2SO4的化学方程式:____ ;
②写出SO2→SO32-的离子方程式:____ 。
(2)三聚磷酸铝(AlH2P3O10·2H2O)是新一代无公害白色防锈颜料,可由膨润土(主要成分:Al2O3·4SiO2·3H2O;含杂质:FeO、Fe2O3、Na2O等)为原料经过如下流程制备。

①“酸浸”时Al2O3·4SiO2·3H2O与硫酸反应的化学方程式为____ 。
②“净化”时发生反应的离子方程式为____ 。
③“沉铝”时发生反应的离子方程式为____ 。
(1)请从下列溶液中选择合适的溶液完成指定转化(试剂可以重复选择)。溶液:NH3·H2O、FeSO4、Fe2(SO4)3、HCl、NaCl
①写出SO2→H2SO4的化学方程式:
②写出SO2→SO32-的离子方程式:
(2)三聚磷酸铝(AlH2P3O10·2H2O)是新一代无公害白色防锈颜料,可由膨润土(主要成分:Al2O3·4SiO2·3H2O;含杂质:FeO、Fe2O3、Na2O等)为原料经过如下流程制备。

①“酸浸”时Al2O3·4SiO2·3H2O与硫酸反应的化学方程式为
②“净化”时发生反应的离子方程式为
③“沉铝”时发生反应的离子方程式为
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】目前从海水提溴(Br2)大致有以下步骤。
(1)向浓缩的海水中通入某种气体,将海水中的Br﹣氧化为Br2,该气体是___ 。
(2)用热空气将Br2从上述溶液中吹出,并由浓Na2CO3溶液吸收,转变为NaBr、NaBrO3、1molBr2需消耗Na2CO3___ mol。
(3)再将所得混合溶液用稀硫酸酸化,得到浓度较高的溴水,配平该反应的离子方程式。
__ Br﹣+__ BrO3﹣+__ H+→___ Br2+___ H2O。
(1)向浓缩的海水中通入某种气体,将海水中的Br﹣氧化为Br2,该气体是
(2)用热空气将Br2从上述溶液中吹出,并由浓Na2CO3溶液吸收,转变为NaBr、NaBrO3、1molBr2需消耗Na2CO3
(3)再将所得混合溶液用稀硫酸酸化,得到浓度较高的溴水,配平该反应的离子方程式。
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐3】(1)工业上利用 和
和 反应来制取单质
反应来制取单质 。
。
①配平化学方程式:________ 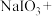
____________  =
=_______ 
________ 
________ 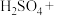
_______ 
②该反应中还原剂是________ (填化学式),_____ (填元素名称)元素被还原,生成1mol氧化产物转移的电子数目为________  (设
(设 为阿伏加 德罗常数的值)。
为阿伏加 德罗常数的值)。
(2)已知: 、
、 、
、 、
、 和一些未知物组成的氧化还原反应中
和一些未知物组成的氧化还原反应中 是氧化产物。该反应中还原性:
是氧化产物。该反应中还原性:
________ (填“>”或“<”) ,写出配平后的离子方程式:
,写出配平后的离子方程式:___________ 。
 和
和 反应来制取单质
反应来制取单质 。
。①配平化学方程式:
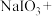
 =
=

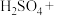

②该反应中还原剂是
 (设
(设 为阿伏加 德罗常数的值)。
为阿伏加 德罗常数的值)。(2)已知:
 、
、 、
、 、
、 和一些未知物组成的氧化还原反应中
和一些未知物组成的氧化还原反应中 是氧化产物。该反应中还原性:
是氧化产物。该反应中还原性:
 ,写出配平后的离子方程式:
,写出配平后的离子方程式:
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐1】物质的分离提纯。
(1)下列各组混合物的分离提纯或是检验应采用什么方法?
①实验室中的石灰水久置,液面上常悬浮有CaCO3微粒.可用________ 的方法除去Ca(OH)2溶液中悬浮的CaCO3微粒。
②鉴别胶体和溶液的一般方法是________ 。
③除去乙醇中溶解的微量食盐可采用________ 的方法。
④从碘水中提取碘可采用________ 的方法。
⑤除去氧化钙中的碳酸钙可用________ 的方法。
(2)填表:
(1)下列各组混合物的分离提纯或是检验应采用什么方法?
①实验室中的石灰水久置,液面上常悬浮有CaCO3微粒.可用
②鉴别胶体和溶液的一般方法是
③除去乙醇中溶解的微量食盐可采用
④从碘水中提取碘可采用
⑤除去氧化钙中的碳酸钙可用
(2)填表:
| 混合物(括号内为杂质) | 提纯用试剂 | 发生反应的离子方程式 |
| Na2SO4(MgSO4) | ||
| KOH(Ba(OH)2) | ||
| NaCl(NaOH和Na2CO3) |
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
【推荐2】写出除杂试剂和提纯方法。
| 需提纯物 | 杂质 | 所需试剂 | 提纯方法 | |
| (1) | 乙醇 | 水 | ||
| (2) | 溴乙烷 | 液溴 |
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐1】(15分)重铬酸钠(Na2Cr2O7)主要用于印染、制革、医药、电镀等。工业上以铬铁矿(主要成分FeO·Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠(Na2Cr2O7·2H2O)的主要反应如下:
①4FeO·Cr2O3+8Na2CO3+7O2 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2
②2Na2CrO4+H2SO4=Na2SO4+Na2Cr2O7+H2O
(1)反应①是在回转窑中进行,反应时需不断搅拌,其目的是___________ 。
(2)右图是红矾钠(Na2Cr2O7·2H2O)和Na2SO4的溶

解度曲线。从Na2Cr2O7和Na2SO4的混合溶液中提取Na2Cr2O7,晶体的操作:先将混合溶液蒸发浓缩,趁热过滤。趁热过滤的目的是__________ ;然后将滤液_______ ,从而析出红矾钠。
(3)Na2Cr2O7与KCl或K2SO4进行复分解反应可制取K2Cr2O7,现用Na2Cr2O7与KCl来制备K2Cr2O7,简述操作步骤(有关物质的溶解度见右表):__________ 。

(4)重铬酸钾可用于铁矿石中铁的含量测定,实验步骤如下:
步骤1:将mg铁矿石加浓盐酸加热溶解
步骤2:加入SnCl2溶液将Fe3+还原至黄色消失
步骤3:将所得溶液冷却,加入HgC2溶液,将过量的Sn2+氧化为Sn4+
步骤4:加入15mL硫酸和磷酸的混合酸及5滴O.2%二苯胺磺酸钠指示剂
步骤5:立即用cmol·L。重铬酸钾溶液滴定至溶液呈稳定紫色,即为终点,消耗重铬酸钾溶液VmL
①写出SnCl2还原Fe3+的离子方程式___________ 。
②如省去步骤③,则所测定的铁的含量_________ (填“偏高”、“偏低”或“无影响”)。
③步骤5使用的玻璃仪器有________ 。
①4FeO·Cr2O3+8Na2CO3+7O2
 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2②2Na2CrO4+H2SO4=Na2SO4+Na2Cr2O7+H2O
(1)反应①是在回转窑中进行,反应时需不断搅拌,其目的是
(2)右图是红矾钠(Na2Cr2O7·2H2O)和Na2SO4的溶

解度曲线。从Na2Cr2O7和Na2SO4的混合溶液中提取Na2Cr2O7,晶体的操作:先将混合溶液蒸发浓缩,趁热过滤。趁热过滤的目的是
(3)Na2Cr2O7与KCl或K2SO4进行复分解反应可制取K2Cr2O7,现用Na2Cr2O7与KCl来制备K2Cr2O7,简述操作步骤(有关物质的溶解度见右表):

(4)重铬酸钾可用于铁矿石中铁的含量测定,实验步骤如下:
步骤1:将mg铁矿石加浓盐酸加热溶解
步骤2:加入SnCl2溶液将Fe3+还原至黄色消失
步骤3:将所得溶液冷却,加入HgC2溶液,将过量的Sn2+氧化为Sn4+
步骤4:加入15mL硫酸和磷酸的混合酸及5滴O.2%二苯胺磺酸钠指示剂
步骤5:立即用cmol·L。重铬酸钾溶液滴定至溶液呈稳定紫色,即为终点,消耗重铬酸钾溶液VmL
①写出SnCl2还原Fe3+的离子方程式
②如省去步骤③,则所测定的铁的含量
③步骤5使用的玻璃仪器有
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
【推荐2】《宋史·食货志》中有这样一段话:“浸铜之法,以生铁煅成薄铁片,排置胆水槽中,浸渍数日,铁片为胆水所薄,上生赤煤。去刮赤煤,入炉三炼成铜。大率用铁二斤四两得铜一斤。”
(1)文中胆水可能是__________________________ 赤煤又可能是_________________
(2)上文中炼铜,假如生铁中含铁95%,那么铁的利用率是__________________________
(1斤以16两计算)
(1)文中胆水可能是
(2)上文中炼铜,假如生铁中含铁95%,那么铁的利用率是
(1斤以16两计算)
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐3】氯化钙(CaCl2)的用途十分广泛。在工业生产中,氯化钙常被用作干燥剂,因其溶解放热可用于制作自加热罐头,它还是制作豆腐等美食的食品添加剂。请你设计尽可能多的方案制得氯化钙。并写出化学方程式_____________ 。
您最近一年使用:0次

 及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如图(用于沉淀的试剂稍过量):
及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如图(用于沉淀的试剂稍过量):