氯化亚铜(CuCl)常用作催化剂、杀菌剂等。
(1)将Na2SO3溶液逐滴加入到CuCl2溶液中,再加入少量浓盐酸混匀,得到CuCl沉淀。写出该反应的离子方程式____________________________ 。
(2)为测定制得CuCl样品的纯度,进行下列实验:
a.称取0.5000 g样品,放入盛有20 mL过量FeCl3 溶液和玻璃珠的锥形瓶中,不断摇动;
b.待样品溶解后,加水50 mL;
c.立即用0.2000 mol/LCe(SO4)2标准溶液滴至反应完全,记录消耗标准溶液的体积;
d.重复步骤a至c操作2次,记录消耗标准溶液的平均体积为25.00 mL。已知:CuC1+Fe3+=Cu2++Fe2++Cl-、 Fe2++Ce4+=Fe3++Ce3+
①配制100 mL 0.2000 mol/L的Ce(SO4)2标准溶液时,需要的玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管,还需要______________ 。
②进行步骤c时若操作缓慢,则测得CuCl的纯度________ (填“偏大”、“偏小”或“无影响”)。
③通过计算确定该样品中CuCl的纯度_____________ (写出计算过程)。
(1)将Na2SO3溶液逐滴加入到CuCl2溶液中,再加入少量浓盐酸混匀,得到CuCl沉淀。写出该反应的离子方程式
(2)为测定制得CuCl样品的纯度,进行下列实验:
a.称取0.5000 g样品,放入盛有20 mL过量FeCl3 溶液和玻璃珠的锥形瓶中,不断摇动;
b.待样品溶解后,加水50 mL;
c.立即用0.2000 mol/LCe(SO4)2标准溶液滴至反应完全,记录消耗标准溶液的体积;
d.重复步骤a至c操作2次,记录消耗标准溶液的平均体积为25.00 mL。已知:CuC1+Fe3+=Cu2++Fe2++Cl-、 Fe2++Ce4+=Fe3++Ce3+
①配制100 mL 0.2000 mol/L的Ce(SO4)2标准溶液时,需要的玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管,还需要
②进行步骤c时若操作缓慢,则测得CuCl的纯度
③通过计算确定该样品中CuCl的纯度
更新时间:2020-09-16 18:11:35
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】为研究甲的组成,某研究小组设计了方案,其流程如下:

(1)为研究氧化物A的组成,进行如下实验:
Ⅰ.①取少许氧化物A于试管中,加入稀 反应,得到蓝色溶液同时有不溶性的红色物质生成,则为了除去其中的红色物质,最好加入
反应,得到蓝色溶液同时有不溶性的红色物质生成,则为了除去其中的红色物质,最好加入___________ (填字母),其反应的离子方程式为___________ 。
A.适量的 溶液 B.适量的硝酸 C.适量的
溶液 B.适量的硝酸 C.适量的 溶液
溶液
Ⅱ.取上述蓝色溶液于试管中,进行下列实验

资料:
i. 可与
可与 反应生成CuSCN白色溶液和
反应生成CuSCN白色溶液和 。
。
ii. 称为“拟卤素”,在水溶液中呈黄色;
称为“拟卤素”,在水溶液中呈黄色; 的化学性质与
的化学性质与 相似,可与水、碱等发生反应。
相似,可与水、碱等发生反应。
②a中 溶液显酸性的原因是
溶液显酸性的原因是___________ (用离子方程式表示)。
③a→b中试管内溶液pH减小,可能的原因是___________ 。
④b→c产生沉淀的原因是___________ 。
(2)为研究气体B的成分,研究小组设计的实验方案是:
①将气体B通入水中,向其中滴加品红溶液,充分振荡后红色褪去,加热后颜色恢复。因此气体B中含有___________
②将气体B通入盐酸酸化 溶液中,一段时间生成了少量白色沉淀,发生的反应的离子方程式为
溶液中,一段时间生成了少量白色沉淀,发生的反应的离子方程式为___________ 。
(3)通过上述实验,可知甲中所含元素为___________ (填元素符号),为确定甲的化学式,需要收集的数据是甲的质量和___________ 。

(1)为研究氧化物A的组成,进行如下实验:
Ⅰ.①取少许氧化物A于试管中,加入稀
 反应,得到蓝色溶液同时有不溶性的红色物质生成,则为了除去其中的红色物质,最好加入
反应,得到蓝色溶液同时有不溶性的红色物质生成,则为了除去其中的红色物质,最好加入A.适量的
 溶液 B.适量的硝酸 C.适量的
溶液 B.适量的硝酸 C.适量的 溶液
溶液Ⅱ.取上述蓝色溶液于试管中,进行下列实验

资料:
i.
 可与
可与 反应生成CuSCN白色溶液和
反应生成CuSCN白色溶液和 。
。ii.
 称为“拟卤素”,在水溶液中呈黄色;
称为“拟卤素”,在水溶液中呈黄色; 的化学性质与
的化学性质与 相似,可与水、碱等发生反应。
相似,可与水、碱等发生反应。②a中
 溶液显酸性的原因是
溶液显酸性的原因是③a→b中试管内溶液pH减小,可能的原因是
④b→c产生沉淀的原因是
(2)为研究气体B的成分,研究小组设计的实验方案是:
①将气体B通入水中,向其中滴加品红溶液,充分振荡后红色褪去,加热后颜色恢复。因此气体B中含有
②将气体B通入盐酸酸化
 溶液中,一段时间生成了少量白色沉淀,发生的反应的离子方程式为
溶液中,一段时间生成了少量白色沉淀,发生的反应的离子方程式为(3)通过上述实验,可知甲中所含元素为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】三氧化二铁和氧化亚铜( )都是红色粉末,常用作颜料。某校一化学实验小组通过实验探究一红色粉末的成分。探究过程如下:
)都是红色粉末,常用作颜料。某校一化学实验小组通过实验探究一红色粉末的成分。探究过程如下:
【查阅资料】 溶于稀硫酸生成Cu、
溶于稀硫酸生成Cu、 和
和 ,在空气中加热生成
,在空气中加热生成 。
。
【提出假设】假设1:红色粉末是 ;
;
假设2:红色粉末是 ;
;
假设3:红色粉末是 和
和 的混合物。
的混合物。
【设计实验】取少量该红色粉末加入足量稀硫酸中,再向所得溶液中滴加KSCN溶液。
(1)若假设1成立,则实验现象是____________________________________________________________ 。
(2)若滴加KSCN溶液,溶液不变红,则证明原红色粉末中一定不含 。你认为这种说法
。你认为这种说法_________ (填“合理”或“不合理”),理由是______________________________________________________ 。
(3)若红色粉末完全溶解,滴加KSCN溶液,溶液不变红,则证明原红色粉末是_____________________ ,写出发生反应的离子方程式:_________________________________________________________ 。
【探究延伸】
(4)经实验分析,确定该红色粉末为 和
和 的混合物。某实验小组欲用加热法测定该红色粉末中
的混合物。某实验小组欲用加热法测定该红色粉末中 的质量分数。取
的质量分数。取 红色粉末在空气中充分加热,待质量不再变化时,称其质量为
红色粉末在空气中充分加热,待质量不再变化时,称其质量为 ,则该红色粉末中
,则该红色粉末中 的质量分数为
的质量分数为_____________________ 。
 )都是红色粉末,常用作颜料。某校一化学实验小组通过实验探究一红色粉末的成分。探究过程如下:
)都是红色粉末,常用作颜料。某校一化学实验小组通过实验探究一红色粉末的成分。探究过程如下:【查阅资料】
 溶于稀硫酸生成Cu、
溶于稀硫酸生成Cu、 和
和 ,在空气中加热生成
,在空气中加热生成 。
。【提出假设】假设1:红色粉末是
 ;
;假设2:红色粉末是
 ;
;假设3:红色粉末是
 和
和 的混合物。
的混合物。【设计实验】取少量该红色粉末加入足量稀硫酸中,再向所得溶液中滴加KSCN溶液。
(1)若假设1成立,则实验现象是
(2)若滴加KSCN溶液,溶液不变红,则证明原红色粉末中一定不含
 。你认为这种说法
。你认为这种说法(3)若红色粉末完全溶解,滴加KSCN溶液,溶液不变红,则证明原红色粉末是
【探究延伸】
(4)经实验分析,确定该红色粉末为
 和
和 的混合物。某实验小组欲用加热法测定该红色粉末中
的混合物。某实验小组欲用加热法测定该红色粉末中 的质量分数。取
的质量分数。取 红色粉末在空气中充分加热,待质量不再变化时,称其质量为
红色粉末在空气中充分加热,待质量不再变化时,称其质量为 ,则该红色粉末中
,则该红色粉末中 的质量分数为
的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某校化学研究性学习小组的同学在学习了金属的知识后,为了解Cu的常见化合物性质,运用类比学习的思想提出如下的问题,探究。请你协助该小组的同学完成下列研究。
【提出问题】
①Cu的金属活泼性小于Al,Al(OH)3具有两性,Cu(OH)2也具有两性吗?
②通常情况下,+2价Fe的稳定性小于+3价Fe,+1价Cu的稳定性也小于+2价Cu吗?③CuO能被H2、CO等还原,也能被NH3还原吗?
【实验方案】
(1)解决问题①需用到的药品有:CuSO4溶液、____ (填试剂),同时进行相关实验。
(2)解决问题②的实验步骤和现象如下:取98g Cu(OH)2固体,加热至80℃~100℃时,得到黑色固体粉末,继续加热到1000℃以上,黑色粉末全部变成红色粉末A.冷却后称量A的质量为72g。向A中加入适量的稀硫酸,得到蓝色溶液,同时观察到容器还有红色固体存在。据些可推得,A的化学式为___ 。
(3)为解决问题③,设计的实验装置为(夹持及尾气处理装置未画出):
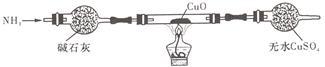
实验中观察到CuO变为红色物质,无水CuSO4变___ 色。同时生成一种对大气无污染的气体。
【实验结论】
(1)Cu(OH)2具有两性,证明Cu(OH)2具有两性的实验现象应是_____ 。
(2)根据“实验方案(2)”,得出的+1价Cu和+2价Cu稳定性大小的结论是____ 。
【问题讨论】
有同学认为NH3与CuO反应生成的红色物质是Cu,也有同学认为NH3与CuO反应生成的红色物质是Cu和A的混合物。
请你设计一个简单的实验检验NH3与CuO反应中生成的红色物质中是否含有A___ 。
【提出问题】
①Cu的金属活泼性小于Al,Al(OH)3具有两性,Cu(OH)2也具有两性吗?
②通常情况下,+2价Fe的稳定性小于+3价Fe,+1价Cu的稳定性也小于+2价Cu吗?③CuO能被H2、CO等还原,也能被NH3还原吗?
【实验方案】
(1)解决问题①需用到的药品有:CuSO4溶液、
(2)解决问题②的实验步骤和现象如下:取98g Cu(OH)2固体,加热至80℃~100℃时,得到黑色固体粉末,继续加热到1000℃以上,黑色粉末全部变成红色粉末A.冷却后称量A的质量为72g。向A中加入适量的稀硫酸,得到蓝色溶液,同时观察到容器还有红色固体存在。据些可推得,A的化学式为
(3)为解决问题③,设计的实验装置为(夹持及尾气处理装置未画出):

实验中观察到CuO变为红色物质,无水CuSO4变
【实验结论】
(1)Cu(OH)2具有两性,证明Cu(OH)2具有两性的实验现象应是
(2)根据“实验方案(2)”,得出的+1价Cu和+2价Cu稳定性大小的结论是
【问题讨论】
有同学认为NH3与CuO反应生成的红色物质是Cu,也有同学认为NH3与CuO反应生成的红色物质是Cu和A的混合物。
请你设计一个简单的实验检验NH3与CuO反应中生成的红色物质中是否含有A
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】氧化亚铜是大型水面舰艇防护涂层的重要原料.某小组通过查阅资料,进行如图研究.

I.Cu2O的制取
(1)葡萄糖还原法制Cu2O的化学方程式为____________
(2)实验室用此方法制取并获得少量Cu2O固体,需要的玻璃仪器除试管、酒精灯、烧杯外,还需要____________
Ⅱ.检验样品中是否含有CuO
方案1:将制得的Cu2O样品溶于足量稀硫酸.
(3)甲同学认为若溶液变为蓝色,则说明样品中含有CuO杂质.乙同学认为此推论不合理,用化学用语解释原因_____________
(4)甲同学通过反思,认为将定性检验改为定量测定便能确定样品中是否含有CuO杂质,应测量的数据是________________
方案2:丙同学认为采用如下装置(所加药品均足量)进行实验,通过测定c装置反应后固体的质量以及d装置反应前后增重的质量,可计算,从而确定样品中是否含有氧化铜.
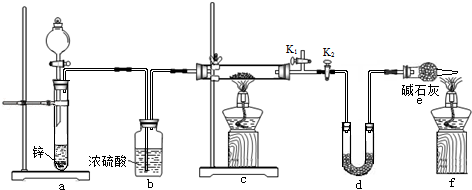
(5)装置a中所加的酸是__________
(填化学式),装置e中碱石灰的作用是_______________
(6)点燃装置c中酒精灯之前需进行的操作是_________________
(7)熄灭酒精灯之后,仍需通一段时间H2至试管冷却,原因是_______________ .

I.Cu2O的制取
(1)葡萄糖还原法制Cu2O的化学方程式为
(2)实验室用此方法制取并获得少量Cu2O固体,需要的玻璃仪器除试管、酒精灯、烧杯外,还需要
Ⅱ.检验样品中是否含有CuO
方案1:将制得的Cu2O样品溶于足量稀硫酸.
(3)甲同学认为若溶液变为蓝色,则说明样品中含有CuO杂质.乙同学认为此推论不合理,用化学用语解释原因
(4)甲同学通过反思,认为将定性检验改为定量测定便能确定样品中是否含有CuO杂质,应测量的数据是
方案2:丙同学认为采用如下装置(所加药品均足量)进行实验,通过测定c装置反应后固体的质量以及d装置反应前后增重的质量,可计算,从而确定样品中是否含有氧化铜.

(5)装置a中所加的酸是
(填化学式),装置e中碱石灰的作用是
(6)点燃装置c中酒精灯之前需进行的操作是
(7)熄灭酒精灯之后,仍需通一段时间H2至试管冷却,原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】一氯甲烷是-种重要的化工原料,常温下它是无色有毒气体,微溶于水,易溶于乙醇、CCl4等。
(1)甲组同学在实验室用如图所示装置模拟催化法制备和收集一氯甲烷。①无水ZnCl2为催化剂,a瓶中发生反应的化学方程式为_______ ,如果实验时a瓶加热时间过长,最终在瓶底得到一种白色物质,该物质的化学式是__________ 。②装置B的主要作用是___________ 。
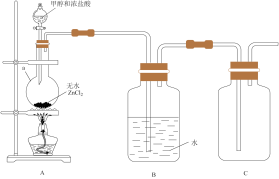
(2)收集到的CH3Cl气体在氧气中充分燃烧,产物用过量的 溶液充分吸收,以甲基橙作指示剂,用
溶液充分吸收,以甲基橙作指示剂,用 盐酸标准液对吸收液进行滴定(发生的反应为:NaOH+HCl=NaCl+H2O,Na2CO3+2HCl=2NaCl+CO2↑+H2O),当观察到
盐酸标准液对吸收液进行滴定(发生的反应为:NaOH+HCl=NaCl+H2O,Na2CO3+2HCl=2NaCl+CO2↑+H2O),当观察到___________ 时即达到滴定终点,消耗V2mL盐酸。则所收集CH3Cl的物质的量为____________ mol。(已知:2CH3Cl+3O2 2CO2+2H2O+2HCl)
2CO2+2H2O+2HCl)
(3)乙组同学选用甲组装置A、B和如图所示的部分装置检验CH3Cl中的氯元素。(已知:CH3Cl+NaOH CH3OH+NaCl)
CH3OH+NaCl)
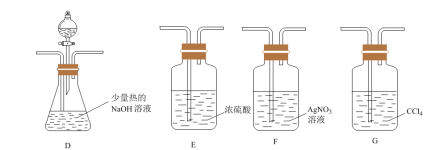
①乙组同学的实验装置中,依次连接的合理顺序为A、B、__ 。
②通入一段时间的CH3Cl气体,打开装置D中分液漏斗的活塞观察实验现象。分液漏斗中盛放的试剂是________________ 。
③能证明CH3Cl中含有氯元素的实验现象是______________ 。
(1)甲组同学在实验室用如图所示装置模拟催化法制备和收集一氯甲烷。①无水ZnCl2为催化剂,a瓶中发生反应的化学方程式为

(2)收集到的CH3Cl气体在氧气中充分燃烧,产物用过量的
 溶液充分吸收,以甲基橙作指示剂,用
溶液充分吸收,以甲基橙作指示剂,用 盐酸标准液对吸收液进行滴定(发生的反应为:NaOH+HCl=NaCl+H2O,Na2CO3+2HCl=2NaCl+CO2↑+H2O),当观察到
盐酸标准液对吸收液进行滴定(发生的反应为:NaOH+HCl=NaCl+H2O,Na2CO3+2HCl=2NaCl+CO2↑+H2O),当观察到 2CO2+2H2O+2HCl)
2CO2+2H2O+2HCl)(3)乙组同学选用甲组装置A、B和如图所示的部分装置检验CH3Cl中的氯元素。(已知:CH3Cl+NaOH
 CH3OH+NaCl)
CH3OH+NaCl)
①乙组同学的实验装置中,依次连接的合理顺序为A、B、
②通入一段时间的CH3Cl气体,打开装置D中分液漏斗的活塞观察实验现象。分液漏斗中盛放的试剂是
③能证明CH3Cl中含有氯元素的实验现象是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】孔雀石主要成分是Cu2(OH)2CO3,还含少量FeCO3及Si的化合物,实验室以孔雀石为原料制备硫酸铜晶体的步骤如下:
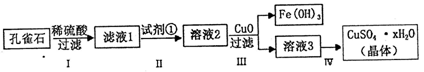
(1)步骤I中涉及的主要反应用离子方程式表示为___________ .
(2)步骤Ⅱ中试剂①是_______ (填代号).
a.KMnO4 b.H2O2 c.Fe粉 d.KSCN
(3)步骤Ⅲ加入CuO 的目的是_________
(4)步骤Ⅳ获得硫酸铜晶体,需要经过_____________ 冷却结晶、过滤等操作.
(5)测定硫酸铜晶体(CuSO4·xH2O)中结晶水的x值:称取2.41g硫酸铜晶体,在____ (填实验仪器名称)中加热至质量不再改变时,称量粉末的质量为1.6g.则计算得x=______ (计算结果精确到0.1)

(1)步骤I中涉及的主要反应用离子方程式表示为
(2)步骤Ⅱ中试剂①是
a.KMnO4 b.H2O2 c.Fe粉 d.KSCN
(3)步骤Ⅲ加入CuO 的目的是
(4)步骤Ⅳ获得硫酸铜晶体,需要经过
(5)测定硫酸铜晶体(CuSO4·xH2O)中结晶水的x值:称取2.41g硫酸铜晶体,在
您最近一年使用:0次



