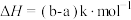下列说法正确的有( )
①活化分子间的碰撞不一定能发生化学反应
②普通分子间的碰撞有时也能发生化学反应
③增大反应物的浓度,可增大单位体积内活化分子数,从而使有效碰撞次数增多
④有气体参加的化学反应,若增大压强(即缩小反应容器的容积),可增大活化分子百分数,从而使反应速率增大
⑤化学反应的实质是旧化学键断裂和新化学键形成的过程
①活化分子间的碰撞不一定能发生化学反应
②普通分子间的碰撞有时也能发生化学反应
③增大反应物的浓度,可增大单位体积内活化分子数,从而使有效碰撞次数增多
④有气体参加的化学反应,若增大压强(即缩小反应容器的容积),可增大活化分子百分数,从而使反应速率增大
⑤化学反应的实质是旧化学键断裂和新化学键形成的过程
| A.1个 | B.2个 | C.3个 | D.4个 |
更新时间:2020-09-17 10:19:11
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列实验设计能达到实验目的的是
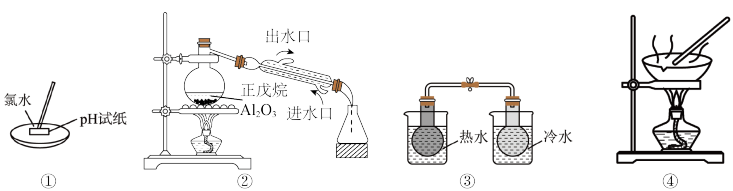

| A.①用于测量氯水的pH |
| B.②可以探究正戊烷(C5H12)催化裂化 |
| C.③可用于探究温度对2NO2(g)⇌N2O4(g)平衡移动的影响 |
| D.④用AlCl3溶液制备AlCl3晶体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】研究表明N2O与CO在Fe+作用下发生反应的能量变化及反应过程如图所示。下列说法错误的是
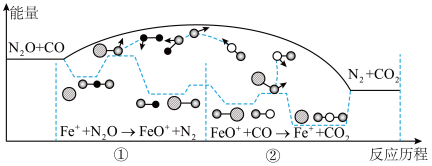

| A.反应总过程∆H<0 |
| B.反应速率大小:①<② |
| C.FeO+是该反应的催化剂 |
| D.①、②两步反应均为放热反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列有关图象的叙述正确的是
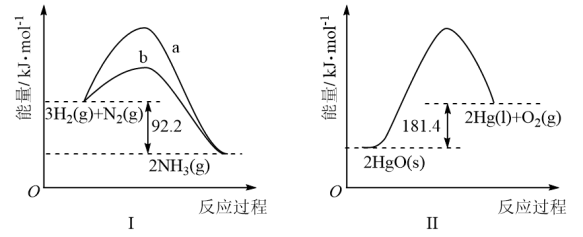

| A.图 I:向容器中充入 1 mol N2、3 mol H2,充分反应后放出热量92.2 kJ |
| B.图 I:b 可能为使用催化剂的曲线,降低了反应的活化能 |
| C.图 II:HgO(s) = Hg(l) + 1/2O2(g) △H = - 90.7 kJ/mol |
| D.图 II:Hg(l) 的能量一定比HgO(s)高 |
您最近一年使用:0次
【推荐2】Burns和Dainton研究发现Cl2与CO合成 的反应机理如下:①
的反应机理如下:① 快;②
快;② 快;③
快;③ 慢。其中反应②存在
慢。其中反应②存在 、
、 。下列说法正确的是
。下列说法正确的是
 的反应机理如下:①
的反应机理如下:① 快;②
快;② 快;③
快;③ 慢。其中反应②存在
慢。其中反应②存在 、
、 。下列说法正确的是
。下列说法正确的是| A.反应①的活化能大于反应③的活化能 |
B.反应②的平衡常数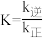 |
C.要提高合成 的速率,关键是提高反应③的速率 的速率,关键是提高反应③的速率 |
D.选择合适的催化剂能加快该反应的速率,并提高 的平衡产率 的平衡产率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列关于可逆反应:A(g)+3B(g) 2C(g) △H<0,下列叙述正确的( )
2C(g) △H<0,下列叙述正确的( )
 2C(g) △H<0,下列叙述正确的( )
2C(g) △H<0,下列叙述正确的( )| A.增大反应物的浓度,可以提高活化分子百分数,所以v(正)会增大,v(逆)会减小 |
| B.升高温度可以提高物质的能量,提高活化分子百分数,所以v(正)、v(逆)都增大 |
| C.采用催化剂,可以提高活化分子百分数,所以会引起v(正)、v(逆)同时增大,并改变反应的热效应 |
| D.减小压强可以降低单位体积内活化分子的数目,所以v(正)减小、v(逆)增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】甲酸常被用于橡胶、医药等工业。在一定条件下可分解生成 和
和 。在有、无催化剂条件下的能量与反应历程的关系如图所示。下列说法错误的是
。在有、无催化剂条件下的能量与反应历程的关系如图所示。下列说法错误的是

 和
和 。在有、无催化剂条件下的能量与反应历程的关系如图所示。下列说法错误的是
。在有、无催化剂条件下的能量与反应历程的关系如图所示。下列说法错误的是
| A.途径一与途径二甲酸平衡转化率相同 |
B.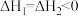 |
C.途径二 参与反应,通过改变反应途径,降低反应的活化能,加快反应速率 参与反应,通过改变反应途径,降低反应的活化能,加快反应速率 |
D.途径二反应的快慢由生成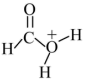 的速率决定 的速率决定 |
您最近一年使用:0次

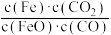
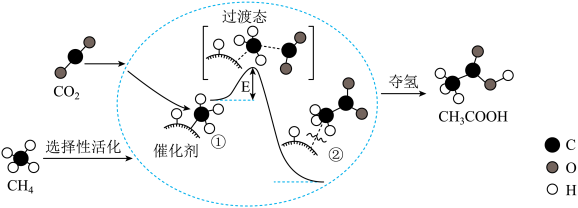
 ②吸收能量并形成了C-C键
②吸收能量并形成了C-C键 稳定的高分散Pt用于高效催化丙烷脱氢。反应原理如图1所示,丙烷脱氢的能量变化如图2所示。下列叙述正确的是
稳定的高分散Pt用于高效催化丙烷脱氢。反应原理如图1所示,丙烷脱氢的能量变化如图2所示。下列叙述正确的是