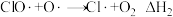钛被称为“第三金属”,其制取原料为金红石( ),制取步骤如下:
),制取步骤如下:
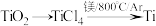
已知:①

②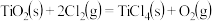

则反应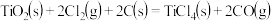 的ΔH为
的ΔH为
 ),制取步骤如下:
),制取步骤如下: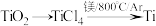
已知:①


②
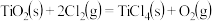

则反应
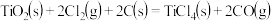 的ΔH为
的ΔH为| A.2ΔH1+2ΔH2 | B.2ΔH1+ΔH2 |
| C.2ΔH1-ΔH2 | D.2ΔH1-2ΔH2 |
更新时间:2020-09-21 16:05:08
|
相似题推荐
单选题
|
容易
(0.94)
名校
解题方法
【推荐1】已知:弱碱MOH(aq)与H2SO4(aq)反应生成1mol正盐的△H=-24.2kJ/mol,强酸与强碱的稀溶液的中和热为△H=-57.3kJ/mol。则MOH在水溶液中电离的△H为
| A.+45.2kJ/mol | B.+69.4kJ/mol | C.-69.4kJ/mol | D.-45.2kJ/mol |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐2】煤炭燃烧过程中会释放出大量的SO2,严重破坏生态环境。采用一定的脱硫技术可以把硫元素以CaSO4的形式固定,从而降低SO2的排放。但是煤炭燃烧过程中产生的CO又会与CaSO4发生化学反应,降低脱硫效率。相关反应的热化学方程式如下:
CaSO4(s)+CO(g) CaO(s)+SO2(g)+CO2(g) △H1=+218.4 kJ/mol(反应I)
CaO(s)+SO2(g)+CO2(g) △H1=+218.4 kJ/mol(反应I)
CaSO4(s)+4CO(g) CaS(s)+4CO2(g) △H2=-175.6 kJ/mol (反应II)
CaS(s)+4CO2(g) △H2=-175.6 kJ/mol (反应II)
下列有关说法正确的是
CaSO4(s)+CO(g)
 CaO(s)+SO2(g)+CO2(g) △H1=+218.4 kJ/mol(反应I)
CaO(s)+SO2(g)+CO2(g) △H1=+218.4 kJ/mol(反应I)CaSO4(s)+4CO(g)
 CaS(s)+4CO2(g) △H2=-175.6 kJ/mol (反应II)
CaS(s)+4CO2(g) △H2=-175.6 kJ/mol (反应II)下列有关说法正确的是
| A.反应I在较低的温度下可自发进行 |
| B.反应II在较低的温度下可自发进行 |
C.用生石灰固硫的反应为:4CaO(s)+4SO2(g)  3CaSO4(s)+CaS(s) △H3,则△H3>△H2 3CaSO4(s)+CaS(s) △H3,则△H3>△H2 |
D.由反应I和反应II可计算出反应CaSO4(s)  CaO(s)+SO3(g)的焓变 CaO(s)+SO3(g)的焓变 |
您最近一年使用:0次

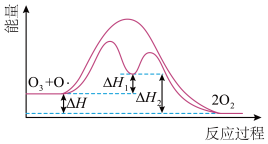
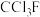 可在强烈紫外光作用下分解
可在强烈紫外光作用下分解 ,自由基
,自由基 会对臭氧层产生长久的破坏作用,反应历程可表示为
会对臭氧层产生长久的破坏作用,反应历程可表示为