化学反应可视为旧键断裂和新键形成的过程。已知白磷和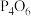 的分子结构如图所示,现提供以下化学键的键能(
的分子结构如图所示,现提供以下化学键的键能( ):P-P键:198,P-O键:360,
):P-P键:198,P-O键:360, 键:498,则依据反应
键:498,则依据反应 (白磷)
(白磷)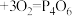 ,生成1mol
,生成1mol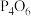 时的能量变化为( )
时的能量变化为( )

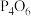 的分子结构如图所示,现提供以下化学键的键能(
的分子结构如图所示,现提供以下化学键的键能( ):P-P键:198,P-O键:360,
):P-P键:198,P-O键:360, 键:498,则依据反应
键:498,则依据反应 (白磷)
(白磷)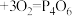 ,生成1mol
,生成1mol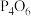 时的能量变化为( )
时的能量变化为( )
| A.吸收1638kJ的能量 | B.放出1638kJ的能量 |
| C.吸收126kJ的能量 | D.放出126kJ的能量 |
更新时间:2020-09-24 18:11:59
|
相似题推荐
单选题
|
较易
(0.85)
解题方法
【推荐1】火箭常使用肼( )作燃料,有关化学反应的能量变化如图所示。已知
)作燃料,有关化学反应的能量变化如图所示。已知 键的键能为
键的键能为 ,
, 键的键能为
键的键能为 ,
, 键的键能为
键的键能为 ,则
,则 键的键能为
键的键能为

 )作燃料,有关化学反应的能量变化如图所示。已知
)作燃料,有关化学反应的能量变化如图所示。已知 键的键能为
键的键能为 ,
, 键的键能为
键的键能为 ,
, 键的键能为
键的键能为 ,则
,则 键的键能为
键的键能为
A. | B. |
C. | D. |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】化学家们对化学学科的发展做出巨大的贡献。下列有关说法错误的是
| A.俄国化学家盖斯提出盖斯定律,为化学动力学发展奠定了基础 |
| B.德国化学家维勒合成了尿素,开创了人工合成有机化合物的新时代 |
| C.中国化学家侯德榜发明了联合制碱法,打破外国对我国的技术封锁 |
| D.法国化学家拉瓦锡提出燃烧的氧化学说,使近代化学取得革命性的进展 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列过程释放能量的是
A. | B. | C. | D. |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】根据下图所示的N2(g)和O2(g)反应生成NO(g)过程中的能量变化情况,判断下列说法正确的是


| A.N2(g)+O2(g)=2NO(g)的反应,反应物的总能量小于生成物的总能量 |
| B.2molO原子结合生成O2(g)时需要吸收498kJ能量 |
| C.1molNO(g)分子中的化学键断裂时需要放出632kJ能量 |
| D.NO(g)分解为N2(g)和O2(g)反应为吸热反应 |
您最近一年使用:0次
【推荐1】下列关于反应热的说法正确的是
A. 时,表示该反应为吸热反应 时,表示该反应为吸热反应 |
| B.反应热的大小与反应物所具有的能量和生成物所具有的能量无关 |
| C.化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关 |
| D.所有化学反应都伴随着能量的变化,伴有能量的变化一定是化学反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】已知: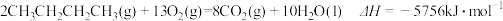

下列说法正确的是
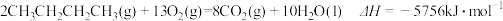

下列说法正确的是
A.异丁烷的燃烧热为 |
| B.正丁烷所具有的能量低于异丁烷,更稳定 |
C.正丁烷和异丁烷分子中 键的键能完全相同 键的键能完全相同 |
D. 异丁烷转化为 异丁烷转化为 正丁烷的过程,需要吸收 正丁烷的过程,需要吸收 的热量 的热量 |
您最近一年使用:0次


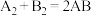 的能量变化如图所示,则下列说法中正确的是
的能量变化如图所示,则下列说法中正确的是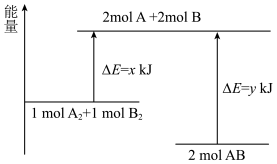
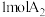 和
和 的总能量低于2molAB的总能量
的总能量低于2molAB的总能量

