为节省药品和时间,甲、乙、丙三位同学选用铜片、锌片、稀硫酸、CuSO4溶液、直流电源、石墨电极、导线、烧杯、试管等中学化学中常见的药品和仪器(用品),以巧妙的构思,“接力”的方式,设计了比较铜与锌的金属活动性相对强弱的系列实验。试回答下列问题:
(1)甲同学分别将一小片铜片、锌片置于烧杯底部(铜与锌不接触),小心向烧杯中加入稀硫酸,可以观察到的现象是:_______________________ 。甲同学的设计思路是_______________________ 。
(2)乙同学接着甲同学的实验,向烧杯中滴加少量_________ (填化学式)溶液,进而观察到的现象是_______________ 。乙同学判断锌、铜的金属活动性相对强弱所依据的原理是________________________ 。
(3)再单独设计一个电化学方面的实验(试剂、仪器自选), 在方框内画出装置图_________ ,探究锌和铜的金属活动性的相对强弱(简要说明操作和现象)_____________________________________ 。
(1)甲同学分别将一小片铜片、锌片置于烧杯底部(铜与锌不接触),小心向烧杯中加入稀硫酸,可以观察到的现象是:
(2)乙同学接着甲同学的实验,向烧杯中滴加少量
(3)再单独设计一个电化学方面的实验(试剂、仪器自选), 在方框内画出装置图
更新时间:2020/10/11 09:22:48
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】有甲、乙两位学生均想利用原电池反应检测金属的活动性顺序,两人均使用镁片与铝片作电极,但甲同学将电极放入2 mol·L-1H2SO4溶液中,乙同学将电极放入2mol·L-1的NaOH溶液中,如下图所示。
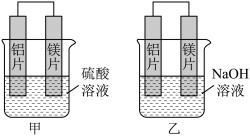
(1)甲池中,镁片上发生_________ (填“氧化”或“还原”)反应,硫酸根离子往_________ (填“正极”或“负极”)迁移;写出甲池中正极的电极反应式:_____________________ 。
(2)写出乙池中负极的电极反应式:_____________________ 。
(3)如果甲与乙同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出_________ 活动性更强,而乙会判断出________ 活动性更强(填写元素符号)。
(4)由此实验,以下结论正确的是_____________ 。
A.利用原电池反应判断金属活动顺序时应注意选择合适的介质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动顺序表已过时,已没有实用价值
D.该实验说明化学研究对象复杂、反应受条件影响较大,因此应具体问题具体分析
(5)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应为3Zn +2K2FeO4+8H2O 3Zn(OH)3+2Fe(OH)3+4KOH 。则放电时,正极反应方程式
3Zn(OH)3+2Fe(OH)3+4KOH 。则放电时,正极反应方程式___________________ 。

(1)甲池中,镁片上发生
(2)写出乙池中负极的电极反应式:
(3)如果甲与乙同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出
(4)由此实验,以下结论正确的是
A.利用原电池反应判断金属活动顺序时应注意选择合适的介质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动顺序表已过时,已没有实用价值
D.该实验说明化学研究对象复杂、反应受条件影响较大,因此应具体问题具体分析
(5)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应为3Zn +2K2FeO4+8H2O
 3Zn(OH)3+2Fe(OH)3+4KOH 。则放电时,正极反应方程式
3Zn(OH)3+2Fe(OH)3+4KOH 。则放电时,正极反应方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】利用原电池原理可比较金属的活泼性,原电池中,作负极的金属活动性一般比作正极的金属活动性强。结合相关知识解答下列问题。由A、B、C三种金属按表中装置进行实验:
(1)在甲中,金属片_______ (填“A”或“B”)发生氧化反应。
(2)在乙中,金属片_______ (填“B”或“C”)作负极。
(3)如果把B、C用导线连接后同时浸入稀硫酸溶液中,有一电极产生气泡。则金属片_______ (填“B”或“C”)上有气泡产生。
(4)上述三种金属的活动性顺序是_______ 。
(5)氢氧燃料电池在酸性环境下的电极式:
负极:_______ 。
正极:_______ 。
| 装置 | 甲 | 乙 |
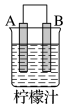 | 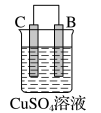 | |
| 现象 | A不断溶解,B上产生气泡 | C的质量增加,B的质量减轻 |
(2)在乙中,金属片
(3)如果把B、C用导线连接后同时浸入稀硫酸溶液中,有一电极产生气泡。则金属片
(4)上述三种金属的活动性顺序是
(5)氢氧燃料电池在酸性环境下的电极式:
负极:
正极:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】工业上从海水中提取金属镁,工艺流程如图:
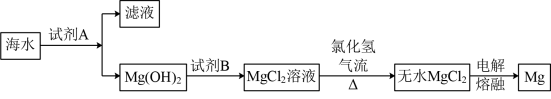
(1)试剂A为____ (填名称,下同),试剂B为____ 。
(2)为探究制得的金属镁与金属铜、钛的金属活动性强弱,某兴趣小组将打磨过的钛片投入硫酸铜溶液中,一段时间后在钛片的表面析出红色固体,则钛和铜的金属活泼性:Ti____ Cu(填“>”,“<”或“=”),上述反应的离子方程式为____ 。(已知Ti在化合物中一般显+4价)。为比较镁与钛的金属活泼性强弱,该兴趣小组设计原电池如图所示:
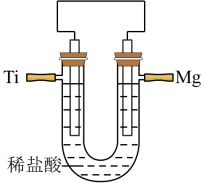
若Mg片不断溶解,Ti片上有无色气泡产生,则可证明Ti____ Mg(填“>”、“<”或“=”)。请写出该电池的负极的电极反应式:____ 。

(1)试剂A为
(2)为探究制得的金属镁与金属铜、钛的金属活动性强弱,某兴趣小组将打磨过的钛片投入硫酸铜溶液中,一段时间后在钛片的表面析出红色固体,则钛和铜的金属活泼性:Ti

若Mg片不断溶解,Ti片上有无色气泡产生,则可证明Ti
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】如图,C、D、E、F、X、Y都是惰性电极,A、B为电源。将电源接通后,向(乙)中滴入酚酞溶液,在F极附近显红色。
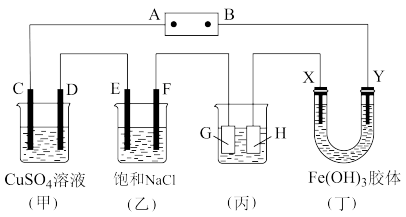
(1)若用CO、氧气燃料电池作电源,电解质为KOH溶液,则A为____ 极,B电极上的反应式为:__________________________________ 。
(2)若甲中装有100ml 1 mol•L-1的硫酸铜溶液,工作一段时间后,停止通电此时C、D两极上都产生2.24L气体(标准状况),C极气体为____ (化学式),D极气体为____ (化学式),欲使溶液恢复到起始状态,可向溶液中加入____ 。
A.CuO B.Cu2(OH)2CO3 C.Cu(OH)2 D.CuCO3
(3)通电后乙中反应的化学方程式:__________________________________ 。
(4)工作一段时间后,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这说明Fe(OH)3胶粒带________ 电,在电场作用下向Y极移动。

(1)若用CO、氧气燃料电池作电源,电解质为KOH溶液,则A为
(2)若甲中装有100ml 1 mol•L-1的硫酸铜溶液,工作一段时间后,停止通电此时C、D两极上都产生2.24L气体(标准状况),C极气体为
A.CuO B.Cu2(OH)2CO3 C.Cu(OH)2 D.CuCO3
(3)通电后乙中反应的化学方程式:
(4)工作一段时间后,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这说明Fe(OH)3胶粒带
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】以V2O5为原料制备氧钒(Ⅳ)碱式碳酸铵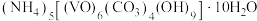 .其过程
.其过程 溶液
溶液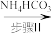 氧钒(Ⅳ)碱式碳酸铵粗产品
氧钒(Ⅳ)碱式碳酸铵粗产品
已知VO2+能被O2氧化,回答下列问题:
(1)步骤Ⅰ的反应装置如右图(夹持及加热装置略去)

①仪器a的名称为___________ ,使用此仪器的优点是_________________________ 。
②步骤Ⅰ生成 的同时,还生成一种无色无污染的气体,该反应的化学方程式为
的同时,还生成一种无色无污染的气体,该反应的化学方程式为_____________________________________ 。
(2)步骤Ⅱ可在如下图装置中进行.
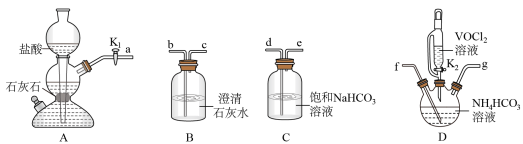
①接口的连接顺序为
___________ 。
②实验开始时,关闭 ,打开
,打开 ,其目的是
,其目的是__________________________ .当___________ 时(写实验现象),再关闭 ,打开
,打开 ,充分反应,静置,得到固体。
,充分反应,静置,得到固体。
(3)测定产品纯度
称取 氧钒(Ⅳ)碱式碳酸铵粗产品经处理后,钒(V)元素均以
氧钒(Ⅳ)碱式碳酸铵粗产品经处理后,钒(V)元素均以 的形式存在,然后用
的形式存在,然后用 标准溶液滴定达终点时,消耗体积为
标准溶液滴定达终点时,消耗体积为 。
。
(已知: )
)
产品中氧钒(Ⅳ)碱式碳酸铵(摩尔质量为 )的质量分数为
)的质量分数为___________ 。
(4)全钒液流电池是一种新型的绿色环保储能电池,工作原理如图所示,a、b均为惰性电极,放电时左槽溶液颜色由黄色变为蓝色.
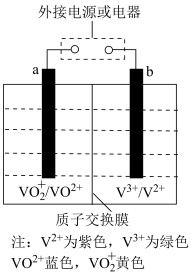
其充电时,阳极的电极方程式为_______________________________________ 。
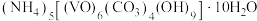 .其过程
.其过程 溶液
溶液 氧钒(Ⅳ)碱式碳酸铵粗产品
氧钒(Ⅳ)碱式碳酸铵粗产品已知VO2+能被O2氧化,回答下列问题:
(1)步骤Ⅰ的反应装置如右图(夹持及加热装置略去)

①仪器a的名称为
②步骤Ⅰ生成
 的同时,还生成一种无色无污染的气体,该反应的化学方程式为
的同时,还生成一种无色无污染的气体,该反应的化学方程式为(2)步骤Ⅱ可在如下图装置中进行.

①接口的连接顺序为

②实验开始时,关闭
 ,打开
,打开 ,其目的是
,其目的是 ,打开
,打开 ,充分反应,静置,得到固体。
,充分反应,静置,得到固体。(3)测定产品纯度
称取
 氧钒(Ⅳ)碱式碳酸铵粗产品经处理后,钒(V)元素均以
氧钒(Ⅳ)碱式碳酸铵粗产品经处理后,钒(V)元素均以 的形式存在,然后用
的形式存在,然后用 标准溶液滴定达终点时,消耗体积为
标准溶液滴定达终点时,消耗体积为 。
。(已知:
 )
)产品中氧钒(Ⅳ)碱式碳酸铵(摩尔质量为
 )的质量分数为
)的质量分数为(4)全钒液流电池是一种新型的绿色环保储能电池,工作原理如图所示,a、b均为惰性电极,放电时左槽溶液颜色由黄色变为蓝色.

其充电时,阳极的电极方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节能30%以上,并同时制得 和
和 溶液。相关物料的传输与转化关系如图所示:
溶液。相关物料的传输与转化关系如图所示:
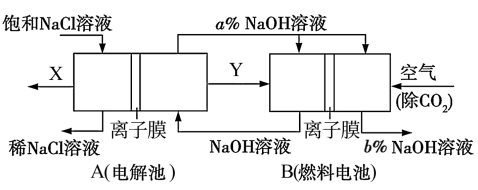
请回答下列问题:
(1)A池总反应的离子反应方程式为___________ 。燃料电池B中正极上发生的电极反应式为___________ 。
(2)装置中的离子膜是阳离子交换膜,当阴极产生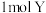 时,通过离子交换膜的
时,通过离子交换膜的 有
有___________  。
。
(3)装置图中氢氧化钠溶液质量分数的大小:
___________ 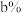 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
 和
和 溶液。相关物料的传输与转化关系如图所示:
溶液。相关物料的传输与转化关系如图所示:
请回答下列问题:
(1)A池总反应的离子反应方程式为
(2)装置中的离子膜是阳离子交换膜,当阴极产生
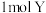 时,通过离子交换膜的
时,通过离子交换膜的 有
有 。
。(3)装置图中氢氧化钠溶液质量分数的大小:

 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
您最近一年使用:0次



