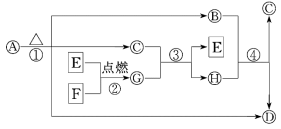
A~H为中学化学中常见的物质,转化关系如图所示,其中“○”代表化合物,“□”代表单质,A为医学上治疗胃酸过多的一种药剂,G为淡黄色固体,C在通常状况下为无色液体。
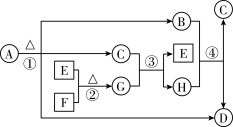
请回答下列问题:
(1)G的化学式为_______ 。
(2)反应①②③④中_______ (填序号)属于氧化还原反应。
(3)写出F+C反应的化学反应方程式:_______ 。
(4)向盛有D溶液的试管中滴加稀盐酸,产生的实验现象为_______ ,用离子方程式解释现象_______ 。

请回答下列问题:
(1)G的化学式为
(2)反应①②③④中
(3)写出F+C反应的化学反应方程式:
(4)向盛有D溶液的试管中滴加稀盐酸,产生的实验现象为
更新时间:2020-10-16 14:43:05
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】粉煤灰是燃煤电厂排出的主要固体废物,以某电厂的粉煤灰(主要含 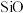 2
2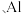 2O3和CaO 等)为原料提取铝的部分工艺流程如下:
2O3和CaO 等)为原料提取铝的部分工艺流程如下:
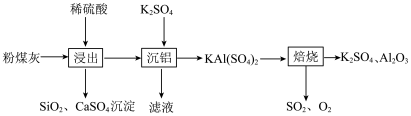
回答下列问题:
(1)上述流程中,用化学式表示的物质中属于金属氧化物的有_______ (填化学式,下同),属于酸性氧化物的有 SO2、_______ ,其中常温下为固态的酸性氧化物与 NaOH 溶液反应的化学方程式为_______ 。
(2)写出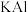 (SO4)2在水溶液中的电离方程式:
(SO4)2在水溶液中的电离方程式:_______ ,其是否属于盐类?_______ (填“是”或“否”)。
(3)向 2
2 4稀溶液中逐滴滴入
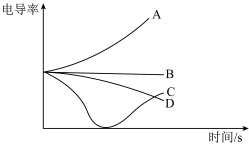
4稀溶液中逐滴滴入 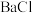 2浓溶液至沉淀不再增加,该过程中溶液电导率随时间变化的趋势正确的是
2浓溶液至沉淀不再增加,该过程中溶液电导率随时间变化的趋势正确的是_______ (填序号,溶液的体积变化忽略不计)。
(4)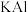 (SO4)2焙烧的反应既属于
(SO4)2焙烧的反应既属于_______ 反应(填四大基本反应类型),又属于_______ 反应(填“氧化还原”或“非氧化还原”)。
(5)将固体 CaSO4研磨为纳米级颗粒后分散到盛有水的烧杯中,如何证明该体系为胶体?_______ (写出实验操作、现象和结论)。
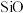 2
2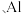 2O3和CaO 等)为原料提取铝的部分工艺流程如下:
2O3和CaO 等)为原料提取铝的部分工艺流程如下:
回答下列问题:
(1)上述流程中,用化学式表示的物质中属于金属氧化物的有
(2)写出
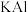 (SO4)2在水溶液中的电离方程式:
(SO4)2在水溶液中的电离方程式:(3)向
 2
2 4稀溶液中逐滴滴入
4稀溶液中逐滴滴入 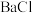 2浓溶液至沉淀不再增加,该过程中溶液电导率随时间变化的趋势正确的是
2浓溶液至沉淀不再增加,该过程中溶液电导率随时间变化的趋势正确的是
(4)
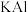 (SO4)2焙烧的反应既属于
(SO4)2焙烧的反应既属于(5)将固体 CaSO4研磨为纳米级颗粒后分散到盛有水的烧杯中,如何证明该体系为胶体?
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】回答下列问题:
(1)将黑色的 固体加入足量盐酸中,溶液中有淡黄色固体生成,产物还有
固体加入足量盐酸中,溶液中有淡黄色固体生成,产物还有_______ 、_______ 。过滤,微热滤液,然后加入过量的氢氧化钠溶液,可观察到的现象是_______ 。
(2)Bunsen热化学循环制氢工艺由下列三个反应组成:
①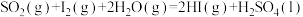
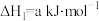
②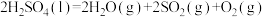

③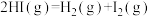
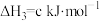
则:
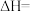
_______ 。
(3) 和
和 的燃烧热分别为
的燃烧热分别为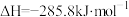 和
和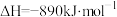 ,标准状况下
,标准状况下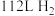 和
和 的混合气体完全燃烧生成
的混合气体完全燃烧生成 气体和液态水时放出
气体和液态水时放出 热量,则混合气体中
热量,则混合气体中 和
和 的物质的量之比是
的物质的量之比是_______ 。
(4)氯化铵固体溶于水温度降低,请解释原因_______ 。
(5)合成氨反应:
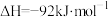 ;
;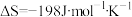 。
。
①判断该反应在室温下能否自发进行?为什么?_______ 。
③室温下推动该反应自发进行的主要因素是熵变还是焓变_______ ?
(1)将黑色的
 固体加入足量盐酸中,溶液中有淡黄色固体生成,产物还有
固体加入足量盐酸中,溶液中有淡黄色固体生成,产物还有(2)Bunsen热化学循环制氢工艺由下列三个反应组成:
①
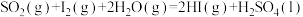
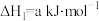
②
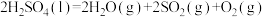

③
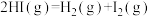
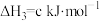
则:

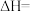
(3)
 和
和 的燃烧热分别为
的燃烧热分别为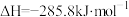 和
和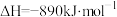 ,标准状况下
,标准状况下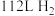 和
和 的混合气体完全燃烧生成
的混合气体完全燃烧生成 气体和液态水时放出
气体和液态水时放出 热量,则混合气体中
热量,则混合气体中 和
和 的物质的量之比是
的物质的量之比是(4)氯化铵固体溶于水温度降低,请解释原因
(5)合成氨反应:

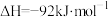 ;
;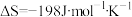 。
。①判断该反应在室温下能否自发进行?为什么?
③室温下推动该反应自发进行的主要因素是熵变还是焓变
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】某单质A经如图所示的过程,A、B、C、D均含有同一种元素,请回答下列问题:
A B
B C
C D
D
(1)若A为淡黄色固体,B是有刺激性气味的无色气体。
①A、D的化学式分别为:A___ ,D___ 。
②工业生产中大量排放的B气体被雨水吸收后形成___ 而污染环境。
③写出B→C反应的化学方程式:___ 。
(2)若C为淡黄色固体。
①C的电子式为___ ,C中阴阳离子数目比为___ 。
②D中化学键类型___ (“离子键”“极性键”或“非极性键”)
③写出C→D反应的离子方程式:___ 。
(3)C为红棕色气体。
①A的电子式为___ 。
②写出C→D反应的化学方程式___ 。
A
 B
B C
C D
D(1)若A为淡黄色固体,B是有刺激性气味的无色气体。
①A、D的化学式分别为:A
②工业生产中大量排放的B气体被雨水吸收后形成
③写出B→C反应的化学方程式:
(2)若C为淡黄色固体。
①C的电子式为
②D中化学键类型
③写出C→D反应的离子方程式:
(3)C为红棕色气体。
①A的电子式为
②写出C→D反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】图中,A是单质,B的焰色反应呈黄色。判断A、B、C、D的化学式:
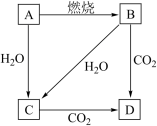
(1)A______ ,B______ ,C______ ,D______ 。
(2)下列转化的化学方程式为:A→C_____________ 。

(1)A
(2)下列转化的化学方程式为:A→C
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】钠是一种重要的金属。中国科学技术大学的钱逸泰教授等以 和金属钠为原料,在700℃时制造出纳米级金刚石粉末。该成果发表在世界权威的《科学》杂志上,立刻被科学家们高度评价为“稻草变黄金”。
和金属钠为原料,在700℃时制造出纳米级金刚石粉末。该成果发表在世界权威的《科学》杂志上,立刻被科学家们高度评价为“稻草变黄金”。
(1)同学们对此有下列一些理解,其中错误的是_______
(2)解释钠与水反应的实验现象的原因有:
A.钠与水界面各部分产生 的量不同,所受推力不均匀;
的量不同,所受推力不均匀;
B.钠的密度比水小;
C.钠与水反应放热,使熔点低的钠熔化成小球;
D.反应很剧烈;
E.生成的氢氧化钠使酚酞试液变红。
请在下表填写与描述的现象相对应的原因。
(3)为验证过氧化钠与水的反应,某学习小组设计了如图所示的装置(夹持仪器已略去)并进行实验。

请回答下列问题:
①仪器a的名称为_______ 。
②装置C中可观察到的实验现象为_______ 。
③装置A中发生反应的化学方程式为_______ 。
 和金属钠为原料,在700℃时制造出纳米级金刚石粉末。该成果发表在世界权威的《科学》杂志上,立刻被科学家们高度评价为“稻草变黄金”。
和金属钠为原料,在700℃时制造出纳米级金刚石粉末。该成果发表在世界权威的《科学》杂志上,立刻被科学家们高度评价为“稻草变黄金”。(1)同学们对此有下列一些理解,其中错误的是_______
| A.金刚石属于金属单质 | B.制造过程中元素种类没有改变 |
C. 是一种化合物 是一种化合物 | D.这个反应是置换反应 |
A.钠与水界面各部分产生
 的量不同,所受推力不均匀;
的量不同,所受推力不均匀;B.钠的密度比水小;
C.钠与水反应放热,使熔点低的钠熔化成小球;
D.反应很剧烈;
E.生成的氢氧化钠使酚酞试液变红。
请在下表填写与描述的现象相对应的原因。
| 实验现象 | 原因填以上序号 |
| 熔成闪亮的小球 | |
| 小球向各个方向迅速游动 | |
| 实验过程中,发出“嘶嘶”的响声 |

请回答下列问题:
①仪器a的名称为
②装置C中可观察到的实验现象为
③装置A中发生反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系。已知B、C、D是非金属单质,且在常温常压下都是气体,D常用于自来水的杀菌、消毒;化合物G的焰色试验呈黄色,化合物F通常状况下呈气态。请回答下列问题。
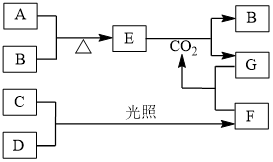
(1)A、B、C、D、E、F、G各为什么物质_____ ?
(2)写出下列物质间反应的化学方程式:A和B_____ ;E和
_____ 。
(3)写出化合物G与F反应的离子方程式_____ 。

(1)A、B、C、D、E、F、G各为什么物质
(2)写出下列物质间反应的化学方程式:A和B

(3)写出化合物G与F反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐2】1940年我国著名科学家侯德榜先生,冲破“索尔维法”技术封锁,并加以改进,生产出 和
和 两种产品,这便是举世闻名的“侯氏联合制碱法”。以下是索尔维法和侯氏制碱法的工艺流程。
两种产品,这便是举世闻名的“侯氏联合制碱法”。以下是索尔维法和侯氏制碱法的工艺流程。
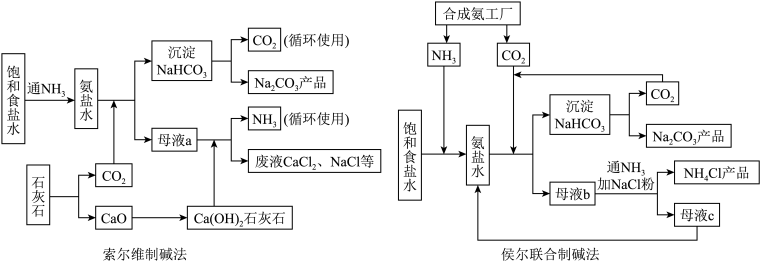
已知:NH3+H2O=NH3∙H2O (一种弱碱)。
I、根据两个流程图回答:
(1)在制备流程中先通入NH3的原因是_______ 。
(2)请分别用一个化学方程式表示两种制碱法的总反应方程式:_______ 、_______ 。
(3)向母液b中通氨气,加入食盐粉,降温结晶析出副产品,通氨气的作用有_______(填序号)。
(4)相比“索尔维制碱法”,“侯氏联合制碱法”的优点有_______(填序号)。
II、工业制碱所得碳酸钠中往往含有少量 。现欲分析某样品中
。现欲分析某样品中 的含量,将25g样品放入干净的烧杯中,加入200g水使其完全溶解,向所得溶液中慢慢加入质量分数为14.6%的盐酸,烧杯中溶液的质量与加入盐酸的质量关系曲线如图所示。请回答下列问题:
的含量,将25g样品放入干净的烧杯中,加入200g水使其完全溶解,向所得溶液中慢慢加入质量分数为14.6%的盐酸,烧杯中溶液的质量与加入盐酸的质量关系曲线如图所示。请回答下列问题:
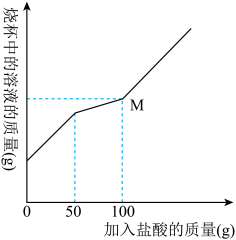
(5)在25g碳酸钠和氯化钠的混合物样品中,碳酸钠的物质的量为_______ 。
(6)已知M点溶液为不饱和溶液,溶质的质量分数为_______ 。(忽略 的溶解,计算结果保留两位有效数字)
的溶解,计算结果保留两位有效数字)
 和
和 两种产品,这便是举世闻名的“侯氏联合制碱法”。以下是索尔维法和侯氏制碱法的工艺流程。
两种产品,这便是举世闻名的“侯氏联合制碱法”。以下是索尔维法和侯氏制碱法的工艺流程。
已知:NH3+H2O=NH3∙H2O (一种弱碱)。
I、根据两个流程图回答:
(1)在制备流程中先通入NH3的原因是
(2)请分别用一个化学方程式表示两种制碱法的总反应方程式:
(3)向母液b中通氨气,加入食盐粉,降温结晶析出副产品,通氨气的作用有_______(填序号)。
A.使 结晶析出 结晶析出 |
B.使 更多地析出 更多地析出 |
C.增大 浓度,使 浓度,使 更多地析出 更多地析出 |
D.使 转化为 转化为 ,提高析出的 ,提高析出的 纯度 纯度 |
A. 利用率高,在物资匮乏的战争年代,可降低制碱成本 利用率高,在物资匮乏的战争年代,可降低制碱成本 |
B.副产品 可作化肥,提高产品经济收益 可作化肥,提高产品经济收益 |
C.制碱用的氨和二氧化碳直接由制氨厂提供,代替分解 制 制 的方法,节约能源、减少污染 的方法,节约能源、减少污染 |
| D.生产出的纯碱纯度较高 |
II、工业制碱所得碳酸钠中往往含有少量
 。现欲分析某样品中
。现欲分析某样品中 的含量,将25g样品放入干净的烧杯中,加入200g水使其完全溶解,向所得溶液中慢慢加入质量分数为14.6%的盐酸,烧杯中溶液的质量与加入盐酸的质量关系曲线如图所示。请回答下列问题:
的含量,将25g样品放入干净的烧杯中,加入200g水使其完全溶解,向所得溶液中慢慢加入质量分数为14.6%的盐酸,烧杯中溶液的质量与加入盐酸的质量关系曲线如图所示。请回答下列问题:
(5)在25g碳酸钠和氯化钠的混合物样品中,碳酸钠的物质的量为
(6)已知M点溶液为不饱和溶液,溶质的质量分数为
 的溶解,计算结果保留两位有效数字)
的溶解,计算结果保留两位有效数字)
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】下列三组物质中,均有一种物质的类别与其他三种不同。
①MgO、Na2O、CO2、CuO;②HCl、H2O、H2SO4、HNO3;③NaOH、Na2CO3、KOH、Cu(OH)2
(1)三种物质依次是(填化学式):A___________ ;B___________ ;C___________ 。
(2)这三种物质相互作用可生成一种新物质NaHCO3,该反应___________ (填“是”或“不是”)氧化还原反应。写出NaHCO3的电离方程式;___________ 。
(3)写出物质C与足量稀盐酸反应的离子方程式:___________ 。
(4) 与H+在溶液中能共存吗?试用离子方程式说明
与H+在溶液中能共存吗?试用离子方程式说明___________ 。
①MgO、Na2O、CO2、CuO;②HCl、H2O、H2SO4、HNO3;③NaOH、Na2CO3、KOH、Cu(OH)2
(1)三种物质依次是(填化学式):A
(2)这三种物质相互作用可生成一种新物质NaHCO3,该反应
(3)写出物质C与足量稀盐酸反应的离子方程式:
(4)
 与H+在溶液中能共存吗?试用离子方程式说明
与H+在溶液中能共存吗?试用离子方程式说明
您最近一年使用:0次