(1)以下列出的是一些原子的2p能级和3d能级中电子排布的情况。试判断,违反了泡利原理的是______ ,违反了洪特规则的是______ 。
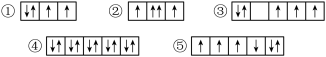
(2)用符号“>”“<”或“=”表示下列各项关系。
①第一电离能:Na______ Mg,Mg______ Ca。
②电负性:O______ F,F______ Cl。
③能量高低:ns______ (n+1)s,ns______ np。

(2)用符号“>”“<”或“=”表示下列各项关系。
①第一电离能:Na
②电负性:O
③能量高低:ns
20-21高二上·宁夏银川·阶段练习 查看更多[3]
(已下线)1.2 原子结构与元素的性质(C级检测练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)(已下线)易错25 电离能和电负性-备战2021年高考化学一轮复习易错题宁夏回族自治区银川市宁夏大学附属中学2020-2021学年高二上学期第一次月考化学试题
更新时间:2020-10-16 06:07:39
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】以下列出的是一些原子的2p能级和3d能级中电子的排布情况。试判断,违反了泡利不相容原理的是 ___________ (填序号,下同),违反了洪特规则的是 _______ 。
① ②
②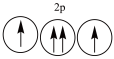 ③
③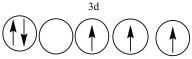 ④
④ ⑤
⑤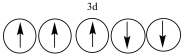
①
 ②
② ③
③ ④
④ ⑤
⑤
您最近半年使用:0次
填空题
|
较易
(0.85)
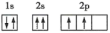
【推荐2】下列原子或离子的电子排布式或轨道表示式正确的是___________ (填序号,下同),违反能量最低原理的是___________ ,违反洪特规则的是___________ ,违反泡利原理的是___________ 。
① :
:
② :
:
③ :
: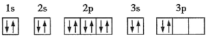
④ :
: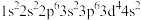
⑤ :
: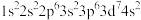
⑥ :
:
⑦ :
:
①
 :
:
②
 :
:
③
 :
: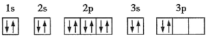
④
 :
: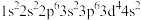
⑤
 :
: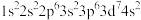
⑥
 :
:
⑦
 :
:
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】根据原子核外电子排布规则,回答下列问题:
(1)写出基态S原子的核外电子排布式___________________________________ ,写出基态24Cr原子的价电子排布式________________________ ;
(2)写出基态N的原子核外电子排布图:__________________ ;
(3)若将基态14Si的电子排布式写成1s22s22p63s33p1,则它违背了_______________________ ;
(4)Fe3+比Fe2+的稳定性更________ (填“强”或“弱”),从结构上分析原因是____________________________________________________________________________ 。
(1)写出基态S原子的核外电子排布式
(2)写出基态N的原子核外电子排布图:
(3)若将基态14Si的电子排布式写成1s22s22p63s33p1,则它违背了
(4)Fe3+比Fe2+的稳定性更
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐1】下列原子或离子的电子排布式或轨道表示式正确的是___________ (填序号,下同),违反能量最低原理的是___________ ,违反洪特规则的是___________ ,违反泡利原理的是___________ 。
① :
:
② :
:
③ :
: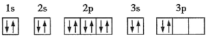
④ :
: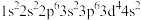
⑤ :
: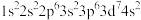
⑥ :
:
⑦ :
:
①
 :
:
②
 :
:
③
 :
: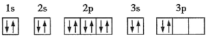
④
 :
: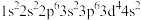
⑤
 :
: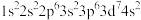
⑥
 :
:
⑦
 :
:
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】根据原子核外电子排布规则,回答下列问题:
(1)写出基态S原子的核外电子排布式___________________________________ ,写出基态24Cr原子的价电子排布式________________________ ;
(2)写出基态N的原子核外电子排布图:__________________ ;
(3)若将基态14Si的电子排布式写成1s22s22p63s33p1,则它违背了_______________________ ;
(4)Fe3+比Fe2+的稳定性更________ (填“强”或“弱”),从结构上分析原因是____________________________________________________________________________ 。
(1)写出基态S原子的核外电子排布式
(2)写出基态N的原子核外电子排布图:
(3)若将基态14Si的电子排布式写成1s22s22p63s33p1,则它违背了
(4)Fe3+比Fe2+的稳定性更
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐3】Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
(1)基态Fe3+离子中未成对的电子数为_____ 。
(2)Li及其周期表中相邻元素的第一电离能I1大小比较关系如下:I1(Li)> I1(Na),原因是__ ,Li、Be、B三元素的第一电离能I1(Be)、 I1(B)、 I1(Li)之间的大小关系是__ 。
(3)磷酸根离子的空间构型为__ ,其中P的价层电子对数为__ 、杂化轨道类型为__ 。
(1)基态Fe3+离子中未成对的电子数为
(2)Li及其周期表中相邻元素的第一电离能I1大小比较关系如下:I1(Li)> I1(Na),原因是
(3)磷酸根离子的空间构型为
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐1】甘氨酸(分子式C2H5NO2)分子中,共有___________ 个σ键。甘氨酸分子中C原子的杂化方式为___________ 。
A. sp B. sp2 C. sp3
甘氨酸钠中第一电离能最小的元素为___________ 。
A. C B. O C. Na D. N
A. sp B. sp2 C. sp3
甘氨酸钠中第一电离能最小的元素为
A. C B. O C. Na D. N
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】(1)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图所示,其中除氮元素外,其他元素的E1自左而右依次增大的原因是___ ;氮元素的E1呈现异常的原因是__ 。

(2)C、H、O三种元素的电负性由小到大的顺序为___ 。
(3)元素铜与镍的第二电离能分别为:ICu=1958kJ·mol-1、INi=1753kJ·mol-1,ICu>INi的原因是__ 。

(2)C、H、O三种元素的电负性由小到大的顺序为
(3)元素铜与镍的第二电离能分别为:ICu=1958kJ·mol-1、INi=1753kJ·mol-1,ICu>INi的原因是
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐1】非金属氟化物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态F原子核外电子的运动状态有_______ 种。
(2)O、F、Cl电负性由大到小的顺序为________ ;OF2分子的空间构型为_______ ;OF2的熔、沸点_______ (填“高于”或“低于”)Cl2O,原因是________ 。
(1)基态F原子核外电子的运动状态有
(2)O、F、Cl电负性由大到小的顺序为
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】根据元素周期表中完整周期元素的性质,在下列空格中填上适当的元素符号。
(1)在第三周期中,第一电离能最小的元素是________ ,第一电离能最大的元素是________ 。
(2)在元素周期表中,电负性最大的元素是________
(3)第二周期,原子最外电子层中p能级半充满的元素是________ 。
(1)在第三周期中,第一电离能最小的元素是
(2)在元素周期表中,电负性最大的元素是
(3)第二周期,原子最外电子层中p能级半充满的元素是
您最近半年使用:0次
【推荐3】第四周期的元素形成的化合物在生产生活中有着重要的用途。
(1)镍铬钢抗腐蚀性能强,基态铬原子的价电子排布式为___________ ,按照电子排布式,镍元素在周期表中位于___________ 区。
(2)“玉兔二号”月球车通过砷化镓(GaAs)太阳能电池提供能量进行工作。基态砷原子的电子占据最高能级的电子云轮廓图为___________ 形。砷的电负性比镓___________ (填“大”或“小”)。
(3)基态Fe3+、Fe2+离子中未成对的电子数之比为___________ 。
(1)镍铬钢抗腐蚀性能强,基态铬原子的价电子排布式为
(2)“玉兔二号”月球车通过砷化镓(GaAs)太阳能电池提供能量进行工作。基态砷原子的电子占据最高能级的电子云轮廓图为
(3)基态Fe3+、Fe2+离子中未成对的电子数之比为
您最近半年使用:0次



