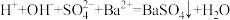高铁酸钾是一种高效绿色水处理剂,其工业制备的反应原理是:Fe(OH)3+ClO-+OH-→ +Cl-+H2O(未配平),下列叙述正确的是
+Cl-+H2O(未配平),下列叙述正确的是
 +Cl-+H2O(未配平),下列叙述正确的是
+Cl-+H2O(未配平),下列叙述正确的是| A.ClO-是还原剂 |
| B.每1个Fe(OH)3得到3个电子 |
| C.反应配平后,H2O的化学计量数为4 |
| D.用高铁酸钾处理水时,用到了其强氧化性,且其还原产物能水解产生具有强吸附能力的胶体 |
更新时间:2020-10-21 21:46:37
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】常温下,在溶液中发生如下反应:①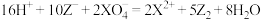 ,②
,②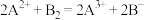 ,③
,③ 。由此推断下列说法不正确的是
。由此推断下列说法不正确的是
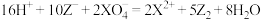 ,②
,②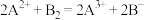 ,③
,③ 。由此推断下列说法不正确的是
。由此推断下列说法不正确的是| A.Z元素在反应③中被还原 |
B. 具有还原性 具有还原性 |
C.在反应①中,每消耗1mol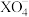 ,转移电子5mol ,转移电子5mol |
D.在常温下,反应 可以进行 可以进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列关于氧化还原反应的叙述中,正确的是
| A.一种元素被氧化,肯定有另一种元素被还原 |
| B.氧化还原反应的实质是电子的转移 |
| C.某元素由化合态变为游离态,则该元素一定被还原 |
| D.氧化还原反应中,得电子越多,氧化性越强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】关于反应 ,下列说法
,下列说法不正确 的是
 ,下列说法
,下列说法A. 中氮元素被还原 中氮元素被还原 | B.氧化产物和还原产物的物质的量之比为 |
C. 中氮原子失去电子 中氮原子失去电子 | D.氧化剂和还原剂的物质的量之比为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】 表示阿伏加 德罗常数,下列说法中正确的是
表示阿伏加 德罗常数,下列说法中正确的是
 表示阿伏加 德罗常数,下列说法中正确的是
表示阿伏加 德罗常数,下列说法中正确的是 A.1 mol  与足量氯气反应时转移的电子数为 与足量氯气反应时转移的电子数为 |
B.标准状况下, 丙烷中含有共价键的数目为 丙烷中含有共价键的数目为 |
C.16g由氧气和臭氧组成的混合物中含有的分子总数为  |
D. mol乙烯和乙醇的混合物完全燃烧所消耗的氧原子数一定为 mol乙烯和乙醇的混合物完全燃烧所消耗的氧原子数一定为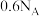 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】用NA代表阿伏加德罗常数的值,下列说法中正确的是
| A.18g水中含有的氢原子数目为NA |
| B.1mol氩气分子所含的原子数目为2NA |
| C.53g碳酸钠中含有的钠离子为0.5NA |
| D.7.8gNa2O2与足量的CO2反应时转移的电子数为0.1NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】S2Cl2是橙黄色液体,少量泄漏会产生窒息性气体,喷水雾可减慢其挥发,并产生酸性悬浊液。其分子结构如图所示。下列关于S2Cl2的说法不正确的是
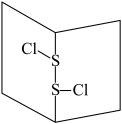

| A.结构式为Cl-S-S-Cl |
| B.是含有极性键的非极性分子 |
| C.与S2Br2结构相似,熔、沸点:S2Br2>S2Cl2 |
| D.与水反应的化学方程式可能为2S2Cl2+2H2O=SO2↑+3S↓+4HCl |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在探究影响化学反应速率的因素时,将H2C2O4溶液滴入KMnO4酸性溶液中,一段时间后,溶液突然变成无色,发生反应:KMnO4+H2C2O4+H2SO4 K2SO4+MnSO4+CO2+H2O(没有配平)。下列有关说法错误的是( )
K2SO4+MnSO4+CO2+H2O(没有配平)。下列有关说法错误的是( )
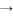 K2SO4+MnSO4+CO2+H2O(没有配平)。下列有关说法错误的是( )
K2SO4+MnSO4+CO2+H2O(没有配平)。下列有关说法错误的是( )| A.H2C2O4中C的化合价为+3 |
| B.每生成22.4L(标况)CO2,转移电子2mol |
| C.该反应中,氧化剂与还原剂物质的量之比为2:5 |
| D.溶液突然褪色的原因是产物MnSO4对该反应有催化作用 |
您最近一年使用:0次

 溶液中通入少量
溶液中通入少量 气体:
气体: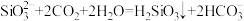
 氧化
氧化 :
: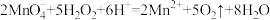
 溶液反应:
溶液反应:
 溶液反应:
溶液反应: