现有失去标签的氯化钙、硝酸银、盐酸、碳酸钠四种无色溶液,为了测定四种溶液各是什么?将它们随意编号为A、B、C、D后,按下表进行实验。产生的现象如下所示:
根据实验现象按要求回答:
(1)A、B、C、D溶液中溶质的化学式:A:________ ;C:__________ 。
(2)写出实验顺序①②中有关的离子方程式,不反应的说明理由。
①_____________ ;②____________ ;
(3)下列离子方程式正确的是_____ 。
①碳酸氢钙溶液与过量烧碱溶液混合:Ca2++ +OH-==CaCO3↓十H2O
+OH-==CaCO3↓十H2O
②碳酸镁与稀硫酸:MgCO3+H+=H2O+CO2↑+Mg+
③醋酸与大理石:2CH3COOH+CaCO3=Ca2++2CH3COO-+H2O+CO2↑
④向NaHSO4溶液逐滴加Ba(OH)2溶液至 刚好沉淀完全:H++
刚好沉淀完全:H++ +Ba2++OH-=H2O+BaSO4↓
+Ba2++OH-=H2O+BaSO4↓
实验顺序 | 实验内容 | 实验现象 |
① | A+B | 没有现象发生 |
② | B+D | 有气体放出 |
③ | C+B | 有沉淀生成 |
④ | A+D | 有沉淀生成 |
(1)A、B、C、D溶液中溶质的化学式:A:
(2)写出实验顺序①②中有关的离子方程式,不反应的说明理由。
①
(3)下列离子方程式正确的是
①碳酸氢钙溶液与过量烧碱溶液混合:Ca2++
 +OH-==CaCO3↓十H2O
+OH-==CaCO3↓十H2O②碳酸镁与稀硫酸:MgCO3+H+=H2O+CO2↑+Mg+
③醋酸与大理石:2CH3COOH+CaCO3=Ca2++2CH3COO-+H2O+CO2↑
④向NaHSO4溶液逐滴加Ba(OH)2溶液至
 刚好沉淀完全:H++
刚好沉淀完全:H++ +Ba2++OH-=H2O+BaSO4↓
+Ba2++OH-=H2O+BaSO4↓
更新时间:2020-10-23 10:31:50
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】某工厂的固体废渣中主要含Cu和CuO,还含有少量SiO2.利用该固体废渣制取Cu(NO3)2·3H2O的部分工艺流程如图所示:

已知:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O;SiO2难于水和酸。
(1)为了加快酸溶的速度,可以采取的措施是_____ 。(任写一条)
(2)滤渣的主要成分为_____ 。
(3)过滤操作需要的玻璃仪器有烧杯、_____ 、_____ 。
(4)以某工业废水(含Cu2+、Na+、SO )为原料,制取Cu(NO3)2·3H2O晶体的实验方案:向工业废水中加入NaOH溶液充分反应,过滤,
)为原料,制取Cu(NO3)2·3H2O晶体的实验方案:向工业废水中加入NaOH溶液充分反应,过滤,_____ ,向滤渣中加入稀硝酸至固体完全溶解,_____ ,降温到温度略高于26.4℃,结晶,过滤,洗涤,干燥。[已知:Cu(NO3)2的溶解度曲线如图所示]。


已知:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O;SiO2难于水和酸。
(1)为了加快酸溶的速度,可以采取的措施是
(2)滤渣的主要成分为
(3)过滤操作需要的玻璃仪器有烧杯、
(4)以某工业废水(含Cu2+、Na+、SO
 )为原料,制取Cu(NO3)2·3H2O晶体的实验方案:向工业废水中加入NaOH溶液充分反应,过滤,
)为原料,制取Cu(NO3)2·3H2O晶体的实验方案:向工业废水中加入NaOH溶液充分反应,过滤,
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】某固体混合物可能由NaCl,K2SO4、FeCl2、CaCl2、K2CO3中的一中或几种混合而成,为鉴定其组成,依次进行如下实验:
①混合物中加入足量水得到无色透明溶液;
②向上述溶液中滴加BaCl2溶液,有白色沉淀产生;
③过滤,然后向上述白色沉淀中加盐酸,沉淀全部溶解;
④向滤液中滴加AgNO3溶液,有白色沉淀产生且白色沉淀不溶于稀硝酸。
(1)肯定存在的物质有_______ (填化学式,下同);
(2)肯定不存在的物质有_______ ;
(3)可能存在的物质有_______ ;
(4)写出第③、④步实验中发生反应的离子方程式:_______ 、_______ 。
①混合物中加入足量水得到无色透明溶液;
②向上述溶液中滴加BaCl2溶液,有白色沉淀产生;
③过滤,然后向上述白色沉淀中加盐酸,沉淀全部溶解;
④向滤液中滴加AgNO3溶液,有白色沉淀产生且白色沉淀不溶于稀硝酸。
(1)肯定存在的物质有
(2)肯定不存在的物质有
(3)可能存在的物质有
(4)写出第③、④步实验中发生反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】有A、B、C三种可溶性正盐,阴、阳离子各不相同,其阴离子的摩尔质量依次增大(按A、B、C的顺序),将等物质的量的A、B、C溶于水,所得溶液中只含有Fe3+、K+、SO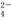 、NO
、NO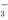 、Cl-五种离子,同时生成一种白色沉淀。
、Cl-五种离子,同时生成一种白色沉淀。
请回答下列问题:
(1)经检验,三种正盐中还含有下列选项中的一种离子,该离子是__________ 。
A.Na+B.Mg2+C.Cu2+D.Ag+
(2)三种正盐的化学式分别是:A________ ,B________ ,C________ 。
(3)若将A、B、C三种正盐按一定比例溶于水后,所得溶液中只含有Fe3+、SO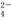 、NO
、NO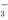 、K+四种离子且物质的量之比依次为1∶2∶3∶4,则A、B、C三种正盐的物质的量之比为
、K+四种离子且物质的量之比依次为1∶2∶3∶4,则A、B、C三种正盐的物质的量之比为______________ 。
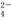 、NO
、NO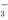 、Cl-五种离子,同时生成一种白色沉淀。
、Cl-五种离子,同时生成一种白色沉淀。请回答下列问题:
(1)经检验,三种正盐中还含有下列选项中的一种离子,该离子是
A.Na+B.Mg2+C.Cu2+D.Ag+
(2)三种正盐的化学式分别是:A
(3)若将A、B、C三种正盐按一定比例溶于水后,所得溶液中只含有Fe3+、SO
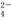 、NO
、NO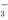 、K+四种离子且物质的量之比依次为1∶2∶3∶4,则A、B、C三种正盐的物质的量之比为
、K+四种离子且物质的量之比依次为1∶2∶3∶4,则A、B、C三种正盐的物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】某固体混合物可能由NaCl、KNO3、K2SO4、CuCl2、CaCl2、K2CO3中的一种或几种混合而成,为鉴定其组成,依次进行如下实验:
(1)取适量混合物加入足量蒸馏水,得到无色透明溶液
(2)向上述溶液中滴加足量BaCl2溶液,有白色沉淀产生
(3)过滤,取上述白色沉淀中加足量盐酸,产生无色气体,沉淀部分溶解
(4)往滤液中加AgNO3溶液,有白色沉淀产生,且白色沉淀不溶于稀硝酸
试判断:
肯定存在的物质有______ ;肯定不存在的物质有_________ ;可能存在的物质有_______ 。
(1)取适量混合物加入足量蒸馏水,得到无色透明溶液
(2)向上述溶液中滴加足量BaCl2溶液,有白色沉淀产生
(3)过滤,取上述白色沉淀中加足量盐酸,产生无色气体,沉淀部分溶解
(4)往滤液中加AgNO3溶液,有白色沉淀产生,且白色沉淀不溶于稀硝酸
试判断:
肯定存在的物质有
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】有一瓶无色澄清溶液,其中可能含有 、
、 、
、 、
、 、
、 、
、 、
、 离子。现进行以下实验:
离子。现进行以下实验:
①用pH试纸检验溶液,发现溶液呈强酸性;
②取部分溶液逐滴加入 溶液,使溶液由酸性变成碱性,无沉淀产生;
溶液,使溶液由酸性变成碱性,无沉淀产生;
③取少量②中的碱性溶液,滴加 溶液,有白色沉淀产生。
溶液,有白色沉淀产生。
(1)根据上述事实确定:该溶液中肯定存在的离子有______ ;肯定不存在的离子有______ ;可能存在的离子有______ 。
(2)写出②中发生反应的离子方程式______ 。
现有下列几种物质:① ;②
;② ;③
;③ ;④稀
;④稀 ;⑤
;⑤ ;⑥熔融
;⑥熔融 ;⑦汞;③
;⑦汞;③ ;⑨液氯;⑩氨水。请回答下列问题:
;⑨液氯;⑩氨水。请回答下列问题:
(3)以上物质属于电解质的是______ ,能导电的是______ 。(填序号)
(4)写出①与⑥的水溶液反应的离子反应方程式:______ 。
 、
、 、
、 、
、 、
、 、
、 、
、 离子。现进行以下实验:
离子。现进行以下实验:①用pH试纸检验溶液,发现溶液呈强酸性;
②取部分溶液逐滴加入
 溶液,使溶液由酸性变成碱性,无沉淀产生;
溶液,使溶液由酸性变成碱性,无沉淀产生;③取少量②中的碱性溶液,滴加
 溶液,有白色沉淀产生。
溶液,有白色沉淀产生。(1)根据上述事实确定:该溶液中肯定存在的离子有
(2)写出②中发生反应的离子方程式
现有下列几种物质:①
 ;②
;② ;③
;③ ;④稀
;④稀 ;⑤
;⑤ ;⑥熔融
;⑥熔融 ;⑦汞;③
;⑦汞;③ ;⑨液氯;⑩氨水。请回答下列问题:
;⑨液氯;⑩氨水。请回答下列问题:(3)以上物质属于电解质的是
(4)写出①与⑥的水溶液反应的离子反应方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】有一无色透明溶液,欲确定是否含有下列离子:Na+、Mg2+、Al3+、Fe2+、Ba2+、NO3-、SO42-、Cl-、I-、HCO3-,进行如下实验:
⑴溶液中肯定存在的离子是________________________ ;
⑵溶液中肯定不存在的离子是________________________ ;
⑶为进一步确定其他离子,应该补充的实验是_____________________________ ;____________________________ 。
| 实验步骤 | 实验现象 |
| ①取少量原溶液,加几滴甲基橙 | 溶液变红色 |
| ②取少量原溶液,浓缩,加Cu片和浓H2SO4,加热 | 有无色气体产生,后在空气中又变成红棕色 |
| ③取少量原溶液,加BaCl2溶液 | 有白色沉淀生成 |
| ④取③中上层清液,加AgNO3溶液 | 有白色沉淀生成,且不溶于HNO3 |
| ⑤取少量原溶液,加NaOH溶液 | 有白色沉淀生成,当NaOH过量时沉淀部分溶解 |
⑴溶液中肯定存在的离子是
⑵溶液中肯定不存在的离子是
⑶为进一步确定其他离子,应该补充的实验是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐1】以含钴废催化剂(主要成分为Co、Fe、SiO2)为原料制取复合氧化钴的流程如下:
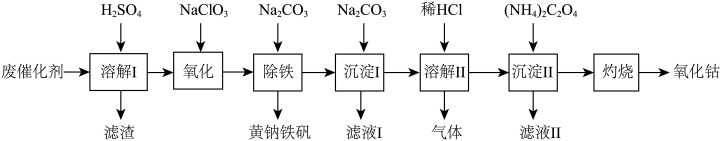
(1)用H2SO4溶解后过滤,得到的滤渣是_____________ (填化学式)。将滤渣洗涤2~3次,再将洗液与滤液合并的目的是___________ 。
(2)氧化过程中加入NaClO3反应的离子方程式是________________ 。为了确定Fe2+已经氧化完全,可选的检验试剂是__________ 。
(3)写出溶解II的离子方程式_______________ 。
(4)灼烧:准确称取沉淀II中所得纯净CoC2O4固体4.410 g,在空气中灼烧得到钴的一种氧化物2.410 g,写出该氧化物的化学式_________ 。

(1)用H2SO4溶解后过滤,得到的滤渣是
(2)氧化过程中加入NaClO3反应的离子方程式是
(3)写出溶解II的离子方程式
(4)灼烧:准确称取沉淀II中所得纯净CoC2O4固体4.410 g,在空气中灼烧得到钴的一种氧化物2.410 g,写出该氧化物的化学式
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
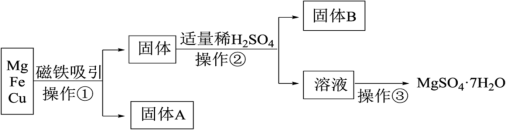
【推荐2】有Mg、Fe、Cu的混合粉末,分离得到MgSO4·7H2O过程如下:___________ 。
(2)操作②的名称是___________ ,需要用到的主要玻璃仪器有 ___________ 、玻璃棒,其中玻璃棒的作用是___________ 。
(3)操作②发生的离子反应方程式为___________ ,属于___________ 反应。(填基本反应类型)
(4)实验中可选用适量的下列试剂中的代替稀H2SO4___________ (填标号)。
A. CuSO4溶液 B.FeSO4溶液 C.稀盐酸
(5)操作③主要包含蒸发浓缩、___________ 、过滤、洗涤烘干等。
(2)操作②的名称是
(3)操作②发生的离子反应方程式为
(4)实验中可选用适量的下列试剂中的代替稀H2SO4
A. CuSO4溶液 B.FeSO4溶液 C.稀盐酸
(5)操作③主要包含蒸发浓缩、
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐3】为了除去粗盐中 、
、 、
、 以及泥沙等杂质,设计了一种制备精盐的实验方案步骤如下:(用于沉淀的试剂稍过量)
以及泥沙等杂质,设计了一种制备精盐的实验方案步骤如下:(用于沉淀的试剂稍过量)
称取粗盐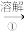
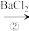
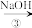
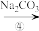
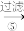 滤液
滤液
 精盐
精盐
(1)判断 过量的方法是取所得溶液的上层清液1~2滴于滴定板上,再滴入1~2滴
过量的方法是取所得溶液的上层清液1~2滴于滴定板上,再滴入1~2滴_______ ,若观察到_______ ,表明 已过量。
已过量。
(2)步骤④中,碳酸钠的作用是_______ 。
(3)经过步骤⑤,所得滤液中含有的阴离子为_______ 。
(4)若先用盐酸调pH再过滤,会对实验结果有影响吗?_______ (填“有”或“无”),试分析原因:_______ 。
 、
、 、
、 以及泥沙等杂质,设计了一种制备精盐的实验方案步骤如下:(用于沉淀的试剂稍过量)
以及泥沙等杂质,设计了一种制备精盐的实验方案步骤如下:(用于沉淀的试剂稍过量)称取粗盐
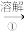
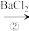
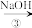
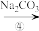
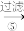 滤液
滤液
 精盐
精盐(1)判断
 过量的方法是取所得溶液的上层清液1~2滴于滴定板上,再滴入1~2滴
过量的方法是取所得溶液的上层清液1~2滴于滴定板上,再滴入1~2滴 已过量。
已过量。(2)步骤④中,碳酸钠的作用是
(3)经过步骤⑤,所得滤液中含有的阴离子为
(4)若先用盐酸调pH再过滤,会对实验结果有影响吗?
您最近一年使用:0次



