题型:解答题-结构与性质
难度:0.85
引用次数:176
题号:11429674
卤族元素能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解。
(1)下面曲线(图1)表示卤族元素某种性质随核电荷数的变化趋势。正确的是___ 。
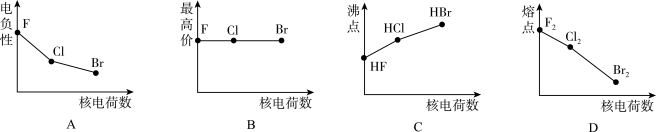
(2)溴化碘(IBr)的化学性质类似于卤素单质,溴化碘和水反应所得产物中有一种为三原子分子,该分子的电子式为___ 。
(3)F2与其他卤素单质反应可以生成ClF3、BrF3等。已知反应Cl2(g)+3F2(g)=2C1F3(g)△H=−313kJ/mol;F−F键的键能为159kJ/mol;Cl−C1键的键能为242kJ/mol;则ClF3中C1−F键的平均键能为___ kJ/mol。ClF3的熔、沸点比BrF3的___ (填“高”或“低”)。
(4)根据第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是___ 。
(5)(CN)2与Cl2的化学性质相似,(CN)2与NaOH溶液反应的化学方程式为___ 。
(6)上述反应涉及到的元素中,氯原子核外电子能量最高能级符号是___ ;H、Cl、N、O、Na的电负性从小到大的顺序为___ 。
(7)氯有多种含氧酸,其酸性:HClO4>HClO3>HClO2>HClO,从物质结构的角度解释以上含氧酸酸性依次减小的原因___ 。
(1)下面曲线(图1)表示卤族元素某种性质随核电荷数的变化趋势。正确的是

(2)溴化碘(IBr)的化学性质类似于卤素单质,溴化碘和水反应所得产物中有一种为三原子分子,该分子的电子式为
(3)F2与其他卤素单质反应可以生成ClF3、BrF3等。已知反应Cl2(g)+3F2(g)=2C1F3(g)△H=−313kJ/mol;F−F键的键能为159kJ/mol;Cl−C1键的键能为242kJ/mol;则ClF3中C1−F键的平均键能为
(4)根据第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是
| 氟 | 氯 | 溴 | 碘 | |
| 第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 |
(5)(CN)2与Cl2的化学性质相似,(CN)2与NaOH溶液反应的化学方程式为
(6)上述反应涉及到的元素中,氯原子核外电子能量最高能级符号是
(7)氯有多种含氧酸,其酸性:HClO4>HClO3>HClO2>HClO,从物质结构的角度解释以上含氧酸酸性依次减小的原因
更新时间:2020/10/23 14:27:28
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
【推荐1】硝酸铵的化学式为 ,是白色结晶性粉末,极易溶于水。硝酸铵在现代农业、工业和国防中都占有重要地位。工业生产硝酸铵的简要流程如图。
,是白色结晶性粉末,极易溶于水。硝酸铵在现代农业、工业和国防中都占有重要地位。工业生产硝酸铵的简要流程如图。
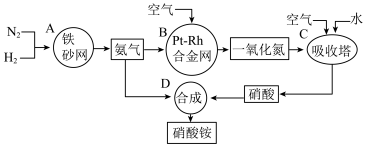
(1) 的结构式为
的结构式为_______ ; 中氮元素的化合价依次为
中氮元素的化合价依次为_______ 、_______ 。
(2)B装置中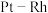 合金网的作用是
合金网的作用是_______ ,其中发生反应的化学方程式为_______
(3)C、D两个装置中发生的反应,属于氧化还原反应的是_______ (填标号),其中氧化剂为_______ (填化学式)。
(4)常温下,铝在浓硝酸中会发生钝化,其本质是发生氧化还原反应,使铝的表面形成一层致密的氧化膜,同时生成二氧化氮,其反应的离子方程式为_______ 。
 ,是白色结晶性粉末,极易溶于水。硝酸铵在现代农业、工业和国防中都占有重要地位。工业生产硝酸铵的简要流程如图。
,是白色结晶性粉末,极易溶于水。硝酸铵在现代农业、工业和国防中都占有重要地位。工业生产硝酸铵的简要流程如图。
(1)
 的结构式为
的结构式为 中氮元素的化合价依次为
中氮元素的化合价依次为(2)B装置中
 合金网的作用是
合金网的作用是(3)C、D两个装置中发生的反应,属于氧化还原反应的是
(4)常温下,铝在浓硝酸中会发生钝化,其本质是发生氧化还原反应,使铝的表面形成一层致密的氧化膜,同时生成二氧化氮,其反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】X、Y、Z、W代表原子序数依次增大的四种短周期元素,X原子核内没有中子,在周期表中,Z与Y﹑W均相邻,Y﹑Z和W三种元素的原子最外层电子数之和为17,且Z﹑W最外层电子数相同。
(1)用电子式表示X与Y所组成化合物的形成过程_________________ 。
(2)W在周期表中的位置是____________________ 。
(3)已知,在101kPa时,X单质在1.00molO2中完全燃烧生成2.00mol液态H2O,放出571.6kJ的热量,则表示X单质燃烧热的热化学方程式为__________ 。
(1)用电子式表示X与Y所组成化合物的形成过程
(2)W在周期表中的位置是
(3)已知,在101kPa时,X单质在1.00molO2中完全燃烧生成2.00mol液态H2O,放出571.6kJ的热量,则表示X单质燃烧热的热化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】根据①~⑩元素的编号所在周期表中的位置,用化学用语回答有关问题:
(1)最易失电子形成阳离子元素是_______ (填元素符号),元素⑧的最高价氧化物的水化物的化学式为_______ ;
(2)①、⑦、⑨能形成原子个数为1:1:1的化合物,其结构式为_______ ;①与⑦可组成原子个数比为1:1的化合物甲,将⑨的单质通入甲的水溶液中,生成一种强酸且有气体放出,该反应的化学方程式为_______ ;
(3)⑨与⑩的单质加热条件下可发生反应,产物的电子式为_______ ;
(4)元素④与铝性质相似,其最高价氧化物的水化物能与⑩的氢氧化物反应,离子方程式为:_______ 。
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | ② | ||||||
| 2 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||
| 3 | ⑧ | ⑨ | ||||||
| 4 | ⑩ |
(2)①、⑦、⑨能形成原子个数为1:1:1的化合物,其结构式为
(3)⑨与⑩的单质加热条件下可发生反应,产物的电子式为
(4)元素④与铝性质相似,其最高价氧化物的水化物能与⑩的氢氧化物反应,离子方程式为:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】已知A、B、C、D是原子序数依次增大的四种短周期主族元素,A的周期数等于其主族序数,B原子的价电子排布为nsnnpn,D是地壳中含量最多的元素.E是第四周期的p区元素且最外层只有2对成对电子,F元素的基态原子第四能层只有一个电子,其它能层均已充满电子.
(1)基态E原子的价电子排布图_____ 。
(2)B、C、D三元素电负性由大到小的顺序为________ (用元素符号表示)。
(3)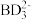 中心原子为
中心原子为_______ 杂化,空间构型为_________ ;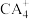 中心原子为
中心原子为_______ 杂化,空间构型为___________ 。
(4)1molBC-中含有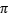 键的数目为
键的数目为________ NA。
(5)D、E元素最简单氢化物的稳定性________________ (填化学式)。
(1)基态E原子的价电子排布图
(2)B、C、D三元素电负性由大到小的顺序为
(3)
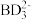 中心原子为
中心原子为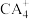 中心原子为
中心原子为(4)1molBC-中含有
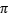 键的数目为
键的数目为(5)D、E元素最简单氢化物的稳定性
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】尿素[ ]是一种重要的工业原料,在160℃下分解生成异氰酸和氨气,化学方程式为
]是一种重要的工业原料,在160℃下分解生成异氰酸和氨气,化学方程式为 。回答下列问题:
。回答下列问题:
(1)上述反应所涉及的各元素中,原子半径最大的是___________ (填元素符号),其原子核外电子共占据___________ 个原子轨道。
(2)上述元素中有三种元素处于同周期,则:
①最高价氧化物对应水化物的酸性最强的是___________ (填化学式)。
②元素的第一电离能由大到小的顺序是___________ (填元素符号,下同)。
③元素的电负性由大到小的顺序是___________ 。
(3)氰酸有两种结构,一种分子内含有三键,称为氰酸,另一种分子内不含三键,称为异氰酸,且两种结构中所有原子最外层均已达到稳定结构,分子中也不含环状结构。写出氰酸和异氰酸的结构式:___________ 、___________ 。
 ]是一种重要的工业原料,在160℃下分解生成异氰酸和氨气,化学方程式为
]是一种重要的工业原料,在160℃下分解生成异氰酸和氨气,化学方程式为 。回答下列问题:
。回答下列问题:(1)上述反应所涉及的各元素中,原子半径最大的是
(2)上述元素中有三种元素处于同周期,则:
①最高价氧化物对应水化物的酸性最强的是
②元素的第一电离能由大到小的顺序是
③元素的电负性由大到小的顺序是
(3)氰酸有两种结构,一种分子内含有三键,称为氰酸,另一种分子内不含三键,称为异氰酸,且两种结构中所有原子最外层均已达到稳定结构,分子中也不含环状结构。写出氰酸和异氰酸的结构式:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐3】氨硼烷(NH3BH3)含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
(1)H、B、N中,原子半径最大的是_______ 。根据对角线规则,B的一些化学性质与元素_______ 的相似。
(2)NH3BH3分子中,N—B化学键称为_______ 键,其电子对由_______ 提供。氨硼烷在催化剂作用下水解释放氢气:3NH3BH3+6H2O=3NH +B3O
+B3O +9H2。B3O
+9H2。B3O 的结构为
的结构为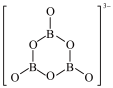 。在该反应中,B原子的杂化轨道类型由
。在该反应中,B原子的杂化轨道类型由_______ 变为_______ 。
(3)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),电负性大小顺序是_______ 。
(4)研究发现,氨硼烷在低温高压条件下为正交晶系结构,晶胞参数分别为a pm、b pm、c pm,α=β=γ=90°。氨硼烷的2×2×2超晶胞结构如图所示。
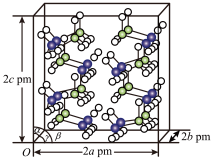
氨硼烷晶体的密度ρ=_______ g·cm-3(列出计算式,设NA为阿伏加德罗常数的值)。
(1)H、B、N中,原子半径最大的是
(2)NH3BH3分子中,N—B化学键称为
 +B3O
+B3O +9H2。B3O
+9H2。B3O 的结构为
的结构为 。在该反应中,B原子的杂化轨道类型由
。在该反应中,B原子的杂化轨道类型由(3)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),电负性大小顺序是
(4)研究发现,氨硼烷在低温高压条件下为正交晶系结构,晶胞参数分别为a pm、b pm、c pm,α=β=γ=90°。氨硼烷的2×2×2超晶胞结构如图所示。

氨硼烷晶体的密度ρ=
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐1】判断
(1)氢键是氢元素与其他元素形成的化学键_____ 。
(2)可燃冰(CH4·8H2O)中甲烷分子与水分子间形成了氢键_____ 。
(3)乙醇分子和水分子间只存在范德华力_____ 。
(4)碘化氢的沸点高于氯化氢的沸点是因为碘化氢分子间存在氢键_____ 。
(5)水分子间既存在范德华力,又存在氢键_____ 。
(6)H2和O2之间存在氢键_____ 。
(7)氢键的存在一定能使物质的熔、沸点升高_____ 。
(1)氢键是氢元素与其他元素形成的化学键
(2)可燃冰(CH4·8H2O)中甲烷分子与水分子间形成了氢键
(3)乙醇分子和水分子间只存在范德华力
(4)碘化氢的沸点高于氯化氢的沸点是因为碘化氢分子间存在氢键
(5)水分子间既存在范德华力,又存在氢键
(6)H2和O2之间存在氢键
(7)氢键的存在一定能使物质的熔、沸点升高
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
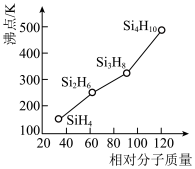
【推荐2】(1)硅烷( )的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是
)的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是______ 。
(2)① 分子内的
分子内的 键、分子间的范德华力和氢键从强到弱依次为
键、分子间的范德华力和氢键从强到弱依次为______ 。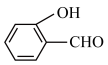 的沸点比
的沸点比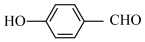 的沸点低,原因是
的沸点低,原因是______ 。
②乙二胺( )和三甲胺
)和三甲胺 均属于胺,但乙二胺比三甲胺的沸点高得多,原因是
均属于胺,但乙二胺比三甲胺的沸点高得多,原因是______ 。
③ 与
与 可以任意比例互溶,除因它们是极性分子外,还因为
可以任意比例互溶,除因它们是极性分子外,还因为______ , 在乙醇中的溶解度大于
在乙醇中的溶解度大于 在乙醇中的溶解度,其原因是
在乙醇中的溶解度,其原因是______ 。
(3)关于化合物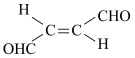 ,下列叙述正确的有
,下列叙述正确的有______ (填标号)。
a.分子间可形成氢键
b.分子中既有极性键又有非极性键
c.分子中含有7个 键和1个π键
键和1个π键
d.该分子在水中的溶解度大于
 )的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是
)的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是
(2)①
 分子内的
分子内的 键、分子间的范德华力和氢键从强到弱依次为
键、分子间的范德华力和氢键从强到弱依次为 的沸点比
的沸点比 的沸点低,原因是
的沸点低,原因是②乙二胺(
 )和三甲胺
)和三甲胺 均属于胺,但乙二胺比三甲胺的沸点高得多,原因是
均属于胺,但乙二胺比三甲胺的沸点高得多,原因是③
 与
与 可以任意比例互溶,除因它们是极性分子外,还因为
可以任意比例互溶,除因它们是极性分子外,还因为 在乙醇中的溶解度大于
在乙醇中的溶解度大于 在乙醇中的溶解度,其原因是
在乙醇中的溶解度,其原因是(3)关于化合物
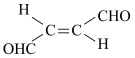 ,下列叙述正确的有
,下列叙述正确的有a.分子间可形成氢键
b.分子中既有极性键又有非极性键
c.分子中含有7个
 键和1个π键
键和1个π键d.该分子在水中的溶解度大于

您最近一年使用:0次



