向100mL稀硫酸和硝酸铁的混合溶液中加入铁粉,溶液中的Fe2+浓度如图所示(不考虑溶液体积的变化):
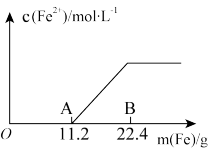
(1)OA段反应的离子方程式为___ ;AB段反应的离子方程式为__ ;由此推出混合液中存在微粒氧化性由大到小的关系是___ 。
(2)原溶液中H2SO4与Fe(NO3)3的物质的量之比为___
(3)B点对应溶液中Fe2+物质的量浓度为__ mol∙L-1; 的物质的量浓度为
的物质的量浓度为__ mol·L-1。

(1)OA段反应的离子方程式为
(2)原溶液中H2SO4与Fe(NO3)3的物质的量之比为
(3)B点对应溶液中Fe2+物质的量浓度为
 的物质的量浓度为
的物质的量浓度为
更新时间:2020-10-24 19:45:13
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)向Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色是由于生成了___ (写离子符号),此过程的离子方程式是___ 。又变为棕黄色原因是(用离子方程式解释)___ 。
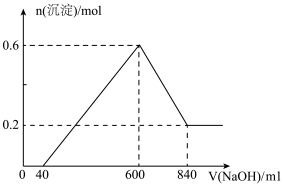
(2)为测定某一混合铵盐的成分(只含NH4HSO4和(NH4)2SO4),若将不同质量的样品分别加入到50mL浓度相同的NaOH溶液中,沸水浴加热至气体全部逸出(此温度下该铵盐不会分解)。气体充分干燥后再用浓硫酸吸收完全,测定浓硫酸增加的质量如表所示:
①样品与NaOH溶液反应产生气体时的离子方程式为___ 。
②NH4HSO4和(NH4)2SO4的物质的量之比___ 。
③第三次实验时浓硫酸增加的质量a的值为___ 。
(2)为测定某一混合铵盐的成分(只含NH4HSO4和(NH4)2SO4),若将不同质量的样品分别加入到50mL浓度相同的NaOH溶液中,沸水浴加热至气体全部逸出(此温度下该铵盐不会分解)。气体充分干燥后再用浓硫酸吸收完全,测定浓硫酸增加的质量如表所示:
| 实验次数 | 1 | 2 | 3 | 4 |
| 铵盐质量/g | 18.10 | 36.20 | 54.30 | 72.40 |
| 浓硫酸增重/g | 3.4 | 3.4 | a | 0 |
①样品与NaOH溶液反应产生气体时的离子方程式为
②NH4HSO4和(NH4)2SO4的物质的量之比
③第三次实验时浓硫酸增加的质量a的值为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】完成下列问题。
(1)下表给出了1mol化学键断开所需要吸收的能量(的平均值),请计算17.6g乙酸乙酯燃烧完全燃烧放出的热量___________ 。
(2)某兴趣小组探究H2和Cl2反应后的气体与氢氧化钠溶液反应。在标准状况下,H2和Cl2的混合气体共2.24L,光照充分反应后,用NaOH溶液充分吸收。
①消耗NaOH物质的量的最大值为_____________________ 。
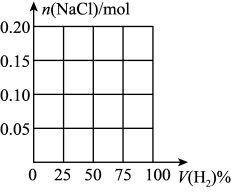
②请在图中画出充分反应后NaCl的物质的量随原混合气体中H2的体积分数的变化图象________ 。
(1)下表给出了1mol化学键断开所需要吸收的能量(的平均值),请计算17.6g乙酸乙酯燃烧完全燃烧放出的热量
| 化学键 | C-H | C-C | C-O | C=O | O=O | O-H |
| 能量(kJ) | a | b | c | d | e | f |
①消耗NaOH物质的量的最大值为
②请在图中画出充分反应后NaCl的物质的量随原混合气体中H2的体积分数的变化图象

您最近一年使用:0次
【推荐1】(1)9.5g MgCl2溶于水配成100mL溶液,所得溶液的物质的量浓度为_______ ,取溶液25.0mL,稀释到500mL,此时溶液中Cl-的物质的量浓度为_______ ,在这两个实验中除了用烧杯、量筒、胶头滴管外,还需用到的玻璃仪器是_______ 。
(2)在反应3Cl2 + 6KOH(浓) =5KCl + KClO3 + 3H2O中,氧化产物与还原产物的物质的量之比为_______ ,3molCl2参加该反应时,反应中转移_______ mol电子。
(3)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO +4H++3e- = NO↑+2H2O。KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
+4H++3e- = NO↑+2H2O。KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
①写出该氧化还原反应的化学方程式(不需要配平):_______ 。
②反应中硝酸体现了_______ 的性质。
(2)在反应3Cl2 + 6KOH(浓) =5KCl + KClO3 + 3H2O中,氧化产物与还原产物的物质的量之比为
(3)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO
 +4H++3e- = NO↑+2H2O。KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
+4H++3e- = NO↑+2H2O。KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。①写出该氧化还原反应的化学方程式(不需要配平):
②反应中硝酸体现了
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】常温下,取2.86gNa2CO3·10H2O溶于水配成100mL溶液,求:
①该溶液中Na2CO3的物质的量浓度为_______ 。
②该溶液中Na+的物质的量为_____ 。
③取出20.0mL该溶液用蒸馏水稀释,使Na2CO3溶液物质的量浓度变为0.04mol/L,则稀释后溶液的体积是______ 。
①该溶液中Na2CO3的物质的量浓度为
②该溶液中Na+的物质的量为
③取出20.0mL该溶液用蒸馏水稀释,使Na2CO3溶液物质的量浓度变为0.04mol/L,则稀释后溶液的体积是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】向一定量的Fe、FeO、Fe2O3的混合物中,加入100 mLl.0 mol·L-1的盐酸,恰好使混合物完全溶解并放出约224 mL(标准状况)气体,假设溶液体积不变,所得溶液中加入KSCN溶液无血红色出现。请回答下列问题:
(1)生成气体的物质的量为___ mol。
(2)所得溶液中溶质为___ (填化学式),物质的量浓度为___ mol·L-1。
(3)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量为___ g。
(4)原混合物的总质量为___ g。
(1)生成气体的物质的量为
(2)所得溶液中溶质为
(3)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量为
(4)原混合物的总质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】有一无色透明溶液,欲确定是否含有下列离子:Na+、Mg2+、Ba2+、 、
、 、Cl-、
、Cl-、 ,实验如下:
,实验如下:
由此判断:
(1)溶液中肯定存在的离子是________________________,肯定不存在的离子是________________,可能存在的离子是________________。
(2)实验②中生成无色气体的离子方程式是________________________________。
(3)为进一步确定可能存在的阴离子,应该补充的实验设计是__________________。
 、
、 、Cl-、
、Cl-、 ,实验如下:
,实验如下:| 实验步骤 | 实验现象 |
| ①取少量原溶液,加入几滴酚酞试液 | 溶液变成红色 |
| ②取少量原溶液加热浓缩,加入Cu片和一定浓度的H2SO4 | 有无色气体产生,该气体遇空气变成红棕色 |
| ③取少量原溶液,加入BaCl2溶液 | 有白色沉淀生成 |
| ④取③中上层清液,先加入稀硝酸,再加入AgNO3溶液 | 有白色沉淀生成 |
(1)溶液中肯定存在的离子是________________________,肯定不存在的离子是________________,可能存在的离子是________________。
(2)实验②中生成无色气体的离子方程式是________________________________。
(3)为进一步确定可能存在的阴离子,应该补充的实验设计是__________________。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知a、b、c、d、e分别是Ca(OH)2、Ca(HCO3)2、HCl、Ba(NO3)2、Na2CO3五种物质水溶液中的各一种。它们互相反应的情况如下表所示:
“↓”表示生成沉淀;“↑”表示产生气体;“-”表示无明显现象;“/”表示实验未做。
由上表可推知:c是___________ ,e是___________ (均填化学式)。
| a | b | c | d | e | |
| c | ↓ | ↓ | / | ↑ | - |
| b | ↓ | / | ↓ | - | - |
由上表可推知:c是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】实验室中有失去标签的五瓶溶液甲、乙、丙、丁、戊,只知它们分别是 溶液、
溶液、 溶液、
溶液、 溶液、
溶液、 溶液、
溶液、 溶液中的一种,为鉴别这些物质,进行如下实验:
溶液中的一种,为鉴别这些物质,进行如下实验:
回答下列问题:
(1)不用其他物质,丁可直接鉴别出,丁为___________ ,鉴别出的依据是___________ ,该物质也可采用焰色试验鉴别出,操作方法及现象是___________ 。
(2)写出戊中溶质在水溶液中的电离方程式:___________ 。
(3)从实验ii后的混合体系中获取溶液中溶质的操作方法是___________ (填操作名称)。
(4)实验iii中乙和戊恰好完全反应后的溶液中的溶质是___________ (填化学式)。
(5)写出实验v中反应的离子方程式:___________ 。
 溶液、
溶液、 溶液、
溶液、 溶液、
溶液、 溶液、
溶液、 溶液中的一种,为鉴别这些物质,进行如下实验:
溶液中的一种,为鉴别这些物质,进行如下实验:| 实验编号 | 实验方法及现象 |
| 实验i | 甲+戊→溶液+气体 |
| 实验ii | 乙+丙→溶液+沉淀 |
| 实验iii | 乙+戊→溶液+沉淀 |
| 实验iv | 甲+乙→溶液+沉淀 |
| 实验v | 将iv得到的沉淀加入iii所得的溶液中,沉淀很快溶解,生成无色无味的气体 |
回答下列问题:
(1)不用其他物质,丁可直接鉴别出,丁为
(2)写出戊中溶质在水溶液中的电离方程式:
(3)从实验ii后的混合体系中获取溶液中溶质的操作方法是
(4)实验iii中乙和戊恰好完全反应后的溶液中的溶质是
(5)写出实验v中反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.写出下列反应的离子方程式:
(1)磁性氧化铁溶于稀盐酸:___________ 。
(2)用硫氰酸钾溶液检验待测液中的
___________ 。
(3)用酸性高锰酸钾溶液检验待测液中的
___________ 。
Ⅱ.根据信息配平下列反应的离子方程式
(4)将 固体(黄色,微溶)加入
固体(黄色,微溶)加入 和
和 的混合溶液里,加热,溶液显紫色(
的混合溶液里,加热,溶液显紫色( 无色)。请根据题中信息配平该反应的离子方程式:
无色)。请根据题中信息配平该反应的离子方程式:___________
___________ ___________
___________ ___________=___________
___________=___________ ___________
___________ ___________
___________ ___________
___________
(5) 虽然具有净水作用,但是腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比
虽然具有净水作用,但是腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比 高效,且腐蚀性小。完成
高效,且腐蚀性小。完成 氧化
氧化 的离子方程式:
的离子方程式:___________
___________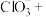 ___________
___________ ___________=___________
___________=___________ ___________
___________ ___________
___________
(1)磁性氧化铁溶于稀盐酸:
(2)用硫氰酸钾溶液检验待测液中的

(3)用酸性高锰酸钾溶液检验待测液中的

Ⅱ.根据信息配平下列反应的离子方程式
(4)将
 固体(黄色,微溶)加入
固体(黄色,微溶)加入 和
和 的混合溶液里,加热,溶液显紫色(
的混合溶液里,加热,溶液显紫色( 无色)。请根据题中信息配平该反应的离子方程式:
无色)。请根据题中信息配平该反应的离子方程式:___________
 ___________
___________ ___________=___________
___________=___________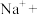 ___________
___________ ___________
___________ ___________
___________(5)
 虽然具有净水作用,但是腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比
虽然具有净水作用,但是腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比 高效,且腐蚀性小。完成
高效,且腐蚀性小。完成 氧化
氧化 的离子方程式:
的离子方程式:___________
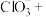 ___________
___________ ___________=___________
___________=___________ ___________
___________ ___________
___________
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】完成下列各题。
(1)按如图所示操作,充分反应后:
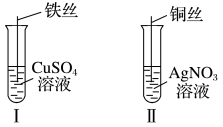
①Ⅰ中发生反应的离子方程式为_____ 。
②Ⅱ中铜丝上观察到现象是_____ 。
③结合Ⅰ、Ⅱ实验现象可知 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为_____ 。
(2)人体内的铁元素以 和
和 的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含
的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含 的亚铁盐,如硫酸亚铁。服用维生素
的亚铁盐,如硫酸亚铁。服用维生素 ,可使食物中的
,可使食物中的 还原成
还原成 ,有利于人体吸收。这句话说明维生素
,有利于人体吸收。这句话说明维生素 在这一反应中起的作用是
在这一反应中起的作用是_____ 。
(3)实验室可以用铜和稀硝酸反应制取 ,反应的化学方程式如下(未配平):
,反应的化学方程式如下(未配平):
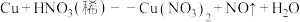
①写出配平后的上述化学方程式:_____ 。
②该反应中,被还原的硝酸与未被还原的硝酸质量比为_____ 。
(1)按如图所示操作,充分反应后:

①Ⅰ中发生反应的离子方程式为
②Ⅱ中铜丝上观察到现象是
③结合Ⅰ、Ⅱ实验现象可知
 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为(2)人体内的铁元素以
 和
和 的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含
的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含 的亚铁盐,如硫酸亚铁。服用维生素
的亚铁盐,如硫酸亚铁。服用维生素 ,可使食物中的
,可使食物中的 还原成
还原成 ,有利于人体吸收。这句话说明维生素
,有利于人体吸收。这句话说明维生素 在这一反应中起的作用是
在这一反应中起的作用是(3)实验室可以用铜和稀硝酸反应制取
 ,反应的化学方程式如下(未配平):
,反应的化学方程式如下(未配平):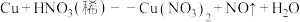
①写出配平后的上述化学方程式:
②该反应中,被还原的硝酸与未被还原的硝酸质量比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】我国古代就已经开始研究金属,《抱朴子内篇》记载:“曾青涂铁,铁赤色如铜” 描述了古代炼铜的原理。现对其中的原理作出进一步研究。
【实验探究】
【实验结论】铁可以置换出铜,铜不可以置换出铁。
(1)写出步骤一对应的实验现象___________ 。
(2)写出步骤一发生反应的离子方程式,并用单线桥标出电子转移___________ 。
(3)金属活动性顺序表反应了金属性质的递变规律,根据金属活动性顺序表判断,下列金属还原性最强的是___________ (填标号),其对应的金属离子氧化性最强的是___________ (填标号)。
A.Ag B.K C.Mg D.Cu
(4)经实验测得 Hg2+的氧化性与 Fe3+的氧化性近似相同,请你预测Fe与Fe3+___________ (填“能”或“不能”)发生氧化还原反应,如果能,请分别写出该反应的氧化产物和还原产物的离子符号:氧化产物___________ ,还原产物 ___________ ;如果不能,请说明理由_________ 。
(5)向含有 AgNO3和Cu(NO3)2的溶液中同时加入 ag 铁粉和镁粉的混合物,充分反应后过滤,得到滤渣 M 和滤液N。向滤液N中滴入NaCl溶液,有白色沉淀产生。则下列判断中,错误的是_______ (填标号)
【实验探究】
| 实验操作 | 实验现象 |
| 步骤一:向 CuSO4溶液中加入足量的铁片 | |
| 步骤二:向 FeSO4溶液中加入足量的铜片 | 实验无明显现象 |
(1)写出步骤一对应的实验现象
(2)写出步骤一发生反应的离子方程式,并用单线桥标出电子转移
(3)金属活动性顺序表反应了金属性质的递变规律,根据金属活动性顺序表判断,下列金属还原性最强的是
A.Ag B.K C.Mg D.Cu
(4)经实验测得 Hg2+的氧化性与 Fe3+的氧化性近似相同,请你预测Fe与Fe3+
(5)向含有 AgNO3和Cu(NO3)2的溶液中同时加入 ag 铁粉和镁粉的混合物,充分反应后过滤,得到滤渣 M 和滤液N。向滤液N中滴入NaCl溶液,有白色沉淀产生。则下列判断中,错误的是_______ (填标号)
A.滤液 N 中一定含有 和 Cu2+ 和 Cu2+ | B.滤渣 M 的质量一定小于ag |
| C.滤液 N 中一定含有Fe2+和Mg2+ | D.滤渣 M 中一定是混合物 |
您最近一年使用:0次