下列对一些实验事实和理论解释正确的是
选项 | 实验事实 | 理论解释 |
A | 稀硫酸能导电 | H2SO4为离子化合物 |
B | HBr的酸性强于HI的酸性 | Br的非金属性比I强 |
C | HF的沸点高于HCl | F的非金属性比Cl强 |
D | K3C60在熔融状态下能够导电 | K3C60中含有离子键 |
| A.A | B.B | C.C | D.D |
更新时间:2020/10/28 22:34:54
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】用如图装置(搅拌装置略)探究溶液离子浓度变化,灯光变化不可能 出现“亮→暗(或灭)→亮”现象的是
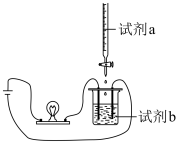

| 选项 | A | B | C | D |
| 试剂a |  |  |  |  |
| 试剂b |  | 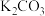 |  |  |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
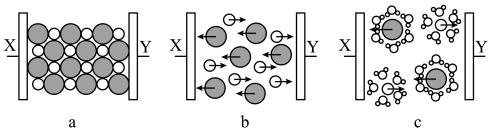
【推荐2】图a、b、c分别为氯化钠在不同状态下的导电实验的微观示意图(X、Y均表示石墨电极,且与直流电源连接方式相同, 表示水分子),下列说法正确的是
表示水分子),下列说法正确的是
 表示水分子),下列说法正确的是
表示水分子),下列说法正确的是
A.“ ”代表 ”代表 ,“ ,“ ”代表 ”代表 |
| B.X是电源的负极 |
| C.NaCl在三种状态下都存在自由移动的离子 |
| D.图c表示NaCl在水溶液中的导电情况 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】科学家发现对LiTFSI(一种亲水有机盐)进行掺杂和改进,能显著提高锂离子电池传输电荷的能力。LiTFSI的结构如图所示,A、B、C、D为同一周期的短周期元素,E与C同族,E的原子序数是B和D的原子序数之和。下列说法正确的是
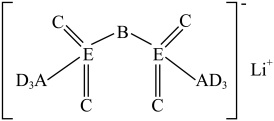
| A.元素A、D形成的分子中一定不含非极性键 |
| B.元素的第一电离能:D>B>C>A |
| C.元素的电负性:D>E>C |
| D.简单氢化物的稳定性:E>D |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列事实不能 用氢键解释的是
A.密度: | B.沸点: |
C.稳定性: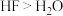 | D.溶解性(水中):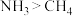 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下表为元素周期表前4周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是


| A.X、Z元素都能形成双原子分子 |
| B.W、R元素单质分子内都存在非极性键 |
C. 中心原子价层电子对数为3 中心原子价层电子对数为3 |
D.键能 ,键的极性 ,键的极性 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D为前20号元素,分别处于不同周期,其中A、B同主族,其原子序数之和等于C、D的原子序数之和。C的单质可分别与B、D的最高价氧化物的水化物发生反应,生成的两种盐溶液混合后可得到一种白色胶状沉淀。下列说法不正确的是
A.简单离子的半径 | B.氧化物的熔点: |
C.化合物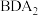 中含有离子键和共价键 中含有离子键和共价键 | D.化合物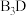 与水反应可生成两种碱 与水反应可生成两种碱 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】次磷酸(H3PO2)为一元弱酸,是一种精细磷化工产品,其制备过程的第一步反应为:2P4+3Ba(OH)2+6H2O=3Ba(H2PO2)2+2PH3↑。则下列叙述不正确 的是
| A.若反应消耗白磷3.1g,反应断开了0.15molP-P键 |
| B.当生成标况下4.48LPH3转移了0.6NA电子 |
C.0.1mol/L的Ba(H2PO2)2溶液中:c(H3PO2)+c(H2PO )+c(HPO )+c(HPO )+c(PO )+c(PO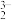 )=0.2mol/L )=0.2mol/L |
| D.标况下,1molH2O中含有的中子数为8NA |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】关于氢键,下列说法正确的是
| A.每一个水分子内含有两个氢键 |
| B.冰、水中都存在氢键 |
| C.分子间形成的氢键使物质的熔点和沸点降低 |
| D.H2O是一种非常稳定的化合物,这是由于氢键所致 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法不正确的是
| A.氯化铵固体受热分解破坏了离子键 |
| B.由于H-O键比H-S键牢固,所以水的熔沸点比H2S高 |
| C.F2、Cl2、Br2、I2熔沸点逐渐升高,是因为它们的组成结构相似,分子间的范德华力增大 |
| D.金属元素的最高价氧化物对应水化物的碱性越强,金属性就越强 |
您最近半年使用:0次



