(1)将40gNaOH溶于水,配成250mL溶液甲,甲的浓度为______ mol/L;将50mL甲加水稀释至100mL后,得溶液乙,乙的浓度为_____ mol/L。
(2)若18.6gNa2X中含有0.6mol钠离子,Na2X的摩尔质量是__ ,X的相对原子质量是___ 。
(2)若18.6gNa2X中含有0.6mol钠离子,Na2X的摩尔质量是
更新时间:2020-11-02 16:19:38
|
相似题推荐
计算题
|
较易
(0.85)
解题方法
【推荐1】已知一个12C原子的质量为1.993×10-23 g。填表:(保留三位小数)
| 35Cl | 37Cl | |
| 原子质量(×10-23 g) | 5.807 | 6.139 |
| 相对原子质量 | ① | ② |
| 原子百分率(丰度) | 74.82% | 25.18% |
| 元素的相对原子质量 | ③ | |
您最近半年使用:0次
计算题
|
较易
(0.85)
名校
解题方法
【推荐2】北京奥运会主体育场的外形好似“鸟巢”,有一类物质的结构也好似“鸟巢”,如化学式为B5H9的五硼烷。计算:五硼烷的摩尔质量是________ ,96 g五硼烷的物质的量是________ 。
您最近半年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐1】取某镀锌铁片56.9 g, 将其投入足量稀硫酸中,镀锌铁片完全溶解,产生氢气22.4 L (标准状况)。试计算:
(1)产生氢气的物质的量___________ mol。
(2)镀锌铁片中铁的质量是___________ g。
(1)产生氢气的物质的量
(2)镀锌铁片中铁的质量是
您最近半年使用:0次
计算题
|
较易
(0.85)
名校
【推荐2】回答下列问题:
(1)现有下列10种物质:①铝,②纯醋酸,③CO2,④苏打,⑤Ba(OH)2,⑥氢氧化铁胶体,⑦稀盐酸,⑧NaHSO4固体,⑨碳酸钙,⑩氨水。
①上述物质中属于盐的是____ ,属于电解质的有____ 。(填序号)
②简述实验室制备⑥的方法_____ 。
③写出⑧在水中的电离方程式为____ 。
④将⑨和⑦混合,反应的离子方程式为____ 。
(2)完成下列有关物质的量的相关计算:
①3.4gNH3与标准状况下的____ L的H2S含有相同数目的氢原子。
②40.5g某金属氯化物MCl2中含有0.6molCl-,则该金属氯化物的摩尔质量为____ 。
③实验室配制100mL0.2mol•L-1的Na2CO3溶液,通过计算得出可用天平称取Na2CO3固体____ g。若用4mol•L-1的Na2CO3浓溶液配制100mL0.2mol•L-1的稀溶液,应用量筒量取____ mL该浓溶液。
(1)现有下列10种物质:①铝,②纯醋酸,③CO2,④苏打,⑤Ba(OH)2,⑥氢氧化铁胶体,⑦稀盐酸,⑧NaHSO4固体,⑨碳酸钙,⑩氨水。
①上述物质中属于盐的是
②简述实验室制备⑥的方法
③写出⑧在水中的电离方程式为
④将⑨和⑦混合,反应的离子方程式为
(2)完成下列有关物质的量的相关计算:
①3.4gNH3与标准状况下的
②40.5g某金属氯化物MCl2中含有0.6molCl-,则该金属氯化物的摩尔质量为
③实验室配制100mL0.2mol•L-1的Na2CO3溶液,通过计算得出可用天平称取Na2CO3固体
您最近半年使用:0次
计算题
|
较易
(0.85)
名校
解题方法
【推荐1】在标准状况下4.48LH2与0.3molCl2混合见光反应后,再全部通入100mLNaOH溶液中,恰好完全反应,无剩余气体逸出。则:
①氢气与氯气混合反应后气体的总体积为__________ L。
②原氢氧化钠溶液浓度为_____ mol/L。
①氢气与氯气混合反应后气体的总体积为
②原氢氧化钠溶液浓度为
您最近半年使用:0次
【推荐2】为测定人体血液中Ca2+的含量,设计了如下方案:
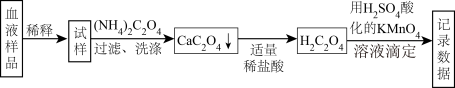
若血液样品取15.00mL,滴定时消耗0.0010mol/LKMnO4溶液15.00mL,求血液样品中Ca2+的物质的量浓度______ 。(已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O)

若血液样品取15.00mL,滴定时消耗0.0010mol/LKMnO4溶液15.00mL,求血液样品中Ca2+的物质的量浓度
您最近半年使用:0次
计算题
|
较易
(0.85)
名校
【推荐1】实验室常用硫酸的质量分数为98%,密度为1.80g/cm3。
(1)此硫酸的物质的量浓度是_______ (列式计算)。
(2)从该溶液中取出2L,加水稀释到10L,稀释后溶液的物质的量浓度是_______ 。
(1)此硫酸的物质的量浓度是
(2)从该溶液中取出2L,加水稀释到10L,稀释后溶液的物质的量浓度是
您最近半年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐2】如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:

(1)该浓盐酸中HCl的物质的量浓度为_______ mol/L (写出计算过程)
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是( )
a. 溶液中溶解的HCl的物质的量 b. 溶液的浓度 c. 溶液中Cl-的数目 d. 溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制500ml 物质的量浓度为0.400 mol/L 的稀盐酸。该学生需要量取_______ ml上述浓盐酸进行配制。
(4)假设该同学成功配制了0.400 mol/L 的盐酸,他又用该盐酸中和含0.4g NaOH的NaOH溶液,则该同学需取_______ ml盐酸

(1)该浓盐酸中HCl的物质的量浓度为
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是
a. 溶液中溶解的HCl的物质的量 b. 溶液的浓度 c. 溶液中Cl-的数目 d. 溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制500ml 物质的量浓度为0.400 mol/L 的稀盐酸。该学生需要量取
(4)假设该同学成功配制了0.400 mol/L 的盐酸,他又用该盐酸中和含0.4g NaOH的NaOH溶液,则该同学需取
您最近半年使用:0次

 ;其中所含碳元素的质量分数为20%,所含氢元素的质量分数为3.0%,所含氧元素的质量分数为28%,其余为N、S。
;其中所含碳元素的质量分数为20%,所含氢元素的质量分数为3.0%,所含氧元素的质量分数为28%,其余为N、S。

