下图为实验室制取纯净干燥的Cl2,并进行检验Cl2性质实验和收集装置。其中E瓶中放有干燥红色布条;F中为铜网,F右端出气管口附近放在脱脂棉。试回答:
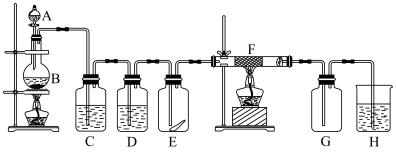
(1)A中所放试剂为__________ ,B中所放试剂为__________ ,二者反应的离子方程式为__________ 。
(2)C中试剂是__________ ;D中试剂的作用是__________ 。
(3)E中现象是__________ ;若要使红色布条褪色,需将红条预先进行__________ 。
(4)F中现象是__________ ,其反应的化学方程式为__________ ;F管中脱脂棉的作用是__________ 。
(5)H中试剂是__________ ,反应的离子方程式为__________ 。
(6)整套装置中有两处用酒精灯加热,两处酒精灯点燃的先后顺序是__________ 。

(1)A中所放试剂为
(2)C中试剂是
(3)E中现象是
(4)F中现象是
(5)H中试剂是
(6)整套装置中有两处用酒精灯加热,两处酒精灯点燃的先后顺序是
更新时间:2020-11-06 15:39:04
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】亚硝酰氯(NOCl,熔点:-64.5℃,沸点:-5.5℃)是一种黄色气体,遇水易反应,生成一种氯化物和两种常见的氮氧化物,其中一种呈红棕色。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
(1)甲组的同学拟制备原料气NO和Cl2,制备装置如图所示:

为制备纯净干燥的气体,下表中缺少的药品是:
(2)乙组同学利用甲组制得的NO和Cl2制备NOCl,装置如图所示:


①装置连接顺序为a→_______ (按气流自左向右方向,用小写字母表示)。
②为了使实验顺利进行,实验中先通入的气体是_____ (填Cl2或NO),待装置Ⅴ中充满气体时,再将另一气体缓缓通入,此操作的目的是_____ 。
③装置Ⅴ生成NOCl的化学方程式是_____ 。
④装置Ⅵ的作用为_____ ,若无该装置,Ⅷ中NOCl可能发生反应的化学方程式为_______ 。
(3)丁组同学用以下方法测定亚硝酰氯(NOCl)纯度:取Ⅷ中所得液体m克溶于水,配制成250mL溶液,取出25.00mL,以K2CrO4溶液为指示剂,用c mol/LAgNO3 标准溶液滴定至终点,消耗标准溶液的体积为b mL。亚硝酰氯(NOCl)的质量分数为_________ (用代数式表示即可)。
(1)甲组的同学拟制备原料气NO和Cl2,制备装置如图所示:

为制备纯净干燥的气体,下表中缺少的药品是:
| 制备原料 | 装置Ⅰ | 装置Ⅱ | |
| 烧瓶中 | 分液漏斗中 | ||
| 制备纯净Cl2 | MnO2 | ① | 饱和食盐水 |
| 制备纯净NO | Cu | 稀硝酸 | ② |


①装置连接顺序为a→
②为了使实验顺利进行,实验中先通入的气体是
③装置Ⅴ生成NOCl的化学方程式是
④装置Ⅵ的作用为
(3)丁组同学用以下方法测定亚硝酰氯(NOCl)纯度:取Ⅷ中所得液体m克溶于水,配制成250mL溶液,取出25.00mL,以K2CrO4溶液为指示剂,用c mol/LAgNO3 标准溶液滴定至终点,消耗标准溶液的体积为b mL。亚硝酰氯(NOCl)的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某研究性学习小组利用 和浓盐酸制取、收集纯净的氯气并探究氯气的性质,他们设计如下实验装置。
和浓盐酸制取、收集纯净的氯气并探究氯气的性质,他们设计如下实验装置。

回答下列问题:
(1)气体发生装置选择______ (填A、B)。装置的连接顺序是:发生装置接______ 、______ 接______ 、______ 接______ 。(填各接口的小写字母)
(2)制氯气的离子方程式是______ 。
(3)C装置的作用是______ ,D装置中试剂Y是______ 。
(4)E装置观察到溶液先变蓝,继续通 ,蓝色褪去。小组同学探究蓝色褪去可能的原因。
,蓝色褪去。小组同学探究蓝色褪去可能的原因。
查阅资料可知: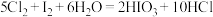
甲同学认为是______ (填化学式)漂白了蓝色物质而褪色;
乙同学认为是过量的氯气与 发生了反应,当溶液中
发生了反应,当溶液中 反应完全了,蓝色褪去。他们设计实验方案并进行了实验:取少量E中恰好褪色的溶液于试管中,加入
反应完全了,蓝色褪去。他们设计实验方案并进行了实验:取少量E中恰好褪色的溶液于试管中,加入______ ,观察到______ ,说明乙同学的观点是正确。
(5)在大扫除中,同学们用漂白粉溶液拖地杀菌消毒,漂白粉生效的化学方程式为______ 。
 和浓盐酸制取、收集纯净的氯气并探究氯气的性质,他们设计如下实验装置。
和浓盐酸制取、收集纯净的氯气并探究氯气的性质,他们设计如下实验装置。
回答下列问题:
(1)气体发生装置选择
(2)制氯气的离子方程式是
(3)C装置的作用是
(4)E装置观察到溶液先变蓝,继续通
 ,蓝色褪去。小组同学探究蓝色褪去可能的原因。
,蓝色褪去。小组同学探究蓝色褪去可能的原因。查阅资料可知:
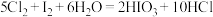
甲同学认为是
乙同学认为是过量的氯气与
 发生了反应,当溶液中
发生了反应,当溶液中 反应完全了,蓝色褪去。他们设计实验方案并进行了实验:取少量E中恰好褪色的溶液于试管中,加入
反应完全了,蓝色褪去。他们设计实验方案并进行了实验:取少量E中恰好褪色的溶液于试管中,加入(5)在大扫除中,同学们用漂白粉溶液拖地杀菌消毒,漂白粉生效的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】如图是某同学设计的制取氯气以及验证氯气的性质的实验,回答下列问题
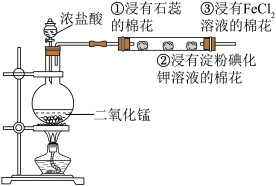
(1)该同学制取氯气的反应原理是:____________________ (写化学方程式)。
(2)实验过程中②处观察到的现象是__________ 说明氯气具有的性质是______________ 。
(3)该实验操作的不足之处是_______________
(4)实验室用MnO2和浓盐酸制取Cl2时,有14.6 g氯化氢被氧化,所得Cl2全部用NaOH溶液吸收,生成NaClO的物质的量是________ mol

(1)该同学制取氯气的反应原理是:
(2)实验过程中②处观察到的现象是
(3)该实验操作的不足之处是
(4)实验室用MnO2和浓盐酸制取Cl2时,有14.6 g氯化氢被氧化,所得Cl2全部用NaOH溶液吸收,生成NaClO的物质的量是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
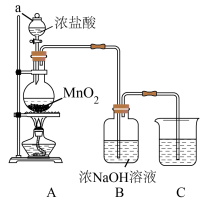
【推荐1】某同学利用 与浓
与浓 溶液制备“84”消毒液,装置如下图:
溶液制备“84”消毒液,装置如下图:
已知:①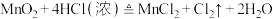 浓
浓
② 与
与 溶液的反应为放热反应,温度升高时易发生副反应。
溶液的反应为放热反应,温度升高时易发生副反应。
(1)仪器 的名称是
的名称是______ ,“84”消毒液的有效成分是______ (填化学式)。
(2)制备“84”消毒液的化学方程式为______ 。
(3)圆底烧瓶中发生反应的离子方程式为______ 。
(4)上述装置存在两处缺陷,会导致产率降低,改进的方法是______ 。
(5)装置 的作用是
的作用是______ 。
 与浓
与浓 溶液制备“84”消毒液,装置如下图:
溶液制备“84”消毒液,装置如下图:
已知:①
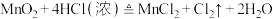 浓
浓②
 与
与 溶液的反应为放热反应,温度升高时易发生副反应。
溶液的反应为放热反应,温度升高时易发生副反应。(1)仪器
 的名称是
的名称是(2)制备“84”消毒液的化学方程式为
(3)圆底烧瓶中发生反应的离子方程式为
(4)上述装置存在两处缺陷,会导致产率降低,改进的方法是
(5)装置
 的作用是
的作用是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】新型绿色氧化剂高铁酸钾的一种制备工艺流程如下:

回答下列问题:
(1)步骤①中NaClO作_______________ (填“氧化剂”“还原剂”或“催化剂”)。写出步骤①反应的离子方程式______________________________ 。
(2)步骤②脱除的盐是_______________ (填他学式)。
(3)步骤③反应的化学方程式为2KOH+Na2FeO4=K2FeO4+2NaOH,分析该反应能发生的原因__________________________________ 。
(4)本次实验中K2FeO4的产率为______ 。
(5)高铁酸盐在水溶液中有四种含铁形体。25℃时,它们的物质的量分数随pH的变化如图所示。则pH=2.2时,溶液中主要含铁形体浓度的大小关系为_______________ ;为获得尽可能纯净的高铁酸盐,pH应控制在____________ 。


回答下列问题:
(1)步骤①中NaClO作
(2)步骤②脱除的盐是
(3)步骤③反应的化学方程式为2KOH+Na2FeO4=K2FeO4+2NaOH,分析该反应能发生的原因
(4)本次实验中K2FeO4的产率为
(5)高铁酸盐在水溶液中有四种含铁形体。25℃时,它们的物质的量分数随pH的变化如图所示。则pH=2.2时,溶液中主要含铁形体浓度的大小关系为

您最近一年使用:0次




