图中,A为一种中学化学中常见的单质,B、C、D、E是含有A元素的常见化合物。它们的焰色实验均为黄色。
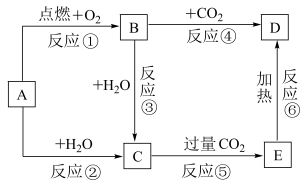
(1)写出A的原子结构示意图___________ ,B的化学式___________ 。
(2)以上6个反应中属于氧化还原反应的有___________ (填写编号)。
(3)写出B→D反应的化学方程式___________ ,C溶液→E反应的离子方程式___________ 。
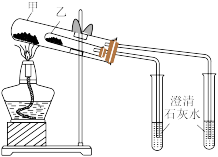
(4)若用所示装置验证D和E的稳定性,则试管乙中装入的固体最好是___________ (填化学式)。
(5)将一定量的B投入到含有下列离子的溶液中: 、
、 、
、 、Na+,反应完毕后,溶液中上述离子数目几乎不变的有(不考虑溶液体积的变化)
、Na+,反应完毕后,溶液中上述离子数目几乎不变的有(不考虑溶液体积的变化)____________ 填离子符号)。


(1)写出A的原子结构示意图
(2)以上6个反应中属于氧化还原反应的有
(3)写出B→D反应的化学方程式
(4)若用所示装置验证D和E的稳定性,则试管乙中装入的固体最好是
(5)将一定量的B投入到含有下列离子的溶液中:
 、
、 、
、 、Na+,反应完毕后,溶液中上述离子数目几乎不变的有(不考虑溶液体积的变化)
、Na+,反应完毕后,溶液中上述离子数目几乎不变的有(不考虑溶液体积的变化)
20-21高一上·浙江丽水·阶段练习 查看更多[3]
更新时间:2020-11-12 20:54:44
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】有关物质的转化关系如下图所示。A、B、C、E为气体,其中A能使湿润的红色石蕊试纸变蓝,B为无色单质,E是为红棕色。G是紫红色金属单质,H的水溶液为蓝色。

⑴A的电子式为______ 。
⑵写出反应①的化学方程式:______ 。
⑶写出反应③的化学方程式:______ 。该方程式中转移的电子数目为______ 个。
⑷写出反应④的离子方程式:_____ 。

⑴A的电子式为
⑵写出反应①的化学方程式:
⑶写出反应③的化学方程式:
⑷写出反应④的离子方程式:
您最近一年使用:0次
【推荐2】已知B是常见金属单质,E为常见非金属单质,H常温下为无色液体,C的浓溶液在加热时才与D反应。根据下列框图所示,试回答:
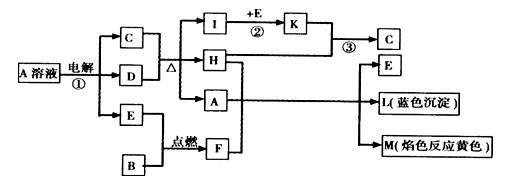
(1)写出化学式:A_______ ;E_______ ;L_______ 。
(2)反应①的离子方程式:_______ 。
(3)反应②,工业上采取的反应条件是_______ 。
(4)反应③,工业上采取的操作不是K直接与H反应,原因是_______ 。
(5)每生成1 mol K,反应放出98.3 kJ热量,该反应的热化学方程式为:_______ 。

(1)写出化学式:A
(2)反应①的离子方程式:
(3)反应②,工业上采取的反应条件是
(4)反应③,工业上采取的操作不是K直接与H反应,原因是
(5)每生成1 mol K,反应放出98.3 kJ热量,该反应的热化学方程式为:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】已知A、B、C、D、E、F是含有同一种元素的化合物,其中F是能使湿润的红色石蕊试纸变蓝的气体,它们之间能发生如下反应:①A+H2O→B+C;②C+F→D;③D+NaOH F+E+H2O。
F+E+H2O。
(1)写出它们的化学式:A________ 、C________ 、D________ 、F________ 。
(2)写出下列反应的离子方程式,并按要求填空:
①_____________ ,这个反应的氧化剂是________ ,还原剂是________ ;
③____________________________ 。
(3)工业生产C的过程中有如下一步反应,即F经催化氧化生成B和H2O,写出该步反应的化学方程式________ 。
 F+E+H2O。
F+E+H2O。(1)写出它们的化学式:A
(2)写出下列反应的离子方程式,并按要求填空:
①
③
(3)工业生产C的过程中有如下一步反应,即F经催化氧化生成B和H2O,写出该步反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】已知A、B均是由两种短周期元素组成的化合物,A中某元素的质量分数为25% ,B的焰色反应呈黄色,C、J、X是同周期的元素的氢化物,X为无色液体,C、J为气体,D是一种不溶于水的白色固体。在一定条件下,它们有如图所示的转化关系。
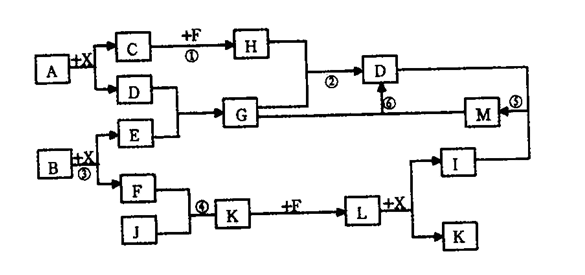
试回答下列问题:
(1)写出化学式:A_______ ,E_______ ,L_______ 。
(2)在反应①~⑥中,属于氧化还原反应的是_______ 。
(3)反应③的化学方程式为_______ 。
(4)写出下列离子反应方程式:
反应②_______ ;
反应⑥_______ 。
(5)将3.4gJ气体与足量的F反应,生成 一种单质和X,恢复到25°C放出a kJ热量,写出该反应的热化学方程式:_______ 。

试回答下列问题:
(1)写出化学式:A
(2)在反应①~⑥中,属于氧化还原反应的是
(3)反应③的化学方程式为
(4)写出下列离子反应方程式:
反应②
反应⑥
(5)将3.4gJ气体与足量的F反应,生成 一种单质和X,恢复到25°C放出a kJ热量,写出该反应的热化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】茶垢清洁剂的主要成分是过碳酸钠(Na2CO3∙3H2O2)。过碳酸钠兼具Na2CO3和H2O2的性质,能溶于水,热水溶解后,能迅速放出活性气体,快速清洁茶具上附着的茶垢。某化学实验小组进行了下列实验。请回答下列问题:
I.探究过碱酸钠与热水反应生成的气体成分:
实验1:向盛有茶垢清洁剂的试管中加入少量热水并将试管加热竹80℃,将试管中生成的气体通入澄清石灰水中,无明显现象。
实验2:向盛有茶垢清洁剂的试管中加入少量热水并将试管加热至80℃,……
实验结论:碳酸钠与热水反应生成的气体为O2。
(1)实验1和实验2中适宜的加热方式为水浴加热,与用酒精灯直接加热相比,采用水浴加热的优点为____ (答一条)。
(2)请补全实验2中能证明生成气体为O2的实验操作和现象:___ 。
II.测定茶垢清洁剂中的过碳酸钠含量
实验3:排水量气法测定过碳酸钠含量:按下图连接好实验装置并放入药品,打开分液漏斗活塞,使水滴入锥形瓶中,一段时间后,关闭活塞,读取生成气体的体积。
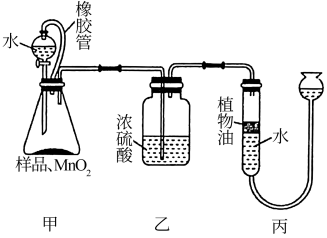
(3)实验3中装置甲中橡胶管的作用为___ 。若实验结束后测得反应生成气体的体积为VL,若加入样品质量为mg,O2的在该实验条件下的密度为dg/L,则计算得到茶垢清洁剂中的过碳酸钠的质量分数为__ (结果用含m、d、V的式子表示)。
III.探究过碳酸钠的制备过程中合适的原料配比
实验4:10℃时,将4份等量的饱和 溶液和质量分数均为27.5%的
溶液和质量分数均为27.5%的 溶液按不同配比混合,发生反应
溶液按不同配比混合,发生反应 。反应时间为
。反应时间为 ,测得原料配比对过碳酸钠的产率和溶液中活性氧的含量的关系如下表所示。
,测得原料配比对过碳酸钠的产率和溶液中活性氧的含量的关系如下表所示。
(4)由题给数据可知实验4中 和
和 较合适的物质的量之比为
较合适的物质的量之比为_ ,当原料配比增至1.8∶l时,过碳酸钠的产率下降的原因为_ 。
I.探究过碱酸钠与热水反应生成的气体成分:
实验1:向盛有茶垢清洁剂的试管中加入少量热水并将试管加热竹80℃,将试管中生成的气体通入澄清石灰水中,无明显现象。
实验2:向盛有茶垢清洁剂的试管中加入少量热水并将试管加热至80℃,……
实验结论:碳酸钠与热水反应生成的气体为O2。
(1)实验1和实验2中适宜的加热方式为水浴加热,与用酒精灯直接加热相比,采用水浴加热的优点为
(2)请补全实验2中能证明生成气体为O2的实验操作和现象:
II.测定茶垢清洁剂中的过碳酸钠含量
实验3:排水量气法测定过碳酸钠含量:按下图连接好实验装置并放入药品,打开分液漏斗活塞,使水滴入锥形瓶中,一段时间后,关闭活塞,读取生成气体的体积。

(3)实验3中装置甲中橡胶管的作用为
III.探究过碳酸钠的制备过程中合适的原料配比
实验4:10℃时,将4份等量的饱和
 溶液和质量分数均为27.5%的
溶液和质量分数均为27.5%的 溶液按不同配比混合,发生反应
溶液按不同配比混合,发生反应 。反应时间为
。反应时间为 ,测得原料配比对过碳酸钠的产率和溶液中活性氧的含量的关系如下表所示。
,测得原料配比对过碳酸钠的产率和溶液中活性氧的含量的关系如下表所示。| 过氧化氢与碳酸钠的物质的量比 | 过碳酸钠的产率/% | 活性氧的含量/% |
| 1.8∶l | 78.91 | 12.70 |
| 1.7∶1 | 81.08 | 12.71 |
| 1.6∶1 | 79.53 | 12.67 |
| 1.5∶1 | 76.02 | 12.68 |
 和
和 较合适的物质的量之比为
较合适的物质的量之比为
您最近一年使用:0次
【推荐3】现有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 九种物质,其中
九种物质,其中 为淡黄色粉末,
为淡黄色粉末, 为黄绿色气体单质,
为黄绿色气体单质, 为无色气体单质,
为无色气体单质, 的水溶液与石灰水混合可得
的水溶液与石灰水混合可得 的溶液,它们之间的相互转化关系如图所示,其他与题无关的生成物均已略去。
的溶液,它们之间的相互转化关系如图所示,其他与题无关的生成物均已略去。

请回答下列问题:
(1)写出 、
、 的化学式:
的化学式:
___________ ,
___________ 。 的俗名是
的俗名是___________ , 的重要用途:
的重要用途:___________ 。
(2)写出反应①②的离子方程式:①___________ ;②___________ 。
(3)已知 (氰根离子)和
(氰根离子)和 有相似之处;氰分子
有相似之处;氰分子 的性质与
的性质与 的性质有相似之处,且常温常压下是气体。试写出
的性质有相似之处,且常温常压下是气体。试写出 和
和 溶液加热反应的化学方程式:
溶液加热反应的化学方程式:___________ 。
(4)利用如图装置进行实验,证明氧化性强弱: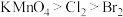 。限选试剂:
。限选试剂: 溶液、
溶液、 、浓盐酸、浓硫酸。
、浓盐酸、浓硫酸。

已知: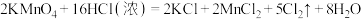 。
。
请回答下列问题:
①装置 、
、 中盛放的试剂分别是
中盛放的试剂分别是___________ 、___________ 。
②此实验装置的不足之处是___________ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 九种物质,其中
九种物质,其中 为淡黄色粉末,
为淡黄色粉末, 为黄绿色气体单质,
为黄绿色气体单质, 为无色气体单质,
为无色气体单质, 的水溶液与石灰水混合可得
的水溶液与石灰水混合可得 的溶液,它们之间的相互转化关系如图所示,其他与题无关的生成物均已略去。
的溶液,它们之间的相互转化关系如图所示,其他与题无关的生成物均已略去。
请回答下列问题:
(1)写出
 、
、 的化学式:
的化学式:

 的俗名是
的俗名是 的重要用途:
的重要用途:(2)写出反应①②的离子方程式:①
(3)已知
 (氰根离子)和
(氰根离子)和 有相似之处;氰分子
有相似之处;氰分子 的性质与
的性质与 的性质有相似之处,且常温常压下是气体。试写出
的性质有相似之处,且常温常压下是气体。试写出 和
和 溶液加热反应的化学方程式:
溶液加热反应的化学方程式:(4)利用如图装置进行实验,证明氧化性强弱:
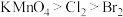 。限选试剂:
。限选试剂: 溶液、
溶液、 、浓盐酸、浓硫酸。
、浓盐酸、浓硫酸。
已知:
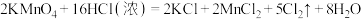 。
。请回答下列问题:
①装置
 、
、 中盛放的试剂分别是
中盛放的试剂分别是②此实验装置的不足之处是
您最近一年使用:0次



