现有含有少量NaCl、Na2SO4、Na2CO3等杂质的NaNO3溶液,选择适当的试剂除去杂质,得到纯净的NaNO3固体,实验流程如图所示。
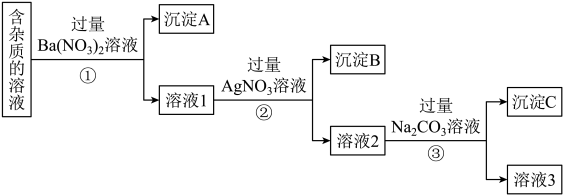
(1)②中反应的离子方程式是________________________ 。
(2)①②③中均进行的分离操作是______ (填操作名称)。
(3)③中加入过量的Na2CO3溶液的目的是________________________________ 。
(4)溶液3经过处理可以得到NaNO3固体,为了除去杂质,可向溶液3中加入适量的_______ 。(填化学式)
(5)实验室用上述实验获得的NaNO3固体配制480mL 0.40mol/L NaNO3溶液。
①配制溶液时,称取NaNO3固体的质量是_____ g。
②实验所需玻璃仪器有烧杯、玻璃棒、量筒、__________ 、___________ 。
③配制时,一般可分为以下几个步骤:
A称量B计算C溶解D摇匀E移液F洗涤G定容H冷却
正确的操作顺序为:_______________________________ (填序号)。
④下列操作可能使配制溶液浓度偏低的是________ (填字母)。
A.移液时,未洗涤烧杯内壁和玻璃棒
B.溶解后未经冷却就移液
C.移液时,有少量液体溅出
D.摇匀后,液面低于刻度线,加蒸馏水至刻度线
E.配制前,容量瓶中有少量蒸馏水

(1)②中反应的离子方程式是
(2)①②③中均进行的分离操作是
(3)③中加入过量的Na2CO3溶液的目的是
(4)溶液3经过处理可以得到NaNO3固体,为了除去杂质,可向溶液3中加入适量的
(5)实验室用上述实验获得的NaNO3固体配制480mL 0.40mol/L NaNO3溶液。
①配制溶液时,称取NaNO3固体的质量是
②实验所需玻璃仪器有烧杯、玻璃棒、量筒、
③配制时,一般可分为以下几个步骤:
A称量B计算C溶解D摇匀E移液F洗涤G定容H冷却
正确的操作顺序为:
④下列操作可能使配制溶液浓度偏低的是
A.移液时,未洗涤烧杯内壁和玻璃棒
B.溶解后未经冷却就移液
C.移液时,有少量液体溅出
D.摇匀后,液面低于刻度线,加蒸馏水至刻度线
E.配制前,容量瓶中有少量蒸馏水
更新时间:2020-11-11 21:02:27
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】高铁酸钾(K2FeO4)是一种环保、高效饮水处理剂,利用铁屑制备的简略流程如图所示:

请回答下列问题:
(1)反应Ⅰ的生成物中可能含有的金属阳离子是___________ (用离子符号表示),如何检验该离子___________ 。
(2)操作A和操作B相同,其操作名称是___________ ;由操作B判断该生产条件下物质的溶解性:Na2FeO4___________ K2FeO4 (填“>”或“<”)。
(3)溶液C可与氯气反应制取漂白液,其离子方程式为___________ 。
(4)当生产过程中制得2mol的K2FeO4时,反应Ⅱ中转移的电子数为___________ 。
(5)反应Ⅱ中用到NaOH,若某同学做实验时要用到200mL 0.1mol/L NaOH溶液,现进行配制,则:
①配制该浓度的溶液需用托盘天平称量NaOH固体的质量为___________ g;
②配制过程中,下列操作导致所配溶液浓度偏大的是___________ (填标号)。
a.转移溶液时有少许液体溅出
b.溶解后,将溶液直接转移到容量瓶中
c.定容时俯视刻度线
d.定容摇匀后,发现液面下降,继续加水至刻度线

请回答下列问题:
(1)反应Ⅰ的生成物中可能含有的金属阳离子是
(2)操作A和操作B相同,其操作名称是
(3)溶液C可与氯气反应制取漂白液,其离子方程式为
(4)当生产过程中制得2mol的K2FeO4时,反应Ⅱ中转移的电子数为
(5)反应Ⅱ中用到NaOH,若某同学做实验时要用到200mL 0.1mol/L NaOH溶液,现进行配制,则:
①配制该浓度的溶液需用托盘天平称量NaOH固体的质量为
②配制过程中,下列操作导致所配溶液浓度偏大的是
a.转移溶液时有少许液体溅出
b.溶解后,将溶液直接转移到容量瓶中
c.定容时俯视刻度线
d.定容摇匀后,发现液面下降,继续加水至刻度线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】实验室需要0.1mol/LNaOH溶液450ml和0.5mol/L硫酸溶液500ml。根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中,配制溶液肯定不需要的是________ (填序号),配制上述溶液还需用到的玻璃仪器是________ (填仪器名称)。
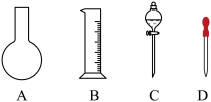
(2)配制0.1mol/L的NaOH溶液的操作步骤如下,正确的顺序是_______ 。
①把称量好的NaOH固体放入小烧杯中,加适量的蒸馏水溶解;
②用少量蒸馏水洗涤烧杯和玻璃棒2~ 3次,每次洗涤的液体都小心转入容量瓶中,并轻轻摇匀;
③继续向容量瓶中加蒸馏水至液面距刻度线1~ 2cm处,改用胶头滴管小心滴加蒸馏水至溶液的凹液面与刻度线相切;
④把①所得溶液冷却至室温,再小心转入一定容积的容量瓶中;
⑤将容量瓶瓶塞塞紧,充分摇匀。
(3)根据计算,用托盘天平称取NaOH的质量为________ g。在实验中其他操作均正确,若容量瓶用蒸馏水洗涤后未干燥,则所得溶液浓度________ 0.1mol/L(填“大于”“小于”或“等于”,下同)。若还未等溶液冷却就定容,则所得溶液浓度________ 0.1mol/L。配制好后,发现称量时所用的托盘天平的砝码生锈了________ 0.1mol/L。
(1)如图所示的仪器中,配制溶液肯定不需要的是

(2)配制0.1mol/L的NaOH溶液的操作步骤如下,正确的顺序是
①把称量好的NaOH固体放入小烧杯中,加适量的蒸馏水溶解;
②用少量蒸馏水洗涤烧杯和玻璃棒2~ 3次,每次洗涤的液体都小心转入容量瓶中,并轻轻摇匀;
③继续向容量瓶中加蒸馏水至液面距刻度线1~ 2cm处,改用胶头滴管小心滴加蒸馏水至溶液的凹液面与刻度线相切;
④把①所得溶液冷却至室温,再小心转入一定容积的容量瓶中;
⑤将容量瓶瓶塞塞紧,充分摇匀。
(3)根据计算,用托盘天平称取NaOH的质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某同学按下列步骤配制500 mL 0.20 mol·L-1KNO3溶液,请回答有关问题。
(6)你认为按上述步骤配制的KNO3溶液的浓度____ 0.20 mol·L-1(填大于、小于、等于),原因是__________________________________________ (若等于,该空可不填)
以下操作不会对所配溶液浓度产生影响的是__________ 。
A.称量时物品与砝码位置放颠倒了 B.溶解时烧杯内有少量水
C.将烧杯内溶液注入容量瓶时有少量液体溅出 D.定容时俯视刻度线
E.容量瓶内有少量水 F.摇匀后发现液面低于刻度线,又补加少量水
| 实验步骤 | 有关问题 |
| (1)计算所需称量KNO3的质量 | 需要KNO3的质量为 |
| (2)称量KNO3固体 | 称量过程中主要用到的仪器是 |
| (3)将KNO3加入100 mL烧杯中,加适量蒸馏水溶解 | 为加快溶解,可采取的措施是 |
| (4)将烧杯中已恢复到室温的溶液转移至 | 为防止溶液溅出,应该采取的措施是 |
| (5)向容量瓶中加蒸馏水至刻度线 | 离刻度线 |
以下操作不会对所配溶液浓度产生影响的是
A.称量时物品与砝码位置放颠倒了 B.溶解时烧杯内有少量水
C.将烧杯内溶液注入容量瓶时有少量液体溅出 D.定容时俯视刻度线
E.容量瓶内有少量水 F.摇匀后发现液面低于刻度线,又补加少量水
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】下图是硫酸试剂瓶标签上的内容:
(1)某化学兴趣小组进行硫酸性质的实验探究时,需要460mL0.5mol/L稀硫酸,则用量筒需要取_______ mL的该浓硫酸。
(2)本实验用到的基本仪器已有烧杯、量筒、玻璃棒,还缺少的仪器是_______ 。
(3)将蒸馏水注入容量瓶,当液面离容量瓶刻度线1~2cm时,_______ 。盖好瓶塞,反复上下颠倒,摇匀。
(4)配制溶液有如下(未按顺序排列):a.溶解b.摇匀c.洗涤d.冷却e.称量f.将溶液移至容量瓶g.定容等操作。其中摇匀的前一步操作是_______ (填写字母)
(5)下列配制过程示意图中,有不正确 的是(填写序号)_______
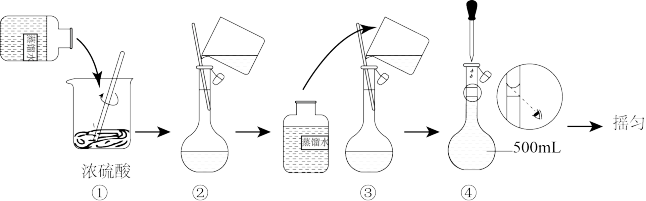
(6)配制0.5mol/L稀硫酸的过程中,下列情况会引起硫酸溶液物质的量浓度偏高是_______。
| 硫酸:化学纯(CP)(500mL) 品名:硫酸 化学式:H2SO4 相对分子质量:98 密度:1.84g/cm3 质量分数:98% |
(2)本实验用到的基本仪器已有烧杯、量筒、玻璃棒,还缺少的仪器是
(3)将蒸馏水注入容量瓶,当液面离容量瓶刻度线1~2cm时,
(4)配制溶液有如下(未按顺序排列):a.溶解b.摇匀c.洗涤d.冷却e.称量f.将溶液移至容量瓶g.定容等操作。其中摇匀的前一步操作是
(5)下列配制过程示意图中,有

(6)配制0.5mol/L稀硫酸的过程中,下列情况会引起硫酸溶液物质的量浓度偏高是_______。
| A.用量筒量取浓硫酸时仰视读数 | B.未经冷却将溶液注入容量瓶中 |
| C.摇匀后液面低于刻度线,再滴加蒸馏水 | D.未洗涤烧杯和玻璃棒 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】如图为实验室某浓盐酸试制瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:

(1)该浓盐酸中HCl的物质的量浓度为_______ 。
(2)某学生欲用上述浓盐酸和蒸馏水配制480 mL物质的量浓度为0.400 mol·L-1的稀盐酸。
可供选用的仪器有:玻璃棒、烧杯、量筒、托盘天平。
①配制稀盐酸时,还缺少的仪器有_______ 。(写仪器名称)
②该学生需要量取_______ mL上述浓盐酸进行配制。
③在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(填“偏大”“偏小”或“无影响”)
a.用量筒量取浓盐酸时俯视观察凹液面_______ 。
b.洗涤量取浓盐酸的量筒,并将洗涤液移入容量瓶_______ 。
(3)假设该同学成功配制了0.400 mol·L-1的盐酸,他又用该盐酸中和含0.4 g NaOH的NaOH溶液,则该同学需用量筒取_______ mL盐酸。

(1)该浓盐酸中HCl的物质的量浓度为
(2)某学生欲用上述浓盐酸和蒸馏水配制480 mL物质的量浓度为0.400 mol·L-1的稀盐酸。
可供选用的仪器有:玻璃棒、烧杯、量筒、托盘天平。
①配制稀盐酸时,还缺少的仪器有
②该学生需要量取
③在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(填“偏大”“偏小”或“无影响”)
a.用量筒量取浓盐酸时俯视观察凹液面
b.洗涤量取浓盐酸的量筒,并将洗涤液移入容量瓶
(3)假设该同学成功配制了0.400 mol·L-1的盐酸,他又用该盐酸中和含0.4 g NaOH的NaOH溶液,则该同学需用量筒取
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某同学欲用浓H2SO4配制480mL0.2mol·L-1的稀H2SO4。
(1)需要用量筒量取98%密度为1.84g·cm-3的浓硫酸___ mL。
(2)配制时,必须使用的仪器有___ (填代号),还缺少的仪器是___ 、___ 。
①烧杯;②10mL量筒;③20mL量筒;④托盘天平(带砝码);⑤玻璃棒
(3)配制过程中出现以下情况,使所配溶液浓度偏高的是____ 。
①容量瓶没有干燥;
②用量筒量取98%的硫酸溶液时仰视;
③溶液转移到容量瓶后,未进行洗涤操作;
④定容时仰视;
⑤如果加水超过了刻度线,取出水使液面恰好到刻度线;
⑥溶解后未冷却就转移到容量瓶
(1)需要用量筒量取98%密度为1.84g·cm-3的浓硫酸
(2)配制时,必须使用的仪器有
①烧杯;②10mL量筒;③20mL量筒;④托盘天平(带砝码);⑤玻璃棒
(3)配制过程中出现以下情况,使所配溶液浓度偏高的是
①容量瓶没有干燥;
②用量筒量取98%的硫酸溶液时仰视;
③溶液转移到容量瓶后,未进行洗涤操作;
④定容时仰视;
⑤如果加水超过了刻度线,取出水使液面恰好到刻度线;
⑥溶解后未冷却就转移到容量瓶
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现如图所示的物质之间的变化:

据此回答下列问题:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是_______ 。
(2)固体B的化学式为_______ ;沉淀C所含的物质为_______ (填化学式)。
(3)反应②的离子方程式为_______ 。
(4)反应③的离子方程式为_______ 。
(5)若要将硫酸铁溶液中含有的少量Fe2+除去,可加适量双氧水,则离子方程式为:_______ 。

据此回答下列问题:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是
(2)固体B的化学式为
(3)反应②的离子方程式为
(4)反应③的离子方程式为
(5)若要将硫酸铁溶液中含有的少量Fe2+除去,可加适量双氧水,则离子方程式为:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】氯化钠样品含有少量的Na2SO4和Na2CO3,按下列流程进行净化。
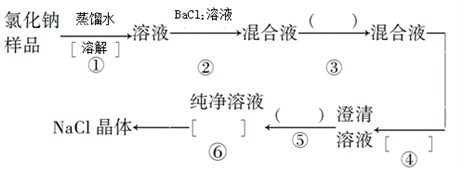
(1)步骤③加入沉淀剂是________ ;步骤⑤加入足量盐酸作用是________ ;步骤⑥操作名称__________ 。
(2)写出有关反应离子方程式
步骤②________________ ;__________________ 。
步骤⑤________________________________ 。
(3)在进行①、④、⑥操作时,都要用到玻璃棒,其作用分别是:步骤④_________________ ; ⑥________________ 。

(1)步骤③加入沉淀剂是
(2)写出有关反应离子方程式
步骤②
步骤⑤
(3)在进行①、④、⑥操作时,都要用到玻璃棒,其作用分别是:步骤④
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】I.从海水得到的粗盐中常含有Ca2+、Mg2+、SO ,需要分离提纯。现有含少量CaCl2、MgSO4的粗盐水,在除去悬浮物和泥沙之后,要用4种试剂①盐酸②Na2CO3③NaOH④BaCl2来除去食盐水中Ca2+、Mg2+、SO
,需要分离提纯。现有含少量CaCl2、MgSO4的粗盐水,在除去悬浮物和泥沙之后,要用4种试剂①盐酸②Na2CO3③NaOH④BaCl2来除去食盐水中Ca2+、Mg2+、SO 。提纯的操作步骤和加入试剂的情况如图1:
。提纯的操作步骤和加入试剂的情况如图1:

图中a、b、c、d分别表示上述4种试剂中的一种,试回答:
(1)生成沉淀A的化学方程式是__________________ ;
(2)试剂d是_________ ;判断试剂d已经足量的简单方法是_________ ;如果在加入d试剂前没有过滤,引起的后果是__________________
(3)现有图2仪器,过滤出沉淀A、B、C时必须用到____________ (填序号)。

(4)海水蒸馏是由海水获得淡水的常用方法之一,在实验室里组成一套蒸馏装置肯定需要上述仪器中的一部分,则正确的是_________ (填序号);实验②中除加入少量适量海水外,还需要加入_______________ ,其作用是____________
(5)海带等藻类物质经过处理后,可以得到碘水,欲从碘水中提取碘,需要上述仪器中的______ (填序号),该仪器名称为_______ ,为了使该仪器中液体能够顺利流下,应进行的具体操作是_________ 。向该碘水中加入四氯化碳以提取碘单质的实验操作名称为______________
 ,需要分离提纯。现有含少量CaCl2、MgSO4的粗盐水,在除去悬浮物和泥沙之后,要用4种试剂①盐酸②Na2CO3③NaOH④BaCl2来除去食盐水中Ca2+、Mg2+、SO
,需要分离提纯。现有含少量CaCl2、MgSO4的粗盐水,在除去悬浮物和泥沙之后,要用4种试剂①盐酸②Na2CO3③NaOH④BaCl2来除去食盐水中Ca2+、Mg2+、SO 。提纯的操作步骤和加入试剂的情况如图1:
。提纯的操作步骤和加入试剂的情况如图1:
图中a、b、c、d分别表示上述4种试剂中的一种,试回答:
(1)生成沉淀A的化学方程式是
(2)试剂d是
(3)现有图2仪器,过滤出沉淀A、B、C时必须用到

(4)海水蒸馏是由海水获得淡水的常用方法之一,在实验室里组成一套蒸馏装置肯定需要上述仪器中的一部分,则正确的是
(5)海带等藻类物质经过处理后,可以得到碘水,欲从碘水中提取碘,需要上述仪器中的
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】信息时代产生的大量电子垃圾对环境造成了极大的威胁。某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,得到含70%Cu、25%Al、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜晶体的路线:

回答下列问题:
(1)第①步Cu与酸反应的离子方程式为_______________________________________ ;得到滤渣1的主要成分为________________ 。
(2)第②步加入H2O2的作用是______________________________________ ,使用H2O2的优点是______________________________________________ ;调节pH的目的是使_______________ 生成沉淀。
(3)用第③步所得CuSO4·5H2O制备无水CuSO4的方法是_______________________ 。
(4)由滤渣2制取Al2(SO4)3·18H2O,探究小组设计了三种方案:
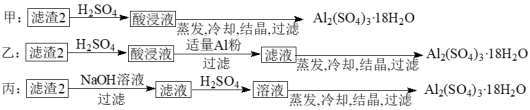
上述三种方案中,______ 方案不可行 。

回答下列问题:
(1)第①步Cu与酸反应的离子方程式为
(2)第②步加入H2O2的作用是
(3)用第③步所得CuSO4·5H2O制备无水CuSO4的方法是
(4)由滤渣2制取Al2(SO4)3·18H2O,探究小组设计了三种方案:

上述三种方案中,
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】青蒿素,是烃的含氧衍生物,为无色针状晶体,易溶于丙酮、氯仿和苯中,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156~157℃,热稳定性差,青蒿素是高效的抗疟药。已知:乙醚沸点为35℃。从青蒿中提取青蒿素的方法之一是以萃取原理为基础的,主要有乙醚浸取法和汽油浸取法。乙醚浸取法的主要工艺为:
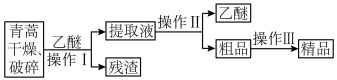
请回答下列问题:
(1)对青蒿进行干燥破碎的目的是__________ ,
(2)操作I需要的玻璃仪器主要有:烧杯、漏斗、__________ ,操作Ⅱ的名称是__________ ,
(3)操作Ⅲ的主要过程可能是_____________ (填字母)。
A.加水溶解,蒸发浓缩、冷却结晶
B.加95%的乙醇,浓缩、结晶、过滤
C.加入乙醚进行萃取分液
(4)用下列实验装置测定青蒿素分子式的方法如下:
将28.2g青蒿素样品放在硬质玻璃管C中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。
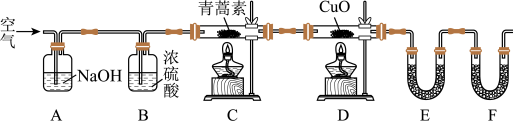
①装置E中盛放的物质是__________ ,
②该实验装置可能会产生误差,造成测定含氧量偏低,改进方法是__________ 。
③用合理改进后的装置进行试验,称得:
则测得青蒿素的最简式是__________ ,
(5)某学生对青蒿素的性质进行探究:将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与__________ (填字母)具有相同的性质。
A.乙醇 B.乙酸 C.乙酸乙酯 D.葡萄糖

请回答下列问题:
(1)对青蒿进行干燥破碎的目的是
(2)操作I需要的玻璃仪器主要有:烧杯、漏斗、
(3)操作Ⅲ的主要过程可能是
A.加水溶解,蒸发浓缩、冷却结晶
B.加95%的乙醇,浓缩、结晶、过滤
C.加入乙醚进行萃取分液
(4)用下列实验装置测定青蒿素分子式的方法如下:
将28.2g青蒿素样品放在硬质玻璃管C中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。

①装置E中盛放的物质是
②该实验装置可能会产生误差,造成测定含氧量偏低,改进方法是
③用合理改进后的装置进行试验,称得:
| 装置 | 实验前/g | 实验后/g |
| E | 22.6 | 42.4 |
| F | 80.2 | 146.2 |
则测得青蒿素的最简式是
(5)某学生对青蒿素的性质进行探究:将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与
A.乙醇 B.乙酸 C.乙酸乙酯 D.葡萄糖
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献,联合制碱法的主要过程如下图所示(部分物质已略去)。已知: 在常温下的溶解度比NaCl大,而在低温下溶解度比NaCl小。
在常温下的溶解度比NaCl大,而在低温下溶解度比NaCl小。

(1)气体A为___________ (填化学式),操作①名称为___________ 。
(2)向饱和NaCl溶液中通入 和氨气,应先通入(填化学式)
和氨气,应先通入(填化学式)___________ 。
(3)写出反应①的化学方程式___________ 。
(4)向母液中通入氨气、加入氯化钠时温度应控制在___________ (填“常温”或者“低温”); 是该流程的副产品,写出
是该流程的副产品,写出 的一种用途
的一种用途___________ 。
(5)产品碳酸钠中通常含有氯化钠,检验产品中存在氯离子的方法为___________ ;现用沉淀法测定碳酸钠的纯度:取 样品,加水溶解,再加过量的
样品,加水溶解,再加过量的 溶液,充分反应后,过滤、洗涤、干燥后称得沉淀的质量为
溶液,充分反应后,过滤、洗涤、干燥后称得沉淀的质量为 。则此样品中碳酸钠的纯度表达式为
。则此样品中碳酸钠的纯度表达式为___________ 。
 在常温下的溶解度比NaCl大,而在低温下溶解度比NaCl小。
在常温下的溶解度比NaCl大,而在低温下溶解度比NaCl小。
(1)气体A为
(2)向饱和NaCl溶液中通入
 和氨气,应先通入(填化学式)
和氨气,应先通入(填化学式)(3)写出反应①的化学方程式
(4)向母液中通入氨气、加入氯化钠时温度应控制在
 是该流程的副产品,写出
是该流程的副产品,写出 的一种用途
的一种用途(5)产品碳酸钠中通常含有氯化钠,检验产品中存在氯离子的方法为
 样品,加水溶解,再加过量的
样品,加水溶解,再加过量的 溶液,充分反应后,过滤、洗涤、干燥后称得沉淀的质量为
溶液,充分反应后,过滤、洗涤、干燥后称得沉淀的质量为 。则此样品中碳酸钠的纯度表达式为
。则此样品中碳酸钠的纯度表达式为
您最近一年使用:0次



