将等物质的量的A、B混合于2L的密闭容器中,发生如下反应: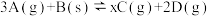 ,经5min后,测得D的浓度为0.4 mol•L-1,C的平均反应速率是0.12mol•L-1•min-1,且此时A、B的物质的量之比为2:3。下列说法不正确的是( )
,经5min后,测得D的浓度为0.4 mol•L-1,C的平均反应速率是0.12mol•L-1•min-1,且此时A、B的物质的量之比为2:3。下列说法不正确的是( )
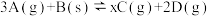 ,经5min后,测得D的浓度为0.4 mol•L-1,C的平均反应速率是0.12mol•L-1•min-1,且此时A、B的物质的量之比为2:3。下列说法不正确的是( )
,经5min后,测得D的浓度为0.4 mol•L-1,C的平均反应速率是0.12mol•L-1•min-1,且此时A、B的物质的量之比为2:3。下列说法不正确的是( )| A.x的值是3 |
| B.开始时A的物质的量为2.8mol |
| C.5min内,B的平均反应速率为0.04mol•L-1•min-1 |
| D.5min时,容器中气体总的物质的量为3.6mol |
20-21高二上·浙江温州·期中 查看更多[10]
2.1.1化学反应速率的表示方法 课后辽宁省沈阳市郊联体2022-2023学年高一下学期5月期中考试化学试题宁夏永宁县永宁中学2021-2022学年高二上学期期中考试化学试题(已下线)专题21 化学反应速率(热点讲义)-2022年高三毕业班化学常考点归纳与变式演练选择性必修1 专题2 第一单元 课时1 化学反应速率的表示方法黑龙江省绥化市海伦市第一中学2021届高三上学期12月月考化学试题湖南省常德市芷兰实验中学2020-2021学年高二上学期第二次月考化学试题湖南省常德市外国语学校2020-2021学年高二上学期第二次月考化学试题陕西省咸阳市秦都区咸阳市实验中学2020-2021学年高二上学期第三次月考化学试题浙江省温州新力量联盟2020-2021学年高二上学期期中联考化学试题
更新时间:2020-11-12 16:35:11
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】反应CO(g)+NO2(g)=CO2(g)+NO(g)的速率方程可表示为v=k·cm(CO)·cn(NO2),其中k为与温度有关的常数,实验测得反应在650K时的数据如下:
下列说法错误的是
| 实验编号 | c(CO)/(mol·L-1) | c(NO2)/(mol·L-1) | v/(mol·L-1·s-1) |
| ① | 0.025 | 0.040 | 2.2×10-4 |
| ② | 0.050 | 0.040 | 4.4×10-4 |
| ③ | 0.025 | 0.120 | 6.6×10-4 |
| ④ | x | y | 8.8×10-4 |
| ⑤ | 0.100 | 0.160 | z |
| A.m=n=1 | B.650K时k=0.22L·mol-1·s-1 |
| C.若x=0.50,则y=0.080 | D.z=3.52×10-3mol·L-1·s-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】反应A(g) +3B(g) 2C(g) +3D(g) 在四种不同情况下的反应速率如下,则反应速率由快到慢的顺序为
2C(g) +3D(g) 在四种不同情况下的反应速率如下,则反应速率由快到慢的顺序为
①v(A)=0.01mol·L-1·s-1 ②v(B)=0.06mol·L-1·s-1
③v(C)=2.4mol·L-1·min-1 ④v(D)=3.5mol·L-1·min-1
 2C(g) +3D(g) 在四种不同情况下的反应速率如下,则反应速率由快到慢的顺序为
2C(g) +3D(g) 在四种不同情况下的反应速率如下,则反应速率由快到慢的顺序为①v(A)=0.01mol·L-1·s-1 ②v(B)=0.06mol·L-1·s-1
③v(C)=2.4mol·L-1·min-1 ④v(D)=3.5mol·L-1·min-1
| A.②>③>④>① | B.④>②=③>① |
| C.②=③>④>① | D.④>①>②>③ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】某化学兴趣小组为探究影响化学反应速率的因素,根据反应 设计并进行实验。实验数据如下:
设计并进行实验。实验数据如下:
表中“3s内 的平均反应速率”的单位是
的平均反应速率”的单位是_______
A.mol/L B.mol/(L·s) C.mol/s
 设计并进行实验。实验数据如下:
设计并进行实验。实验数据如下:| 试验编号 |  起始浓度(mol/L) 起始浓度(mol/L) | HI起始浓度(mol/L) | 温度℃ | 3s内 的平均反应速率 的平均反应速率 |
| 1 | 0.1000 | 0.1000 | 25 | 0.0076 |
| 2 | 0.1000 | 0.2000 | 25 | v |
| 3 | 0.1000 | 0.3000 | 25 | 0.0227 |
| 4 | 0.1000 | c | 35 | 0.0304 |
 的平均反应速率”的单位是
的平均反应速率”的单位是A.mol/L B.mol/(L·s) C.mol/s
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】在2L密闭容器中进行如下反应:N2+3H2 2NH3,5min内氨的物质的量增加了0.1mol,则反应速率为
2NH3,5min内氨的物质的量增加了0.1mol,则反应速率为
 2NH3,5min内氨的物质的量增加了0.1mol,则反应速率为
2NH3,5min内氨的物质的量增加了0.1mol,则反应速率为| A.v(H2)=0.02 mol/(L·min) |
| B.v(N2)=0.01 mol/(L·min) |
| C.v(NH3)=0.01 mol/(L·min) |
| D.v(N2)=0.03 mol/(L·min) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某学习小组为了探究影响酸性高锰酸钾溶液与NaHSO3溶液反应速率的因素,该小组设计如表实验方案。
下列说法正确的是
| 实验 | 0.2mol·L-1NaHSO3溶液/mL | 0.1mol·L-1KMnO4溶液/mL | 0.6mol·L-1H2SO4溶液/mL | 0.1mol·L-1MnSO4溶液/mL | V(H2O)/mL | 混合溶液褪色时间/min |
| 1 | 3.0 | 2.0 | 1.0 | 0 | 2.0 | 8 |
| 2 | 3.0 | 2.0 | 2.0 | 0 | a | 6 |
| 3 | 4.0 | 2.0 | 2.0 | 0 | 0 | 4 |
| 4 | 3.0 | 2.0 | 1.0 | 0.5 | b | 3 |
A.该反应的离子方程式为5SO +2MnO +2MnO +6H+=2Mn2++5SO +6H+=2Mn2++5SO +3H2O +3H2O |
| B.a=1.0、b=1.5 |
C.实验3从反应开始到反应结束这段时间内反应速率v(MnO )=0.025mol·L-1·min-1 )=0.025mol·L-1·min-1 |
D.实验4与实验1相比,说明SO 可能是该反应的催化剂 可能是该反应的催化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】在相同的密闭容器中,用高纯度纳米级Cu2O分别进行催化分解水的实验:2 H2O(g) 2 H2(g) + O2(g) ∆H>0,实验测得反应体系中水蒸气浓度(mol/L)的变化结果如下:
2 H2(g) + O2(g) ∆H>0,实验测得反应体系中水蒸气浓度(mol/L)的变化结果如下:
下列说法不正确 的是
 2 H2(g) + O2(g) ∆H>0,实验测得反应体系中水蒸气浓度(mol/L)的变化结果如下:
2 H2(g) + O2(g) ∆H>0,实验测得反应体系中水蒸气浓度(mol/L)的变化结果如下:| 序号 | 时间/min | 0 | 10 | 20 | 30 | 40 | 60 |
| ① | 温度T1 / 1号Cu2O | 0.0500 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | 温度T1 / 2号Cu2O | 0.0500 | 0.0490 | 0.0483 | 0.0480 | 0.0480 | 0.0480 |
| ③ | 温度T2 / 2号Cu2O | 0.0500 | 0.0480 | 0.0470 | 0.0470 | 0.0470 | 0.0470 |
下列说法
| A.实验①前20 min的平均反应速率v(O2) = 7×10ˉ5 mol/( L·min) |
| B.实验①、②条件下的平衡常数相等,且小于实验③条件下的平衡常数 |
| C.2号Cu2O的催化效率比1号Cu2O的催化效率高 |
| D.实验时的温度T2高于T1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】25℃条件下研究溶液的酸碱性对反应X(aq)→2Y(aq)的影响,各物质浓度c随反应时间t的变化曲线如图,下列说法正确的是
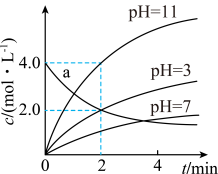
A. 时,反应不能发生 时,反应不能发生 |
| B.H+与OH-相比,H+使反应活化能更低 |
C.a曲线表示 时X的浓度随t的变化 时X的浓度随t的变化 |
D.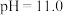 时, 时, 内, 内, |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是()


A.该反应的化学方程式为3A+2D 3B+4C 3B+4C |
| B.反应进行到1s时,v(A)=v(B) |
| C.反应进行到5s时,B的平均反应速率为0.06mol/(L·s) |
| D.反应进行到5s时,v(A)=v(B)=v(C)=v(D) |
您最近一年使用:0次



