氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
(1)如图是N2(g)和H2(g)反应生成1molNH3(g)过程中能量变化示意图。请写出N2和H2反应的热化学方程式___ 。

已如化学键键能是形成或拆开1 mol化学键放出或吸收的能量,单位kJ/mol。若已知下表数据,试根据表中及图中数据计算N-H的键能____ kJ/mol(用含a、b的式子表示)
(2)用NH3催化还原NOx还可以消除氮氧化物的污染。
4NH3(g)+3O2(g)=2N2(g)+6H2O(g)△H1=-m kJ/mol①
N2(g)+O2(g)=2NO(g)△H2=-n kJ/mol②
用NH3还原NO至N2,则反应过程中的反应热△H3=___ kJ/mol(用含m、n的式子表示)。
(3)肼(N2H4)是一种可燃性液体,可作火箭燃料。在常温下,1 g肼在氧气中完全燃烧生成氮气,放出Q kJ的热量,写出N2H4燃烧热的热化学方程式____ 。
(1)如图是N2(g)和H2(g)反应生成1molNH3(g)过程中能量变化示意图。请写出N2和H2反应的热化学方程式

已如化学键键能是形成或拆开1 mol化学键放出或吸收的能量,单位kJ/mol。若已知下表数据,试根据表中及图中数据计算N-H的键能
| 化学键 | H-H | N N N |
| 键能/kJ/mol | a | b |
(2)用NH3催化还原NOx还可以消除氮氧化物的污染。
4NH3(g)+3O2(g)=2N2(g)+6H2O(g)△H1=-m kJ/mol①
N2(g)+O2(g)=2NO(g)△H2=-n kJ/mol②
用NH3还原NO至N2,则反应过程中的反应热△H3=
(3)肼(N2H4)是一种可燃性液体,可作火箭燃料。在常温下,1 g肼在氧气中完全燃烧生成氮气,放出Q kJ的热量,写出N2H4燃烧热的热化学方程式
更新时间:2020-11-12 18:20:44
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】已知下列热化学方程式:
①2H2(g)+O2(g)=2H2O(g) △H=-484kJ/mol,
②H2(g)+1/2O2(g)=H2O(l) △H=-285.8kJ/mol;
③C(s)+1/2O2(g)=CO(g) △H=-110.5kJ/moL;
④C(s)+O2(g)=CO2(g) △H=-393.5kJ/moL。
回答下列各问:
(1)36g水由气态变成等温度的液态水放出热量为_____ kJ。
(2)C的燃烧热△H=______ kJ/mol
(3)燃烧10gH2生成液态水,放出的热量为________ kJ。
(4)可以表示CO的燃烧热的热化学方程式为_________ 。
①2H2(g)+O2(g)=2H2O(g) △H=-484kJ/mol,
②H2(g)+1/2O2(g)=H2O(l) △H=-285.8kJ/mol;
③C(s)+1/2O2(g)=CO(g) △H=-110.5kJ/moL;
④C(s)+O2(g)=CO2(g) △H=-393.5kJ/moL。
回答下列各问:
(1)36g水由气态变成等温度的液态水放出热量为
(2)C的燃烧热△H=
(3)燃烧10gH2生成液态水,放出的热量为
(4)可以表示CO的燃烧热的热化学方程式为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】(1)工业制氢气的一个重要反应是:CO(g)+ H2O(g) = CO2(g) + H2(g)
已知25℃时:C(石墨) +O2 (g) = CO2(g) △H1 =-394 kJ·mol-1
C(石墨) +1/2O2 (g) = CO (g) △H2 =-111 kJ·mol-1
H2(g) +1/2O2 (g) = H2O(g) △H3=-242kJ·mol-1
试计算25℃时CO(g)+ H2O(g) = CO2(g) + H2(g)的反应热__________ kJ·mol-1。
(2)实验测得,5g甲醇(CH3OH)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式______________________ 。
已知25℃时:C(石墨) +O2 (g) = CO2(g) △H1 =-394 kJ·mol-1
C(石墨) +1/2O2 (g) = CO (g) △H2 =-111 kJ·mol-1
H2(g) +1/2O2 (g) = H2O(g) △H3=-242kJ·mol-1
试计算25℃时CO(g)+ H2O(g) = CO2(g) + H2(g)的反应热
(2)实验测得,5g甲醇(CH3OH)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】按要求回答下列问题:
(1)300℃,硅粉与HCl(g)反应生成1mol SiHCl3气体和H2(g) 时,放出225 kJ的热量。该反应的热化学方程式是_____________________ 。
(2)已知:CuCl2(s)=CuCl(s) + Cl2(g) ΔH1=+83 kJ/mol
Cl2(g) ΔH1=+83 kJ/mol
CuCl(s) + O2(g)=CuO(s) +
O2(g)=CuO(s) +  Cl2(g) ΔH2=-20 kJ/mol
Cl2(g) ΔH2=-20 kJ/mol
CuO(s) + 2HCl(g) = CuCl2(s) + H2O(g) ΔH3=-121 kJ/mol
则:4HCl(g) + O2(g) = 2Cl2(g) + 2H2O(g)的ΔH=_________ kJ/mol。
又知:
推算:断开1 mol H-O键与断开1 mol H-Cl键所需能量相差_______ kJ。
(1)300℃,硅粉与HCl(g)反应生成1mol SiHCl3气体和H2(g) 时,放出225 kJ的热量。该反应的热化学方程式是
(2)已知:CuCl2(s)=CuCl(s) +
 Cl2(g) ΔH1=+83 kJ/mol
Cl2(g) ΔH1=+83 kJ/molCuCl(s) +
 O2(g)=CuO(s) +
O2(g)=CuO(s) +  Cl2(g) ΔH2=-20 kJ/mol
Cl2(g) ΔH2=-20 kJ/molCuO(s) + 2HCl(g) = CuCl2(s) + H2O(g) ΔH3=-121 kJ/mol
则:4HCl(g) + O2(g) = 2Cl2(g) + 2H2O(g)的ΔH=
又知:

推算:断开1 mol H-O键与断开1 mol H-Cl键所需能量相差
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】在微生物作用的条件下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
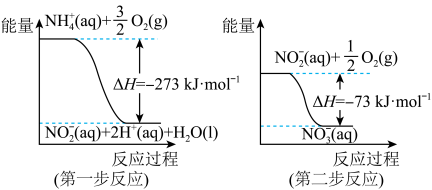
(1)第一步反应是___________ (填“放热”或“吸热”)反应,判断依据是___________ 。
(2)1molNH (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是___________ 。
(3)在0℃、101kPa时,44.8LH2在足量O2中完全燃烧生成H2O(l)放出571.6kJ的热量,则表示H2燃烧热的热化学方程式为___________ 。
(4)把煤作为燃料可通过下列两种途径:
途径Ⅰ:C(s)+O2(g)=CO2(g)ΔH1
途径Ⅱ:先制成水煤气:C(s)+H2O(g)=CO(g) +H2(g)ΔH2
再燃烧水煤气:2CO(g)+O2(g)=2CO2(g)ΔH3
2H2(g)+O2(g)=2H2O(g)ΔH4
则ΔH2=___________ (用ΔH1、ΔH3、ΔH4表示) 。
 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
(1)第一步反应是
(2)1molNH
 (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是(3)在0℃、101kPa时,44.8LH2在足量O2中完全燃烧生成H2O(l)放出571.6kJ的热量,则表示H2燃烧热的热化学方程式为
(4)把煤作为燃料可通过下列两种途径:
途径Ⅰ:C(s)+O2(g)=CO2(g)ΔH1
途径Ⅱ:先制成水煤气:C(s)+H2O(g)=CO(g) +H2(g)ΔH2
再燃烧水煤气:2CO(g)+O2(g)=2CO2(g)ΔH3
2H2(g)+O2(g)=2H2O(g)ΔH4
则ΔH2=
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】按要求写出相关内容
(1)已知:C(s)+O2(g)=CO2(g) △H= -393.5 kJ/mol
CO(g)+ O2(g)=CO2(g) △H= -283 kJ/mol
O2(g)=CO2(g) △H= -283 kJ/mol
则1 mol C(s)与O2(g)反应生成CO(g)放出的热量为_______ ,反应的热化学方程式为:_______ 。
(2)1 L 1 mol/LH2SO4溶液与2 L 1 mol/LNaOH溶液完全反应,放出114.6 kJ的热量,表示该中和热的热化学方程式为_______ 。
(1)已知:C(s)+O2(g)=CO2(g) △H= -393.5 kJ/mol
CO(g)+
 O2(g)=CO2(g) △H= -283 kJ/mol
O2(g)=CO2(g) △H= -283 kJ/mol则1 mol C(s)与O2(g)反应生成CO(g)放出的热量为
(2)1 L 1 mol/LH2SO4溶液与2 L 1 mol/LNaOH溶液完全反应,放出114.6 kJ的热量,表示该中和热的热化学方程式为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)工业上用H2和Cl2反应制HCl,各键能数据为:H-H:436kJ/mol,Cl-Cl:243kJ/mol,H-Cl:431kJ/mol。该反应的热化学方程式是__ 。
(2)已知25℃、101kPa时:
①2SO2(g)+O2(g) 2SO3(g) ΔH1=-197kJ·mol-1
2SO3(g) ΔH1=-197kJ·mol-1
②H2O(g)=H2O(l) ΔH2=-44kJ·mol-1
③2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) ΔH3=-545kJ·mol-1
则SO3(g)与H2O(l)反应的热化学方程式为____ 。
(3)CCS技术是将工业和有关能源产业中所产生的CO2进行捕捉与封存的技术,被认为是拯救地球、应对全球气候变化最重要的手段之一。其中一种以天然气为燃料的“燃烧前捕获系统”的简单流程图如图所示(部分条件及物质未标出)。

CH4在催化剂作用下实现第一步,也叫CH4不完全燃烧,1gCH4不完全燃烧反应放出2.21kJ热量,写出该反应的热化学方程式___ 。
(4)红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如下图所示(中的ΔH表示生成1mol产物的数据)。

根据上图回答下列问题:
①P和Cl2反应生成PCl3的热化学方程式是_____ 。
②PCl5(g)=PCl3(g)+Cl2(g) ΔH2=_____
③P和Cl2分两步反应生成1molPCl5的ΔH3=__
(1)工业上用H2和Cl2反应制HCl,各键能数据为:H-H:436kJ/mol,Cl-Cl:243kJ/mol,H-Cl:431kJ/mol。该反应的热化学方程式是
(2)已知25℃、101kPa时:
①2SO2(g)+O2(g)
 2SO3(g) ΔH1=-197kJ·mol-1
2SO3(g) ΔH1=-197kJ·mol-1②H2O(g)=H2O(l) ΔH2=-44kJ·mol-1
③2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) ΔH3=-545kJ·mol-1
则SO3(g)与H2O(l)反应的热化学方程式为
(3)CCS技术是将工业和有关能源产业中所产生的CO2进行捕捉与封存的技术,被认为是拯救地球、应对全球气候变化最重要的手段之一。其中一种以天然气为燃料的“燃烧前捕获系统”的简单流程图如图所示(部分条件及物质未标出)。

CH4在催化剂作用下实现第一步,也叫CH4不完全燃烧,1gCH4不完全燃烧反应放出2.21kJ热量,写出该反应的热化学方程式
(4)红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如下图所示(中的ΔH表示生成1mol产物的数据)。

根据上图回答下列问题:
①P和Cl2反应生成PCl3的热化学方程式是
②PCl5(g)=PCl3(g)+Cl2(g) ΔH2=
③P和Cl2分两步反应生成1molPCl5的ΔH3=
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】运用化学反应原理的有关知识回答下列问题:
(1)晶体硅在氧气中燃烧的热化学方程式为Si(s)+O2(g)=SiO2(s)△H=-989.2 kJ·mol-1,有关键能数据如下表:
则X的值为_________ 。
(2)加热N2O5,依次发生的分解反应为①N2O5 N2O3+O2,②N2O3
N2O3+O2,②N2O3 N2O+O2,在1 L密闭容器中充入4 mol N2O5,加热到t ℃,达到平衡状态后O2的平衡浓度为4.5 mol/L,N2O3的平衡浓度为1.7 mol/L,则t℃时反应①的平衡常数为
N2O+O2,在1 L密闭容器中充入4 mol N2O5,加热到t ℃,达到平衡状态后O2的平衡浓度为4.5 mol/L,N2O3的平衡浓度为1.7 mol/L,则t℃时反应①的平衡常数为_________ 。
(1)晶体硅在氧气中燃烧的热化学方程式为Si(s)+O2(g)=SiO2(s)△H=-989.2 kJ·mol-1,有关键能数据如下表:
| 化学键 | Si-O | O=O | Si-Si |
| 键能kJ·mol-1 | X | 498.8 | 176 |
(2)加热N2O5,依次发生的分解反应为①N2O5
 N2O3+O2,②N2O3
N2O3+O2,②N2O3 N2O+O2,在1 L密闭容器中充入4 mol N2O5,加热到t ℃,达到平衡状态后O2的平衡浓度为4.5 mol/L,N2O3的平衡浓度为1.7 mol/L,则t℃时反应①的平衡常数为
N2O+O2,在1 L密闭容器中充入4 mol N2O5,加热到t ℃,达到平衡状态后O2的平衡浓度为4.5 mol/L,N2O3的平衡浓度为1.7 mol/L,则t℃时反应①的平衡常数为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】甲醇是人们开发和利用的一种新能源。已知:
①2H2(g)+O2(g)=2H2O(l) ΔH1=-571.8 kJ/mol;
②CH3OH(l)+ O2(g)=CO2(g)+2H2(g) ΔH2=-192.9 kJ/mol
O2(g)=CO2(g)+2H2(g) ΔH2=-192.9 kJ/mol
(1)表示甲醇完全燃烧热的的热化学方程式为________________ ;
(2)反应②中的能量变化如图所示,则ΔH2=__________ 。(用E1、E2的相关式子表示);

(3)捕碳技术(主要指捕获CO2在降低温室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下反应:
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g) (NH4)2CO3(aq) △H1
(NH4)2CO3(aq) △H1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g) NH4HCO3(aq) △H2
NH4HCO3(aq) △H2
反应Ⅲ: (NH4)2CO3(aq)+H2O(l)+CO2(g) 2NH4HCO3(aq) △H3
2NH4HCO3(aq) △H3
则ΔH3与ΔH1 、ΔH2与之间的关系为ΔH3 =_________ ;
(4)拆开1mol气态物质中某种共价键需要吸收的能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量:
已知反应N2(g)+3H2(g) 2NH3(g) ΔH=akJ/mol,试根据表中所列键能数据估算a的值
2NH3(g) ΔH=akJ/mol,试根据表中所列键能数据估算a的值______ 。(注明“+”或“﹣”)。
①2H2(g)+O2(g)=2H2O(l) ΔH1=-571.8 kJ/mol;
②CH3OH(l)+
 O2(g)=CO2(g)+2H2(g) ΔH2=-192.9 kJ/mol
O2(g)=CO2(g)+2H2(g) ΔH2=-192.9 kJ/mol(1)表示甲醇完全燃烧热的的热化学方程式为
(2)反应②中的能量变化如图所示,则ΔH2=

(3)捕碳技术(主要指捕获CO2在降低温室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下反应:
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)
 (NH4)2CO3(aq) △H1
(NH4)2CO3(aq) △H1反应Ⅱ:NH3(l)+H2O(l)+CO2(g)
 NH4HCO3(aq) △H2
NH4HCO3(aq) △H2反应Ⅲ: (NH4)2CO3(aq)+H2O(l)+CO2(g)
 2NH4HCO3(aq) △H3
2NH4HCO3(aq) △H3则ΔH3与ΔH1 、ΔH2与之间的关系为ΔH3 =
(4)拆开1mol气态物质中某种共价键需要吸收的能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量:
| 化学键 | H﹣H | N﹣H | N≡N |
| 键能/kJ/mol | 436 | 391 | 945 |
已知反应N2(g)+3H2(g)
 2NH3(g) ΔH=akJ/mol,试根据表中所列键能数据估算a的值
2NH3(g) ΔH=akJ/mol,试根据表中所列键能数据估算a的值
您最近一年使用:0次
【推荐3】(1)反应2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl中,氧化产物是___________ ,氧化剂和还原剂的物质的量之比为___________ ,依据氧化还原反应规律判断,氧化性强弱为NaClO3___________ Cl2(填>、<或=)。
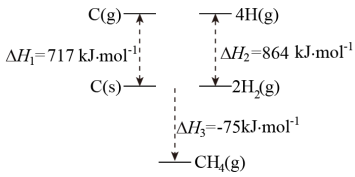
(2)根据下图中的能量关系,可求得C-H键的键能___________ kJ/mol。
(3)已知:
I. CO(g) + 2H2(g) =CH 3OH(l) △H= −128.6 kJ/mol
II.2CO(g) + O2(g) =2 CO2(g) △H=−566.0 kJ/mol
III.2H2(g) + O2(g) =2 H2O(l) △H=−571.6 kJ/mol
写出 CH3OH燃烧热的热化学方程式:___________ 。
(2)根据下图中的能量关系,可求得C-H键的键能

(3)已知:
I. CO(g) + 2H2(g) =CH 3OH(l) △H= −128.6 kJ/mol
II.2CO(g) + O2(g) =2 CO2(g) △H=−566.0 kJ/mol
III.2H2(g) + O2(g) =2 H2O(l) △H=−571.6 kJ/mol
写出 CH3OH燃烧热的热化学方程式:
您最近一年使用:0次



