在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命。下表是500 mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
成分 | 质量(g) | 摩尔质量(g·mol-1) |
蔗糖 | 25.0 | 342 |
硫酸钾 | 0.3 | 174 |
阿司匹林 | 0.2 | 180 |
高锰酸钾 | 0.4 | 158 |
硝酸银 | 0.1 | 170 |
(1)下列“鲜花保鲜剂”的成分中,属于非电解质的是
A.乙醇 B.硫酸钾 C.高锰酸钾 D.硝酸银
在上述物质中任选一种,写出其电离方程式
(2)“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度(注意:只要求用原始数据写表达式,不需要化简与计算)
(3)配制上述“鲜花保鲜剂”所需的仪器有:烧杯、托盘天平、药匙
(4)下列有关容量瓶使用方法的操作中,错误的是
A.使用容量瓶前应该检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加入蒸馏水到接近刻度线2~3cm处,用滴管滴加蒸馏水到刻度线。
D.盖好瓶塞,食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复上下颠倒摇匀。
(5)若在最后的定容过程中不小心多加了几滴,该如何处理?
(6)若溶液配制过程遇到下列情况,溶液的浓度将(填“偏高”、“偏低”或“不变”)。
①容量瓶在使用前未干燥,里面有少量蒸馏水
②忘记将洗涤液转入容量瓶
③定容时仰视容量瓶刻度线
④定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
相似题推荐
| 成分 | 质量(g) | 摩尔质量(g/mol) |
| 蔗糖 | 50.00 | 342 |
| 硫酸钾 | 0.87 | 174 |
| 阿司匹林 | 0.35 | 180 |
| 高锰酸钾 | 0.158 | 158 |
| 硝酸银 | 0.04 | 170 |
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.硝酸
(2)在溶液配制过程中,下列操作正确且对配制结果没有影响的是
A.将药品放入容量瓶中加蒸馏水溶解
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(3)配制上述500mL“鲜花保鲜剂”所需的玻璃仪器有:烧杯、玻璃棒、
(4)鲜花保鲜剂中K+(蔗糖、阿司匹林中不含K+) 的物质的量浓度为
(1)15.6gNa2X含Na+的物质的量为0.4mol,则Na2X的摩尔质量为
(2)除去Na2CO3粉末中混入的NaHCO3杂质用
(3)Cl2和SO2都有漂白作用,现将二者以等物质的量混合后再通入品红溶液中,品红溶液将
(4)明矾在水中的电离方程式是
(5)利用下图装置,写出除去下列气体中的杂质的方法(括号内的气体为杂质),并写出化学方程式。
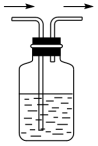
①NO(NO2):
②CO2(SO2):
 溶液回答下列问题,现有下列仪器:
溶液回答下列问题,现有下列仪器:A.烧杯 B.100mL量筒 C.药匙 D.玻璃棒 E.天平
(1)配制时还缺少的仪器是
(2)应用托盘天平称取十水碳酸钠晶体的质量为
(3)若实验遇下列情况,溶液的浓度偏低的是_______。
| A.溶解后没有冷却即进行定容 |
| B.定容时仰视容量瓶的标线 |
| C.容量瓶内壁附有水珠而未干燥处理 |
| D.向容量瓶中转移溶液时溶液流到容量瓶外面 |
| 编号 | 实验操作 | 实验数据 |
| A | 测量下面实验过程中温度的变化 | 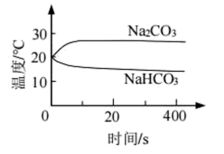 |
| B | 测量下面实验过程中溶液pH的变化 注:Na2CO3溶液和NaHCO3溶液的浓度相等 | 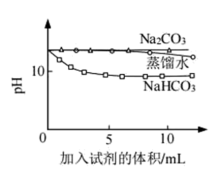 |
①实验A中,溶解时吸收热量的物质是
②实验B中,OH-未参与该反应的实验证据是
③实验B中,滴加NaHCO3溶液的烧杯中溶液pH的变化与滴加Na2CO3溶液的pH有明显差异,写出反应初期的离子方程式:
(1)NaNO2
(2)实验操作如表所示,请完善表格中的实验现象和结论(已知I2遇淀粉变蓝)。
| 实验 | 实验操作及现象或结果 | 结论 |
| 1 | 取5 mL NaNO2溶液于试管中,加入少量KI溶液,充分反应后,再滴加淀粉溶液,溶液变蓝 | NaNO2具有① |
| 2 | 取2 mL KMnO4溶液(先酸化好)于试管中,滴加足量的NaNO2溶液,可观察到的实验现象为② | NaNO2具有还原性 |
| 3 | NaNO2固体与70%硫酸反应生成了NO和NO2两种气体 | NaNO2具有③ |
⑤通过上述实验可知,NaNO2、KMnO4、I2的氧化性由强到弱的顺序为
 ②氨水 ③次磷酸(H3PO2) ④酒精 ⑤铝丝 ⑥过氧化钠 ⑦氧化钙 ⑧苏打。根据要求,回答下列问题:
②氨水 ③次磷酸(H3PO2) ④酒精 ⑤铝丝 ⑥过氧化钠 ⑦氧化钙 ⑧苏打。根据要求,回答下列问题:(1)以上物质属于电解质的是
(2)物质⑧的电离方程式为
(3)将少量⑦投入⑧的稀溶液中可能会出现的实验现象为
(4)在工业上次磷酸(H3PO2)常用于化学镀银,发生的反应如下:
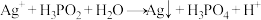
①配平该方程式,并用单线桥表示该反应的电子转移:
②
 中,P元素的化合价为
中,P元素的化合价为③该反应中,表现氧化性与表现还原性的微粒物质的量之比为
④若改用适量氯气恰好将
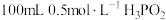 氧化为
氧化为 ,则最终得到的溶液中
,则最终得到的溶液中 的物质的量浓度为
的物质的量浓度为 )。
)。


已知
 极易溶液于水,1体积水可溶液解700体积
极易溶液于水,1体积水可溶液解700体积 。
。(1)
 中,属于非电解质的物质是
中,属于非电解质的物质是(2)合成氨厂所用的氮气可通过蒸馏空气得到。下图是实验室普通蒸馏装置:

 仪器的名称是
仪器的名称是指出装置中两处错误:一是冷凝水应下进上出,另一处是
(3)沉淀池中通常是把氯化钠与两种气体之一配成溶液,再通入过量的另一种气体,后通入的气体是
(4)母液中可提取的主要副产品是
(5)写出煅烧炉中反应的化学方程式
I.小曹同学准备用NaOH固体配制240mL
 的NaOH溶液。
的NaOH溶液。(1)本实验必须用到的玻璃仪器有:量筒、胶头滴管、烧杯、
(2)要配制出此溶液,小曹同学应称出
(3)在配制过程中,小曹同学的其他操作都是正确的,但下列操作中会引起所配制溶液浓度偏高的一项是___________(填字母)。
| A.NaOH固体在称量前已部分变质 |
| B.有少量NaOH溶液残留在烧杯里 |
| C.定容时,俯视容量瓶的刻度线 |
| D.定容摇匀后,发现溶液凹液面最低处时低于刻度线,用胶头滴管补水至刻度线 |
Ⅱ.配制完成NaOH溶液后,小曹同学准备利用下述装置和配制好的NaOH溶液、铁屑、稀硫酸等试剂制取Fe(OH)2沉淀
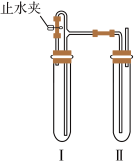
(4)试管I中加入的试剂是
(5)小曹同学分别在试管I和Ⅱ中加入试剂,然后迅速打开止水夹,塞紧塞子后检验试管Ⅱ出口处排出的氢气的纯度。当排出的H2纯净时,再夹紧止水夹,此后试管Ⅱ中可以较长时间看到Fe(OH)2白色沉淀,其原因是
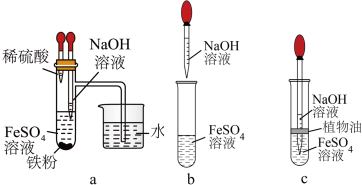
(6)如果Ⅱ中空气未排净,则Fe(OH)2白色沉淀将被氧化为Fe(OH)3,请写出该过程化学方程式
(1)该溶液中NaOH的物质的量浓度为
(3)从该溶液中取出10mL,其中含NaOH的质量为
(4)将取出的10mL溶液加水稀释到100mL,稀释后溶液中NaOH的物质的量浓度为
(5)若将配置的100mlNaOH溶液用稀硫酸进行中和时,消耗稀硫酸的体积为200ml,则该稀硫酸溶液的物质的量浓度为
(1)现要用此回收酸配制上述萃取液,40mL回收酸液经稀释可以得到4mol·L-1的氢氟酸的体积为
(2)在40mL回收酸中加入
| 葡萄糖注射液说明书 |
【名称】 葡萄糖注射液 葡萄糖注射液【主要成分】本品主要成分为葡萄糖,分子式  ,相对分子质量180 ,相对分子质量180【性状】本品为无色或几乎为无色的透明液体 【规格】每  含葡萄糖 含葡萄糖 |
(1)该注射液中葡萄糖的物质的量浓度是
(2)现需要配制
 的葡萄糖溶液,下图所示的仪器中肯定不需要的是
的葡萄糖溶液,下图所示的仪器中肯定不需要的是
(3)配制
 的葡萄糖溶液的步骤有:①称量②计算③摇匀④溶解⑤待溶液恢复到室温⑥洗涤⑦定容⑧转移
的葡萄糖溶液的步骤有:①称量②计算③摇匀④溶解⑤待溶液恢复到室温⑥洗涤⑦定容⑧转移正确的操作顺序为
②→①→④→___________→___________→___________→___________→___________→③;
其中“定容”的具体操作为:沿着玻璃棒缓缓地将蒸馏水注入容量瓶中,直到容量瓶中的液面距离容量瓶的刻度线
 时,改用胶头滴管滴加蒸馏水至
时,改用胶头滴管滴加蒸馏水至(4)下列操作会使所配制的溶液物质的量浓度偏低的是___________(填标号)。
| A.容量瓶洗涤后未烘干 |
| B.转移溶液后,未洗涤烧杯和玻璃棒 |
| C.定容时俯视刻度线 |
| D.定容时加水超过刻度线,把溶液吸出至刻度线 |
 溶液。以下操作1~5是其配制过程及示意图:
溶液。以下操作1~5是其配制过程及示意图: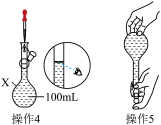
操作1:准确称取一定质量的胆矾晶体用适量蒸馏水溶解。
操作2:将所得溶液转移到仪器X中,用蒸馏水冲洗烧杯和玻璃棒2~3次,将洗涤液也转移到X中。
操作3:继续向X中加手液面离X的刻度线1~2cm处。
①仪器X的名称是
②关于该配制过程?下列说法正确的是
A.操作1中,应称取胆矾晶体的质量为2.5g
B.操作2中,洗涤液不需要转移到仪器X中
C.操作4称为定容,由于该同学观察方法不正确,将导致所配溶液浓度偏低
D.操作5摇匀后静置,发现液面低于刻度线,应继续加水至凹液面与刻度线相切
Ⅰ.配制0.50 mol·L-1 NaOH溶液
(1)若实验中大约要使用245 mL NaOH溶液,至少需要称量NaOH固体
(2)从下表中选择,称量NaOH固体所需要的仪器是(填字母)
| 名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 |  |  |  |  |  |  |
| 序号 | a | b | c | d | e | f |
Ⅱ.测定稀硫酸和稀氢氧化钠溶液中和热的实验装置如图所示。

(1)若生成1 mol H2O时反应放出的热量为57.3 kJ,写出该反应的热化学方程式:
(2)取50 mL NaOH溶液和30 mL硫酸进行实验,实验数据如下表。
①请填写下表中的空白:
| 温度 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差平均值(t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②用上述实验数值计算结果为
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度



