Ⅰ.(1)用20gNaOH配成250mL溶液,它的物质的量浓度为 ______  取出5mL该溶液,它的物质的量浓度为
取出5mL该溶液,它的物质的量浓度为 ______ ,再加水稀释至100mL,则稀释后溶液的物质的量浓度为 ______
(2)现有14.4gCO和 的混合气体,在标准状况下其体积为8.96L。
的混合气体,在标准状况下其体积为8.96L。
①该混合气体的平均摩尔质量为____ 。
②混合气体中碳原子的个数为____ (用 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。
Ⅱ.已知NaHSO4晶体易溶于水,它溶于水时,电离出三种不同的离子,电离方程式为 NaHSO4=Na++H++ ,因此 NaHSO4 溶液显酸性。但 NaHSO4受热熔化时却只能电离出两种不同离子。
,因此 NaHSO4 溶液显酸性。但 NaHSO4受热熔化时却只能电离出两种不同离子。
(1)NaHSO4在熔融状态下的电离方程式是_________ 。
(2)下列说法中正确的是_________ (填字母)。
A.NaHSO4属于酸
B.NaHSO4属于氢化物
C.NaHSO4晶体属于电解质
D.NaHSO4溶液能与Zn反应生成氢气
(3)向一定量的Ba(OH)2溶液中,逐滴加入NaHSO4溶液,直至不再生成沉淀,该过程中发生反应的离子方程式为____________ ,沉淀完全后,继续滴加NaHSO4溶液,此时发生反应的离子方程式为____________ 。
(4)NaHSO4和NaHCO3中都含有氢元素,但将二者同时加入水中,可以发生化学反应,该反应的离子方程式为____________________ .
 取出5mL该溶液,它的物质的量浓度为
取出5mL该溶液,它的物质的量浓度为 (2)现有14.4gCO和
 的混合气体,在标准状况下其体积为8.96L。
的混合气体,在标准状况下其体积为8.96L。①该混合气体的平均摩尔质量为
②混合气体中碳原子的个数为
 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。Ⅱ.已知NaHSO4晶体易溶于水,它溶于水时,电离出三种不同的离子,电离方程式为 NaHSO4=Na++H++
 ,因此 NaHSO4 溶液显酸性。但 NaHSO4受热熔化时却只能电离出两种不同离子。
,因此 NaHSO4 溶液显酸性。但 NaHSO4受热熔化时却只能电离出两种不同离子。(1)NaHSO4在熔融状态下的电离方程式是
(2)下列说法中正确的是
A.NaHSO4属于酸
B.NaHSO4属于氢化物
C.NaHSO4晶体属于电解质
D.NaHSO4溶液能与Zn反应生成氢气
(3)向一定量的Ba(OH)2溶液中,逐滴加入NaHSO4溶液,直至不再生成沉淀,该过程中发生反应的离子方程式为
(4)NaHSO4和NaHCO3中都含有氢元素,但将二者同时加入水中,可以发生化学反应,该反应的离子方程式为
更新时间:2020-12-06 15:39:15
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】完成下列填空:
(1)0.3molNH3分子中所含原子数与___ 个H2O分子中所含原子数相等。
(2)在一定的温度和压强下,1体积气体X2跟3体积气体Y2刚好化合生成2体积气体A,则A的化学式可表示为___ 。
(3)在同温同压同体积的条件下,H2与气体B的质量之比是1:8,则B的摩尔质量为___ 。
(4)在25℃、101kPa的条件下,同质量的CH4和气体C的体积之比是15:8,则C的摩尔质量为___ 。
(5)在两个相同容积的密闭容器D、E中,分别充入相同质量的X气体和CO气体,D和E中的压强之比是7:16,则X的摩尔质量为___ 。
(6)物质的量浓度相同的NaCl、MgCl2、AlCl3,溶液中Cl-的物质的量浓度之比为___ ;体积相同的、物质的量浓度之比为1:2:3的NaCl、MgCl2、AlCl3三种溶液中Cl-的物质的量之比为___ 。
(1)0.3molNH3分子中所含原子数与
(2)在一定的温度和压强下,1体积气体X2跟3体积气体Y2刚好化合生成2体积气体A,则A的化学式可表示为
(3)在同温同压同体积的条件下,H2与气体B的质量之比是1:8,则B的摩尔质量为
(4)在25℃、101kPa的条件下,同质量的CH4和气体C的体积之比是15:8,则C的摩尔质量为
(5)在两个相同容积的密闭容器D、E中,分别充入相同质量的X气体和CO气体,D和E中的压强之比是7:16,则X的摩尔质量为
(6)物质的量浓度相同的NaCl、MgCl2、AlCl3,溶液中Cl-的物质的量浓度之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】化学计量在化学中占有重要地位。请回答下列问题:
(1)2019年1月21日13时42分,我国在酒泉卫星发射中心用长征十一号运载火箭成功发射了三颗卫星。长征系列运载火箭的燃料之一是肼( )。回答下列问题:
)。回答下列问题:
①肼的摩尔质量是_______ 。
②16g肼中含有氮原子的数目为_______ 。
③肼在氧气中燃烧生成 和
和 ,一定质量的肼燃烧后生成
,一定质量的肼燃烧后生成 和
和 的物质的量之比是
的物质的量之比是_______ 。每生成标准状况下44.8L的氮气,需要消耗肼的质量为_______ 。
(2)22.2g某二价金属氯化物(ACl2)中含有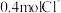 ,则A的相对原子质量是
,则A的相对原子质量是_______ ;ACl2的化学式是_______ 。
(3)在0.2L由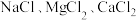 组成的混合液中,部分离子浓度大小如图所示。
组成的混合液中,部分离子浓度大小如图所示。
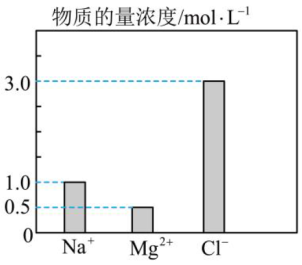
①该混合液中 的物质的量为
的物质的量为_______ mol,将该混合液加水稀释至体积为1L,稀释后溶液中 的物质的量浓度为
的物质的量浓度为_______ mol/L。
②向该稀释后的溶液中加入足量硝酸酸化的硝酸银溶液,可得到沉淀_______ mol。
(4)如图所示,气缸的总体积一定,内部被活塞隔成Ⅰ、Ⅱ两部分,活塞可以自由移动,也可以固定。0℃时向Ⅰ中充入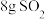 ,Ⅱ中充入
,Ⅱ中充入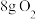 ,则当活塞不再移动时,Ⅰ、Ⅱ两部分体积比为
,则当活塞不再移动时,Ⅰ、Ⅱ两部分体积比为_______ 。

(1)2019年1月21日13时42分,我国在酒泉卫星发射中心用长征十一号运载火箭成功发射了三颗卫星。长征系列运载火箭的燃料之一是肼(
 )。回答下列问题:
)。回答下列问题:①肼的摩尔质量是
②16g肼中含有氮原子的数目为
③肼在氧气中燃烧生成
 和
和 ,一定质量的肼燃烧后生成
,一定质量的肼燃烧后生成 和
和 的物质的量之比是
的物质的量之比是(2)22.2g某二价金属氯化物(ACl2)中含有
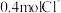 ,则A的相对原子质量是
,则A的相对原子质量是(3)在0.2L由
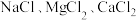 组成的混合液中,部分离子浓度大小如图所示。
组成的混合液中,部分离子浓度大小如图所示。
①该混合液中
 的物质的量为
的物质的量为 的物质的量浓度为
的物质的量浓度为②向该稀释后的溶液中加入足量硝酸酸化的硝酸银溶液,可得到沉淀
(4)如图所示,气缸的总体积一定,内部被活塞隔成Ⅰ、Ⅱ两部分,活塞可以自由移动,也可以固定。0℃时向Ⅰ中充入
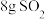 ,Ⅱ中充入
,Ⅱ中充入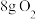 ,则当活塞不再移动时,Ⅰ、Ⅱ两部分体积比为
,则当活塞不再移动时,Ⅰ、Ⅱ两部分体积比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题
(1)在标准状况下,测得 某气体的体积为
某气体的体积为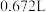 ,该气体的摩尔质量为
,该气体的摩尔质量为_______ 。
(2)将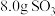 溶于水配成
溶于水配成 溶液,则所得溶液的物质的量浓度为
溶液,则所得溶液的物质的量浓度为_______ 。
(3) 溶液和
溶液和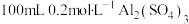 溶液混合后(混合体积变化忽略不计),溶液中
溶液混合后(混合体积变化忽略不计),溶液中 的物质的量浓度为
的物质的量浓度为_______ 。
(4)设 为阿伏加德罗常数的数值,如果
为阿伏加德罗常数的数值,如果 氧气中含有的分子数为b,则
氧气中含有的分子数为b,则 氧气在标准状况下的体积约是
氧气在标准状况下的体积约是_______ (用含 的式子表示)
的式子表示)
(5)标准状况下,将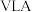 气体(摩尔质量为
气体(摩尔质量为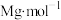 )全部溶于
)全部溶于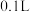 水(水的密度为
水(水的密度为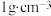 )中(假设气体与水不反应),所得溶液的密度为
)中(假设气体与水不反应),所得溶液的密度为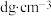 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为_______ 。
(6)某盐混合溶液中含有离子: ,测得
,测得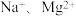 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: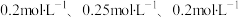 ,则
,则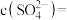
_______ 。
(1)在标准状况下,测得
 某气体的体积为
某气体的体积为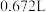 ,该气体的摩尔质量为
,该气体的摩尔质量为(2)将
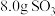 溶于水配成
溶于水配成 溶液,则所得溶液的物质的量浓度为
溶液,则所得溶液的物质的量浓度为(3)
 溶液和
溶液和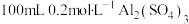 溶液混合后(混合体积变化忽略不计),溶液中
溶液混合后(混合体积变化忽略不计),溶液中 的物质的量浓度为
的物质的量浓度为(4)设
 为阿伏加德罗常数的数值,如果
为阿伏加德罗常数的数值,如果 氧气中含有的分子数为b,则
氧气中含有的分子数为b,则 氧气在标准状况下的体积约是
氧气在标准状况下的体积约是 的式子表示)
的式子表示)(5)标准状况下,将
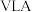 气体(摩尔质量为
气体(摩尔质量为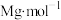 )全部溶于
)全部溶于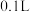 水(水的密度为
水(水的密度为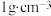 )中(假设气体与水不反应),所得溶液的密度为
)中(假设气体与水不反应),所得溶液的密度为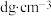 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为(6)某盐混合溶液中含有离子:
 ,测得
,测得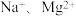 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: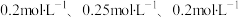 ,则
,则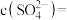
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】一定质量的铜粉恰好完全溶解于 一定浓度的硝酸中,得到
一定浓度的硝酸中,得到 和
和 的混合气体
的混合气体 (标准状况),将这些气体与
(标准状况),将这些气体与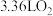 (标准状况)混合后通入
(标准状况)混合后通入 溶液,所有气体被完全吸收生成硝酸钠。计算:
溶液,所有气体被完全吸收生成硝酸钠。计算:
(1)溶解的铜粉质量是_______ g
(2)混合气体中 与
与 的物质的量之比为
的物质的量之比为_______ 。
(3)硝酸的物质的量浓度为_______ mol/L。
 一定浓度的硝酸中,得到
一定浓度的硝酸中,得到 和
和 的混合气体
的混合气体 (标准状况),将这些气体与
(标准状况),将这些气体与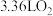 (标准状况)混合后通入
(标准状况)混合后通入 溶液,所有气体被完全吸收生成硝酸钠。计算:
溶液,所有气体被完全吸收生成硝酸钠。计算:(1)溶解的铜粉质量是
(2)混合气体中
 与
与 的物质的量之比为
的物质的量之比为(3)硝酸的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氨氮废水中的氮元素多以NH4+和NH3·H2O的形式存在。某工厂处理氨氮废水的流程如下:
(1)过程Ⅰ:加NaOH溶液,调节pH至11后,并鼓入大量空气。用离子方程式表示加NaOH溶液的作用是______________ ;用化学平衡理论解释鼓入大置空气的目的__________________ 。
(2) II中加入适量NaClO溶液,控制pH在3~4,将NH4+转化为无毒物质。则反应的离子方程式是__________________ 。
(3)分别称取2.39 g (NH4)2SO4和NH4Cl固体混合物两份。
①将其中一份配成溶液,逐滴加入一定浓度的Ba(OH)2溶液,产生的沉淀质量与加入Ba(OH)2溶液体积的关系如图。混合物中n[(NH4)2SO4]:n(NH4Cl)为__________ 。
②另一份固体混合物中NH4+与Ba(OH)2溶液(浓度同上)恰好完全反应时,溶液中c(Cl-)=_______ (溶液体积变化忽略不计)。
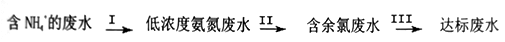
(1)过程Ⅰ:加NaOH溶液,调节pH至11后,并鼓入大量空气。用离子方程式表示加NaOH溶液的作用是
(2) II中加入适量NaClO溶液,控制pH在3~4,将NH4+转化为无毒物质。则反应的离子方程式是
(3)分别称取2.39 g (NH4)2SO4和NH4Cl固体混合物两份。
①将其中一份配成溶液,逐滴加入一定浓度的Ba(OH)2溶液,产生的沉淀质量与加入Ba(OH)2溶液体积的关系如图。混合物中n[(NH4)2SO4]:n(NH4Cl)为
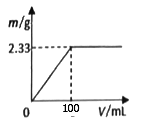
②另一份固体混合物中NH4+与Ba(OH)2溶液(浓度同上)恰好完全反应时,溶液中c(Cl-)=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】现有下列物质:①稀硫酸②小苏打③氨水④二氧化碳⑤FeCl3固体⑥稀NaOH溶液⑦硝酸亚铁溶液。
(1)上述物质中属于电解质的物质序号为______ 。
(2))有两种物质发生反应的离子方程式为:H++OH-=H2O,这两种物质的序号是______ 。
(3)加入盐酸、NaOH溶液均能发生化学反应的物质序号为______ 。
(4)能导电的物质序号为_______________ 。
(5)实验室用⑤制备胶体的化学方程式为__________________________________ 。
(1)上述物质中属于电解质的物质序号为
(2))有两种物质发生反应的离子方程式为:H++OH-=H2O,这两种物质的序号是
(3)加入盐酸、NaOH溶液均能发生化学反应的物质序号为
(4)能导电的物质序号为
(5)实验室用⑤制备胶体的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有下列10种物质:
①铜 ②熔融 ③
③ ④
④ ⑤
⑤ 晶体 ⑥胆矾 ⑦碳酸钙 ⑧
晶体 ⑥胆矾 ⑦碳酸钙 ⑧ ⑨氯化铁饱和溶液 ⑩酒精
⑨氯化铁饱和溶液 ⑩酒精
(1)上述物质中属于电解质的有___________ (填序号,下同),属于非电解质的有___________ ,能导电的有___________ 。
(2)⑧在熔化状态下电离方程式为___________ 。
(3)过量④通入③的溶液中,反应的离子方程式为___________ 。
(4)将⑨滴入沸水中,继续加热至液体呈___________ 色,得到氢氧化铁胶体,其分散质粒子直径范围是___________ ,用激光笔照射装有 胶体的烧杯,能在侧面看到一条光亮的“通路”,这种现象称为
胶体的烧杯,能在侧面看到一条光亮的“通路”,这种现象称为___________ 效应。
①铜 ②熔融
 ③
③ ④
④ ⑤
⑤ 晶体 ⑥胆矾 ⑦碳酸钙 ⑧
晶体 ⑥胆矾 ⑦碳酸钙 ⑧ ⑨氯化铁饱和溶液 ⑩酒精
⑨氯化铁饱和溶液 ⑩酒精(1)上述物质中属于电解质的有
(2)⑧在熔化状态下电离方程式为
(3)过量④通入③的溶液中,反应的离子方程式为
(4)将⑨滴入沸水中,继续加热至液体呈
 胶体的烧杯,能在侧面看到一条光亮的“通路”,这种现象称为
胶体的烧杯,能在侧面看到一条光亮的“通路”,这种现象称为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】现有以下物质: 氢氧化钡
氢氧化钡 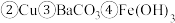 胶体
胶体  酒精
酒精  稀硫酸
稀硫酸 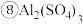
(1)以上物质中属于混合物的是___________  填序号,下空同
填序号,下空同 ,属于电解质的是
,属于电解质的是___________ ,属于非电解质的是___________ 能导电的是___________
(2)向 中逐滴滴加
中逐滴滴加 ,可观察到的现象
,可观察到的现象___________ 。
(3)写出物质 在水中的电离方程式:
在水中的电离方程式:___________ 。
(4)写出物质 和
和 反应的离子方程式
反应的离子方程式___________ 。
(5)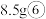 约含有
约含有 ___________ 个分子,含___________ mol质子。
(6)将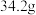 ⑧溶于水配成100mL溶液,从该溶液中取出10mL,其中
⑧溶于水配成100mL溶液,从该溶液中取出10mL,其中 的物质的量浓度为
的物质的量浓度为___________ 。
 氢氧化钡
氢氧化钡 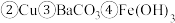 胶体
胶体  酒精
酒精  稀硫酸
稀硫酸 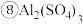
(1)以上物质中属于混合物的是
 填序号,下空同
填序号,下空同 ,属于电解质的是
,属于电解质的是(2)向
 中逐滴滴加
中逐滴滴加 ,可观察到的现象
,可观察到的现象(3)写出物质
 在水中的电离方程式:
在水中的电离方程式:(4)写出物质
 和
和 反应的离子方程式
反应的离子方程式(5)
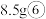 约含有
约含有 (6)将
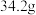 ⑧溶于水配成100mL溶液,从该溶液中取出10mL,其中
⑧溶于水配成100mL溶液,从该溶液中取出10mL,其中 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】水是生命之源,保护水资源人人有责。
Ⅰ.高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法是:在强碱性条件下,NaClO溶液和FeCl3溶液反应生成高铁酸钠和氯化钠。
(1)高铁酸钠中铁元素的化合价为_______ 。
(2)反应中高铁酸钠是_______ 产物(填“氧化”或“还原”)。
(3)写出制备高铁酸钠的离子方程式_______ 。
(4)使用氯气对自来水消毒时,氯气与水中的有机物反应生成对人体有害的物质,人们开始使用新的自来水消毒剂,如氯元素的某种氧化物,写出这种新消毒剂的名称_______ 。
Ⅱ.工业酸性废水中含有的重铬酸根离子(Cr2O )有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)作处理剂,将Cr2O
)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)作处理剂,将Cr2O 转化为Cr3+。
转化为Cr3+。
(5)绿矾是结晶水合物,风化是指在室温和干燥的空气里,结晶水合物失去结晶水的现象,则风化属于_______ 变化(填“物理”或“化学”)。
(6)在溶液中Cr2O 存在反应:Cr2O
存在反应:Cr2O +H2O⇌2CrO
+H2O⇌2CrO +2H+,该反应
+2H+,该反应_______ 氧化还原反应(填“属于”或“不属于”)。
(7)写出处理工业酸性废水时发生反应的离子方程式_______ 。
Ⅰ.高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法是:在强碱性条件下,NaClO溶液和FeCl3溶液反应生成高铁酸钠和氯化钠。
(1)高铁酸钠中铁元素的化合价为
(2)反应中高铁酸钠是
(3)写出制备高铁酸钠的离子方程式
(4)使用氯气对自来水消毒时,氯气与水中的有机物反应生成对人体有害的物质,人们开始使用新的自来水消毒剂,如氯元素的某种氧化物,写出这种新消毒剂的名称
Ⅱ.工业酸性废水中含有的重铬酸根离子(Cr2O
 )有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)作处理剂,将Cr2O
)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)作处理剂,将Cr2O 转化为Cr3+。
转化为Cr3+。(5)绿矾是结晶水合物,风化是指在室温和干燥的空气里,结晶水合物失去结晶水的现象,则风化属于
(6)在溶液中Cr2O
 存在反应:Cr2O
存在反应:Cr2O +H2O⇌2CrO
+H2O⇌2CrO +2H+,该反应
+2H+,该反应(7)写出处理工业酸性废水时发生反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】写出下列反应的离子方程式:
(1)Zn和稀H2SO4反应:______________________________________ 。
(2)CaCO3与稀HCl反应:__________________________________ 。
(3)CH3COOH与NaOH溶液的中和反应:_____________________ 。
(4)Ba(OH)2与CuSO4溶液反应:_____________________________ 。
(1)Zn和稀H2SO4反应:
(2)CaCO3与稀HCl反应:
(3)CH3COOH与NaOH溶液的中和反应:
(4)Ba(OH)2与CuSO4溶液反应:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求完成下列内容
(1)请写出下列反应的化学方程式。
①Na2SO3和较浓H2SO4制取SO2气体:_______
②足量氨水中通入SO2气体:_______
③Cu与浓H2SO4加热条件下反应:_______
(2)一定条件下, 和氟气可发生如下反应:
和氟气可发生如下反应: ,从而可知在
,从而可知在 中,元素R的化合价是
中,元素R的化合价是_______ 。
(3)实验室用氯酸钾和浓盐酸制取氯气,配平下列方程式_______ _______KClO3+_______HCl=_______Cl2↑+_______KCl+_______H2O
(4)①配平该反应的化学方程式:_______ ______FeSO4+_______KNO3+_______H2SO4=_______K2SO4+_______Fe2(SO4)3+_______NO↑+_______H2O。
②该反应中氧化产物是_______ (填化学式);当15.2 g FeSO4恰好完全反应时,转移电子的物质的量为_______ 。
(1)请写出下列反应的化学方程式。
①Na2SO3和较浓H2SO4制取SO2气体:
②足量氨水中通入SO2气体:
③Cu与浓H2SO4加热条件下反应:
(2)一定条件下,
 和氟气可发生如下反应:
和氟气可发生如下反应: ,从而可知在
,从而可知在 中,元素R的化合价是
中,元素R的化合价是(3)实验室用氯酸钾和浓盐酸制取氯气,配平下列方程式
(4)①配平该反应的化学方程式:
②该反应中氧化产物是
您最近一年使用:0次

 表示阿伏加德罗常数。则:
表示阿伏加德罗常数。则: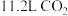 的质量为
的质量为 ,用双线桥表示该反应
,用双线桥表示该反应 的
的 参与反应,转移
参与反应,转移 溶液,需要
溶液,需要
 个X气体分子的质量是
个X气体分子的质量是 。则X气体的摩尔质量是
。则X气体的摩尔质量是

