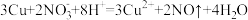标准状况下,将a LSO2和Cl2组成的混合气体通入100mL0.1mol·L-1Fe2(SO4)3溶液中,充分反应后,溶液的棕黄色变浅。向反应后的溶液中加入足量的BaCl2溶液,将所得沉淀过滤、洗涤、干燥后称重,其质量为11.65g。则下列关于该过程的推断正确的是
| A.所得沉淀为0.03mol的BaSO4 | B.混合气体中Cl2的体积为0.448L |
| C.混合气体的体积可能为0.8L | D.a的取值范围为 0.224<a<0.672 |
更新时间:2017-05-23 10:35:01
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】取含Cr2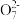 的模拟水样若干份,在不同pH条件下,分别向每个水样中加一定量的FeSO4或NaHSO3固体,充分反应后再滴加碱液生成Cr(OH)3沉淀,从而测定除铬率,实验结果如图所示。下列说法不正确的是
的模拟水样若干份,在不同pH条件下,分别向每个水样中加一定量的FeSO4或NaHSO3固体,充分反应后再滴加碱液生成Cr(OH)3沉淀,从而测定除铬率,实验结果如图所示。下列说法不正确的是

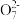 的模拟水样若干份,在不同pH条件下,分别向每个水样中加一定量的FeSO4或NaHSO3固体,充分反应后再滴加碱液生成Cr(OH)3沉淀,从而测定除铬率,实验结果如图所示。下列说法不正确的是
的模拟水样若干份,在不同pH条件下,分别向每个水样中加一定量的FeSO4或NaHSO3固体,充分反应后再滴加碱液生成Cr(OH)3沉淀,从而测定除铬率,实验结果如图所示。下列说法不正确的是 
| A.当+6价铬足量且pH大于7时,等质量的FeSO4的除铬量比NaHSO3高 |
| B.若选用NaHSO3处理含铬污水时,不能将污水的酸性调节的过强 |
| C.pH>8,FeSO4的除铬率下降与废水中溶解氧参与反应有关 |
| D.选择FeSO4做处理剂更有利于Cr(OH)3的沉降及分离 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】有下列三个反应①3Cl2+2FeI2=2FeCl3+2I2②2Fe2++Br2=2Fe3++2Br-③2Fe3++2I-=2Fe2++I2,下列说法正确的是
| A.①中氧化产物和还原产物的质量之比为1:1 |
| B.根据以上方程式可以得到氧化性强弱顺序:Cl2>Fe3+>Br2>Fe2+ |
| C.根据以上方程式一定可推知:Br2+2I-=2Br-+I2 |
| D.根据反应①②一定可以推理得到Cl2+FeBr2=FeCl2+Br2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】 “绿色化学实验”进课堂,某化学教师为“氯气与金属钠反应”设计了如下装置与操作以替代相关的课本实验.实验操作:钠与氯气反应的装置可作如图改进,将一根玻璃管与氯气发生器相连,玻璃管内放一块黄豆粒大的金属钠(已吸净煤油),玻璃管尾部塞一团浸有NaOH溶液的棉花球。先给钠预热,到钠熔融成圆球时,撤火,通入氯气,即可见钠着火燃烧,生成大量白烟。以下叙述错误的是


| A.反应生成的大量白烟是氯化钠晶体 |
| B.玻璃管尾部塞一团浸有NaOH溶液的棉球是用于吸收过量的氯气,以免其污染空气 |
| C.钠着火燃烧产生苍白色火焰 |
| D.若在棉球外沿滴一滴紫色石蕊溶液,可根据其颜色变化判断氯气是否被碱液完全吸收 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】将一定量的氯气通入氢氧化钠浓溶液中,加热一段时间后溶液中形成NaCl、NaClO、NaClO3的共存体系。下列判断不正确的是( )
| A.参加反应所需NaOH与氯气的物质的量之比一定为2:1 |
| B.反应体系中n(NaCl):n(NaClO):n(NaClO3)可能为11:1:2 |
| C.若有a mol 氯气参加反应,则a mol<转移电子的物质的量< 5a/3mol |
| D.反应中NaClO、NaClO3为氧化产物,且两者物质的量之比一定为1:1 |
您最近一年使用:0次

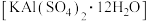 的水溶液中滴加
的水溶液中滴加 溶液至
溶液至 完全沉淀:
完全沉淀:

 溶解铜:
溶解铜: