碘单质与氢气在一定条件下反应的热化学方程式如下:
①I2(g)+H2(g)⇌2HI(g)△H =-9.48 kJ/mol
②I2(s)+H2(g)⇌2HI(g)△H=+26.48 kJ/mol
下列说法正确的是
①I2(g)+H2(g)⇌2HI(g)△H =-9.48 kJ/mol
②I2(s)+H2(g)⇌2HI(g)△H=+26.48 kJ/mol
下列说法正确的是
| A.该条件下,1 molH2(g)和足量I2(g)充分反应,放出热量9.48 kJ |
| B.该条件下,碘升华的热化学方程式为I2(s)⇌I2(g)△H=+35.96 kJ/mol |
| C.相同条件下,Cl2(g)+H2(g)⇌2HCl(g)的△H>-9.48 kJ/mol |
| D.反应①是放热反应,所以反应①的活化能大于反应②的活化能 |
20-21高三上·浙江·期中 查看更多[2]
更新时间:2020-12-11 09:36:29
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列关于热化学方程式说法正确的是
A.甲烷的燃烧热为 ,表示甲烷燃烧热的热化学方程式为 ,表示甲烷燃烧热的热化学方程式为  |
B.  ,则金刚石比石墨稳定 ,则金刚石比石墨稳定 |
C.  ,则稀 ,则稀 溶液和浓 溶液和浓 完全反应生成 完全反应生成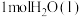 时,放出 时,放出 的热量 的热量 |
D.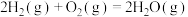  , ,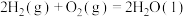  ,则 ,则 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知下列两个热化学方程式
2H2(g)+O2(g)=2H2O(l);ΔH=-571.6kJ/mol
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l);ΔH=-2220kJ/mol
实验测得氢气和丙烷的混合气体共2mol,完全燃烧时放出热量2505.8kJ,则混合气体中氢气和丙烷的体积比约为
2H2(g)+O2(g)=2H2O(l);ΔH=-571.6kJ/mol
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l);ΔH=-2220kJ/mol
实验测得氢气和丙烷的混合气体共2mol,完全燃烧时放出热量2505.8kJ,则混合气体中氢气和丙烷的体积比约为
| A.1:3 | B.1:4 | C.1:1 | D.3:1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列设备工作时,可以实现化学能转化为电能的是( )
| A | B | C | D |
| 太阳能集热器 | 锂离子电池 | 电饭煲 | |
 |  |  |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐2】我国科学家使用新型催化剂实现了电催化合成氨,该反应有远端加氢和交替加氢两种路径,反应路径如图所示,吸附在催化剂表面上的物种用*标注。下列有关说法正确的是


| A.产物从催化剂上脱附会释放能量 |
| B.该过程决速步骤的反应可表示为*NN+H→*NNH |
| C.该反应在电解池的阳极上发生 |
| D.电催化合成氨远端加氢反应路径更容易发生 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
| A.当反应体系放热时其焓减小,ΔH为负值 |
| B.化学键断裂的能量是化学变化中能量变化的主要原因 |
| C.一个化学反应,不管是一步完成的还是分几步完成的,其反应热是不相同的 |
| D.苛性钠固体溶于水属于放热反应 |
您最近一年使用:0次
【推荐2】下列说法正确的是( )。
| A.吸热反应在任何条件下都不能发生 |
| B.Na转化为Na+时,吸收的能量就是该过程的反应热 |
| C.水蒸气变为液态水时,放出的能量就是该变化的反应热 |
| D.同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
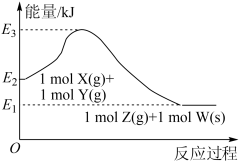
【推荐1】X(g)+Y(g) Z(g)+W(s)反应过程中能量变化如图,下列说法正确的是
Z(g)+W(s)反应过程中能量变化如图,下列说法正确的是
 Z(g)+W(s)反应过程中能量变化如图,下列说法正确的是
Z(g)+W(s)反应过程中能量变化如图,下列说法正确的是
| A.该反应正反应的活化能小于逆反应的活化能 |
| B.该反应的△H=(E2-E1)kJ·mol-1 |
| C.若加入催化剂,(E3-E2)的值不变 |
| D.高温下有利于该反应正向进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在催化剂表面,一种合成碳酸二甲酯的反应机理如图,下列说法错误的是
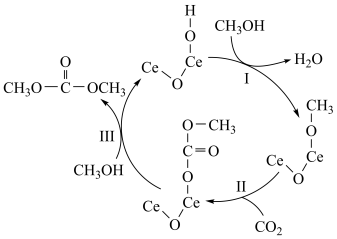
A.该反应总方程式为2CH3OH+CO2 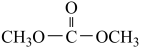 +H2O +H2O |
| B.该反应有利于碳中和和碳达峰 |
| C.反应Ⅲ为取代反应 |
D.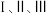 中均有 中均有 键的断裂 键的断裂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】已知:CH4(g)+ O2(g)=CH3OH(g) △H。CH4、O2和H2O(g)(H2O的作用是活化催化剂)按照一定体积比在催化剂表面合成甲醇反应的部分历程如下图所示(吸附在催化剂表面的物种用*标注,TS代表过渡态)。下列说法正确的是
O2(g)=CH3OH(g) △H。CH4、O2和H2O(g)(H2O的作用是活化催化剂)按照一定体积比在催化剂表面合成甲醇反应的部分历程如下图所示(吸附在催化剂表面的物种用*标注,TS代表过渡态)。下列说法正确的是

 O2(g)=CH3OH(g) △H。CH4、O2和H2O(g)(H2O的作用是活化催化剂)按照一定体积比在催化剂表面合成甲醇反应的部分历程如下图所示(吸附在催化剂表面的物种用*标注,TS代表过渡态)。下列说法正确的是
O2(g)=CH3OH(g) △H。CH4、O2和H2O(g)(H2O的作用是活化催化剂)按照一定体积比在催化剂表面合成甲醇反应的部分历程如下图所示(吸附在催化剂表面的物种用*标注,TS代表过渡态)。下列说法正确的是
| A.该反应的△H=-32.51kJ/mol |
| B.在催化剂表面上更容易被吸附的是O2 |
| C.该历程中正反应最大的活化能为21.22kJ/mol |
| D.决定反应速率步骤(慢反应)的化学方程式为:*CH4+*OH+*H=*CH3OH+2*H |
您最近一年使用:0次

 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g) (m-x)CeO2·xCe+xO2;(m-x)CeO2·xCe+xH2O+xCO2
(m-x)CeO2·xCe+xO2;(m-x)CeO2·xCe+xH2O+xCO2 mCeO2+xH2+xCO
mCeO2+xH2+xCO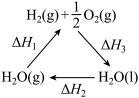
 O2(g)=H2O(g)的反应热大于ΔH3
O2(g)=H2O(g)的反应热大于ΔH3

