(1)含有相同数目氧原子的CO和CO2,其物质的量之比为_______ ,若将两者按此比例混合在一起,其平均摩尔质量为_______ g/mol(结果保留1位小数)
(2)等质量的SO2和SO3,其物质的量之比为_______ ,所含氧原子的个数之比为_______ 。
(3)现有100 ml,2 mol/L的NaCl溶液和200 ml,1 mol/L的Na2CO3溶液,其Na+的浓度之比_______ ,Na+的物质的量之比_______ 。
(2)等质量的SO2和SO3,其物质的量之比为
(3)现有100 ml,2 mol/L的NaCl溶液和200 ml,1 mol/L的Na2CO3溶液,其Na+的浓度之比
更新时间:2020-12-29 20:08:59
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】密闭容器中1 mol PCl3与1 mol Cl2反应制备PCl5(g),增加2NA个P-Cl键___
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】判断下列说法的正误。
1.常温常压下,22.4 L Cl2中含有的分子数为6.02×1023个。________
2.标准状况下,22.4 L N2和O2的混合气体中含有的分子数为NA。________
3.2.24 L CO2中含有的原子数为0.3NA。________
1.常温常压下,22.4 L Cl2中含有的分子数为6.02×1023个。
2.标准状况下,22.4 L N2和O2的混合气体中含有的分子数为NA。
3.2.24 L CO2中含有的原子数为0.3NA。
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐3】(1)为探究氯水中含有的部分粒子及某些粒子的性质,某化学兴趣小组做了如下实验:
①观察氯水颜色,发现氯水呈浅黄绿色,证明氯水中含有的粒子是________ 。
②向氯水中滴入碳酸钠溶液,有气体生成,说明氯水中含有的粒子是________ 。
③盛有氯水的试管中的有色布条褪色,说明氯水中含有的粒子是________ 。
④将紫色石蕊溶液滴入新制氯水中,溶液显红色,起作用的微粒是________ ,过一会儿,溶液的颜色褪去,起作用的微粒是________ 。
⑤向氯水中滴加AgNO3溶液有白色沉淀生成,证明氯水中含有的粒子是________ 。
⑥氯水经光照后,颜色逐渐消失,放出的无色气体是________ ,溶液的酸性________ (填“增强”“不变”或“减弱”)。
⑦将Cl2通入水中,所得溶液中具有氧化性的含氯微粒是________ 。
(2)某AB2气体,摩尔质量为M(g/mol),质量为m,NA为阿伏加德罗常数,则
①该气体在标准状况下体积为________ L;②该气体在标准状况下密度为________ g/L;
③该气体原子总数为________ ;④该气体一个分子质量为________ g。
①观察氯水颜色,发现氯水呈浅黄绿色,证明氯水中含有的粒子是
②向氯水中滴入碳酸钠溶液,有气体生成,说明氯水中含有的粒子是
③盛有氯水的试管中的有色布条褪色,说明氯水中含有的粒子是
④将紫色石蕊溶液滴入新制氯水中,溶液显红色,起作用的微粒是
⑤向氯水中滴加AgNO3溶液有白色沉淀生成,证明氯水中含有的粒子是
⑥氯水经光照后,颜色逐渐消失,放出的无色气体是
⑦将Cl2通入水中,所得溶液中具有氧化性的含氯微粒是
(2)某AB2气体,摩尔质量为M(g/mol),质量为m,NA为阿伏加德罗常数,则
①该气体在标准状况下体积为
③该气体原子总数为
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐1】CO和CO2是碳的两种重要氧化物。
(1)在标准状况下,5.6LCO的物质的量是___________ ,质量是___________ 。
(2)11gCO2的体积是___________ (标准状况)。
(3)相同质量的CO和CO2所含的原子个数比是___________ 。
(1)在标准状况下,5.6LCO的物质的量是
(2)11gCO2的体积是
(3)相同质量的CO和CO2所含的原子个数比是
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】回答下列问题:
(1)3.011023 个CH4 中,含_______ mol 氢原子,_______ mol 电子。
(2)等质量的O2 和O3 ,它们的物质的量之比为_______ ,所含原子数之比为_______ 。
(3)6.02 1023 个CO2 与_______ gSO2 含有的氧原子数相等。
现有以下 8 种物质:①熔融状态的NaCl 、② SO2 、③ Na2CO3 、④铜、⑤ BaCO3 、⑥酒精、⑦稀H2SO4 、⑧ FeCl3 溶液。
(4)上述物质中,属于电解质的是_______ 。(填序号)
(5)上述状态下可导电的是_______ 。(填序号)
(6)写出③与足量⑦反应的离子方程式:_______ 。
(1)3.011023 个CH4 中,含
(2)等质量的O2 和O3 ,它们的物质的量之比为
(3)6.02 1023 个CO2 与
现有以下 8 种物质:①熔融状态的NaCl 、② SO2 、③ Na2CO3 、④铜、⑤ BaCO3 、⑥酒精、⑦稀H2SO4 、⑧ FeCl3 溶液。
(4)上述物质中,属于电解质的是
(5)上述状态下可导电的是
(6)写出③与足量⑦反应的离子方程式:
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】下列说法是否正确(正确的打“√”,不正确的打“×”)若不正确请说明理由。
(1)元素周期表中每一横行称为一周期,每一纵列称为一个族。_________ ;
(2)FeCl3与Cu的反应为置换反应。_________ ;
(3)1 mol Na2O溶于水中形成1 L溶液,所得溶液的物质的量浓度为1 mol/L。_________ ;
(4)镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料。_________
(1)元素周期表中每一横行称为一周期,每一纵列称为一个族。
(2)FeCl3与Cu的反应为置换反应。
(3)1 mol Na2O溶于水中形成1 L溶液,所得溶液的物质的量浓度为1 mol/L。
(4)镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料。
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】回答下列问题:
(1)含1.0molFe3+的Fe2(SO4)3中所含SO 的物质的量是
的物质的量是______ 。
(2)等质量的N2、NH3、NO2、Cl2四种气体中,在相同温度和压强下,体积最大的是______ 。
(3)某混合溶液中含有Na+、Al3+、Cl-、SO ,测得Na+、Al3+和Cl-的物质的量浓度比为3∶2∶1,则Al3+与SO
,测得Na+、Al3+和Cl-的物质的量浓度比为3∶2∶1,则Al3+与SO 的微粒个数比为
的微粒个数比为______ 。
(4)实验室常用KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O制取少量氯气。若转移电子数目为NA,则产生Cl2的体积为______ (标准状况),被氧化的HCl的物质的量为______ 。
(5)黑火药是我国古代四大发明之一,其化学反应方程式为:S+2KNO3+3C=K2S+3CO2↑+N2↑。
①上述反应所涉及到的物质中属于非电解质的是_____ 。
②上述反应中被氧化的元素是_____ (填元素符号);氧化剂是______ (填化学式)。
③收集上述反应生成的气体0.4mol,通入100mL4mol•L-1的氢氧化钠溶液中,最终所得溶液中的溶质是______ (填化学式)。
(6)我国古代常用绿矾FeSO4•7H2O来制备硫酸,若将绿矾投入到稀硝酸中,发生反应的离子方程式为______ 。
(1)含1.0molFe3+的Fe2(SO4)3中所含SO
 的物质的量是
的物质的量是(2)等质量的N2、NH3、NO2、Cl2四种气体中,在相同温度和压强下,体积最大的是
(3)某混合溶液中含有Na+、Al3+、Cl-、SO
 ,测得Na+、Al3+和Cl-的物质的量浓度比为3∶2∶1,则Al3+与SO
,测得Na+、Al3+和Cl-的物质的量浓度比为3∶2∶1,则Al3+与SO 的微粒个数比为
的微粒个数比为(4)实验室常用KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O制取少量氯气。若转移电子数目为NA,则产生Cl2的体积为
(5)黑火药是我国古代四大发明之一,其化学反应方程式为:S+2KNO3+3C=K2S+3CO2↑+N2↑。
①上述反应所涉及到的物质中属于非电解质的是
②上述反应中被氧化的元素是
③收集上述反应生成的气体0.4mol,通入100mL4mol•L-1的氢氧化钠溶液中,最终所得溶液中的溶质是
(6)我国古代常用绿矾FeSO4•7H2O来制备硫酸,若将绿矾投入到稀硝酸中,发生反应的离子方程式为
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐1】按要求填空
(1)标准状况下,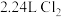 的质量为
的质量为______ ;有______ 个氯原子。
(2)含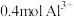 的
的 中所含的
中所含的 的物质的量是
的物质的量是______ 。
(3)阻燃剂碱式碳酸铝镁中 与
与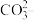 质量之比为51:300,则这两种离子的物质的量之比为
质量之比为51:300,则这两种离子的物质的量之比为______ 。
(4)质量相同的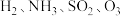 四种气体中,含有分子数目最少的是
四种气体中,含有分子数目最少的是______ 。
(5)标准状况下, 与标准状况下
与标准状况下______ 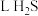 含有相同数目的氢原子。
含有相同数目的氢原子。
(6) 中氧原子的数百为
中氧原子的数百为 ,则元素R的相对原子质量为
,则元素R的相对原子质量为______ ,R元素名称是______ 。
(7)已知CO、 混合气体的质量共
混合气体的质量共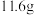 ,在标准状况下的体积为
,在标准状况下的体积为 ,则混合气体中CO的质量为
,则混合气体中CO的质量为______ ﹔ 在相同状况下的体积为
在相同状况下的体积为______ 。
(8)由 和
和 的组成的混合气体,在标况下的密度是
的组成的混合气体,在标况下的密度是 的14.5倍。则该混合气体中
的14.5倍。则该混合气体中 和
和 的体积比为
的体积比为______ 。
(1)标准状况下,
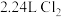 的质量为
的质量为(2)含
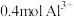 的
的 中所含的
中所含的 的物质的量是
的物质的量是(3)阻燃剂碱式碳酸铝镁中
 与
与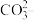 质量之比为51:300,则这两种离子的物质的量之比为
质量之比为51:300,则这两种离子的物质的量之比为(4)质量相同的
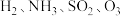 四种气体中,含有分子数目最少的是
四种气体中,含有分子数目最少的是(5)标准状况下,
 与标准状况下
与标准状况下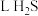 含有相同数目的氢原子。
含有相同数目的氢原子。(6)
 中氧原子的数百为
中氧原子的数百为 ,则元素R的相对原子质量为
,则元素R的相对原子质量为(7)已知CO、
 混合气体的质量共
混合气体的质量共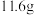 ,在标准状况下的体积为
,在标准状况下的体积为 ,则混合气体中CO的质量为
,则混合气体中CO的质量为 在相同状况下的体积为
在相同状况下的体积为(8)由
 和
和 的组成的混合气体,在标况下的密度是
的组成的混合气体,在标况下的密度是 的14.5倍。则该混合气体中
的14.5倍。则该混合气体中 和
和 的体积比为
的体积比为
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】2023年9月23日晚,第19届杭州亚运会开幕式上主火炬被引燃,火炬采用的燃料是甲醇( ),是通过
),是通过 加氢得到的。一种
加氢得到的。一种 的“捕捉”和转化过程如下:在高压时将烟道气中
的“捕捉”和转化过程如下:在高压时将烟道气中 溶解于甲醇(
溶解于甲醇( ),得到二氧化碳的甲醇溶液;用“捕捉”到的二氧化碳与氢气在一定条件下生产甲醇,同时生成水。
),得到二氧化碳的甲醇溶液;用“捕捉”到的二氧化碳与氢气在一定条件下生产甲醇,同时生成水。
(1)常温常压下,用等质量的a. b.
b. c.
c. d.
d. 四种气体分别吹出四个气球,气球体积由大到小排列的顺序是
四种气体分别吹出四个气球,气球体积由大到小排列的顺序是___________ (填序号,假设气球的材质相同)。
(2)下列说法错误的是___________。
(3)每生产1吨这种甲醇,可以消耗___________ 吨 。
。
(4)甲醇燃烧的火焰接近无色,而亚运会火炬的火焰颜色是亮黄色的,很可能是添加了含 和
和___________ (填写离子符号)的盐类。
 ),是通过
),是通过 加氢得到的。一种
加氢得到的。一种 的“捕捉”和转化过程如下:在高压时将烟道气中
的“捕捉”和转化过程如下:在高压时将烟道气中 溶解于甲醇(
溶解于甲醇( ),得到二氧化碳的甲醇溶液;用“捕捉”到的二氧化碳与氢气在一定条件下生产甲醇,同时生成水。
),得到二氧化碳的甲醇溶液;用“捕捉”到的二氧化碳与氢气在一定条件下生产甲醇,同时生成水。(1)常温常压下,用等质量的a.
 b.
b. c.
c. d.
d. 四种气体分别吹出四个气球,气球体积由大到小排列的顺序是
四种气体分别吹出四个气球,气球体积由大到小排列的顺序是(2)下列说法错误的是___________。
| A.整个过程有助于减少温室气体排放 |
| B.二氧化碳的甲醇溶液,溶剂是甲醇 |
| C.转化过程中的“一定条件”可能需要合适的催化剂 |
D.转化过程中发生反应的化学方程式: |
 。
。(4)甲醇燃烧的火焰接近无色,而亚运会火炬的火焰颜色是亮黄色的,很可能是添加了含
 和
和
您最近半年使用:0次



