2015年8月12日天津港的爆炸事故中,有700t氰化钠放在现场。NaCN为白色结晶颗粒(或粉末),熔点为563.7℃,沸点为1496℃,易溶于水,易水解,有剧毒。回答下列问题:
(1)含NaCN的废液_____ (填“能”或“不能”)直接排放。
(2)处理含CN-废水的方法之一是在微生物的作用下,CN-被氧气氧化成 ,同时生成NH3,则NaCN中C元素的化合价为
,同时生成NH3,则NaCN中C元素的化合价为_____ ,该反应的离子方程式为_____ 。
(3)常温下,氰化钠能与双氧水反应,生成小苏打和某种碱性气体,大大降低其毒性,该反应中氧化剂为_____ ,化学方程式为_____ 。
(1)含NaCN的废液
(2)处理含CN-废水的方法之一是在微生物的作用下,CN-被氧气氧化成
 ,同时生成NH3,则NaCN中C元素的化合价为
,同时生成NH3,则NaCN中C元素的化合价为(3)常温下,氰化钠能与双氧水反应,生成小苏打和某种碱性气体,大大降低其毒性,该反应中氧化剂为
更新时间:2020-12-29 20:09:05
|
相似题推荐
【推荐1】高铁酸钾(K2FeO4)是一种新型绿色消毒剂,其在消毒(发生氧化还原反应)后可形成Fe(OH)3胶体,常用于处理饮用水。工业上有干法与湿法两种制备高铁酸钾的方法。
(1)干法制备高铁酸钾时,先制备得到Na2FeO4,反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中,氧化剂是_______ ,氧化产物是_______ 。
(2)配平湿法制备高铁酸钾反应的离子方程式并用单线桥表示出电子转移的方向和数目:_____ 。
_______Fe(OH)3+_______ClO−+_______OH−=_______ +_______Cl−+_______H2O。
+_______Cl−+_______H2O。
(3)取少量K2FeO4溶液,滴加盐酸,有Cl2产生,该反应表明氧化性:K2FeO4_______ (填“>”或“<”)Cl2。
(1)干法制备高铁酸钾时,先制备得到Na2FeO4,反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中,氧化剂是
(2)配平湿法制备高铁酸钾反应的离子方程式并用单线桥表示出电子转移的方向和数目:
_______Fe(OH)3+_______ClO−+_______OH−=_______
 +_______Cl−+_______H2O。
+_______Cl−+_______H2O。(3)取少量K2FeO4溶液,滴加盐酸,有Cl2产生,该反应表明氧化性:K2FeO4
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.阅读下面一段材料并回答问题。
(1) 中铁元素的化合价为
中铁元素的化合价为___________ 。
(2)制备 需要在
需要在________ (填“酸性”、“碱性”或“中性”)环境中进行。
(3)下列关于 的说法中,不正确的是
的说法中,不正确的是________
a.是强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
Ⅱ.如图是以铁屑为原料制备 的工艺流程图:
的工艺流程图:

请回答下列问题:
(4)流程图中的吸收剂X为________(填字母)。
(5)氧化剂Y为漂白液的有效成分;反应④的化学方程式中氧化剂与还原剂的物质的量之比为______ 。
(6)写出反应⑤的化学方程式________ 。
| 高铁酸钾使用说明书 【化学式】  【性状】暗紫色具有金属光泽的粉末,无臭无味 【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着  减小,稳定性下降,与水反应放出氧气, 减小,稳定性下降,与水反应放出氧气, 通过强烈的氧化作用可迅速杀灭细菌有消毒作用,同时不会产生有害物质。 通过强烈的氧化作用可迅速杀灭细菌有消毒作用,同时不会产生有害物质。 与水反应还能产生具有强吸附性的 与水反应还能产生具有强吸附性的 胶体,可除去水中细微的悬浮物,有净水作用 胶体,可除去水中细微的悬浮物,有净水作用【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理 【用量】消毒净化  水投放: 水投放: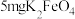 ,即可达到卫生标准 ,即可达到卫生标准 |
(1)
 中铁元素的化合价为
中铁元素的化合价为(2)制备
 需要在
需要在(3)下列关于
 的说法中,不正确的是
的说法中,不正确的是a.是强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
Ⅱ.如图是以铁屑为原料制备
 的工艺流程图:
的工艺流程图:
请回答下列问题:
(4)流程图中的吸收剂X为________(填字母)。
A. 溶液 溶液 | B. 粉 粉 | C. 溶液 溶液 | D. 溶液 溶液 |
(5)氧化剂Y为漂白液的有效成分;反应④的化学方程式中氧化剂与还原剂的物质的量之比为
(6)写出反应⑤的化学方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,具有强氧化性,无二次污染。湿法制备高铁酸钾(K2FeO4)的反应体系中有六种数粒:Fe(OH)3、ClO-、OH-、FeO 、Cl-、H2O。
、Cl-、H2O。
(1)写出并配平湿法制高铁酸钾的离子反应方程式:___ 。
(2)每生成1molFeO 转移
转移___ mol电子,若反应过程中转移了0.3mol电子,则还原产物的物质的量为___ mol。
(3)氧化性:FeO
___ ClO-(填“>”或“<”)。
(4)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力(转移的电子数)相当于多少克Cl2的氧化能力。NaClO的有效氯含量为___ ?
(5)实际在水处理过程中,K2FeO4中的铁元素转化为Fe(OH)3胶体,使水中悬浮物聚沉,如何通过实验证明生成了Fe(OH)3胶体___ ?
 、Cl-、H2O。
、Cl-、H2O。(1)写出并配平湿法制高铁酸钾的离子反应方程式:
(2)每生成1molFeO
 转移
转移(3)氧化性:FeO

(4)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力(转移的电子数)相当于多少克Cl2的氧化能力。NaClO的有效氯含量为
(5)实际在水处理过程中,K2FeO4中的铁元素转化为Fe(OH)3胶体,使水中悬浮物聚沉,如何通过实验证明生成了Fe(OH)3胶体
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】过氧化氢(分子结构为H—O—O—H)俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。根据下列反应回答问题:
A.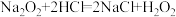
B.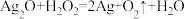
C.
D.
E.4H2O2+ +2H+=2CrO5+5H2O(CrO5分子结构为
+2H+=2CrO5+5H2O(CrO5分子结构为 )
)
(1)A反应属于四种基本反应类型中的___________ (填化学反应名称)。
(2)上述反应中,H2O2仅体现还原性的是___________ (填字母序号,下同),H2O2既体现氧化性又体现还原性的反应是___________ ;
(3)E反应___________ (填“是”、“不是”)氧化还原反应,你的判断理由是___________ 。
(4)配平下列足量的酸性高锰酸钾溶液与过氧化氢溶液反应的离子方程式,并用单线桥法标出反应中电子转移的方向和数目:___________ 。
 +H2O2+_________—Mn2++O2↑+__________
+H2O2+_________—Mn2++O2↑+__________
(5)将黄色、微溶的NaBiO3固体加入MnSO4和H2SO4的混合溶液里并加热,最后溶液显紫色(Bi3+无色)。写出该反应的离子方程式:___________ 。
A.
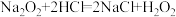
B.
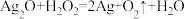
C.

D.

E.4H2O2+
 +2H+=2CrO5+5H2O(CrO5分子结构为
+2H+=2CrO5+5H2O(CrO5分子结构为 )
)(1)A反应属于四种基本反应类型中的
(2)上述反应中,H2O2仅体现还原性的是
(3)E反应
(4)配平下列足量的酸性高锰酸钾溶液与过氧化氢溶液反应的离子方程式,并用单线桥法标出反应中电子转移的方向和数目:
 +H2O2+_________—Mn2++O2↑+__________
+H2O2+_________—Mn2++O2↑+__________(5)将黄色、微溶的NaBiO3固体加入MnSO4和H2SO4的混合溶液里并加热,最后溶液显紫色(Bi3+无色)。写出该反应的离子方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应)。生成物中含有Cl-、ClO-、ClO 三种含氯元素的离子,其中ClO-、ClO
三种含氯元素的离子,其中ClO-、ClO 两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
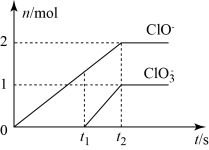
(1)t1时刻之前发生的反应是:___________
(2)t2时,Ca(OH)2与Cl2发生反应的总化学方程式为10Ca(OH)2+10Cl2=2Ca(ClO)2+Ca(ClO3)2+7CaCl2+10H2O,则该石灰乳中含有Ca(OH)2的物质的量是___________ mol。
(3)据分析,生成Ca(ClO3)2的反应是由温度升高引起的,通入Cl2的速度不同,ClO-和ClO 的比例也不同。若在原石灰乳中通入氯气的速度加快,则反应后
的比例也不同。若在原石灰乳中通入氯气的速度加快,则反应后
___________ 2(填“>”、“<”或“=”);氯酸钙(Ca(ClO3)2)为有毒化学品,其粉尘对呼吸道、眼及皮肤有刺激性,吸入氯酸钙粉尘,会因积累在体内而引起中毒。为了防止使用漂白粉时出现意外,制备漂白粉时可以采取的措施___________ (写一条即可)。
(4)请配平化学方程式:KClO3+HCl--KCl+Cl2↑+H2O___________ 。若反应过程中转移2mol e-,则生成标准状况下Cl2的体积为___________ L。
Ⅱ.有下列三个在溶液中发生的氧化还原反应:
①3FeCl3+2KI=2FeCl2+2KCl+I2;
②2FeCl2+Cl2=2FeCl3;
③K2Cr2O7+14HCl=2KCl+2CrCl3+7H2O+3Cl2↑
请根据上述反应分析推断后回答下列问题:
(5)FeCl3、I2、Cl2、K2Cr2O7的氧化性由强到弱依次是___________ 。
(6)在酸性溶液中存在大量的I-,则Cr2O 、Fe3+、Fe2+、Cl-中能与I-大量共存的离子是
、Fe3+、Fe2+、Cl-中能与I-大量共存的离子是___________ 。
 三种含氯元素的离子,其中ClO-、ClO
三种含氯元素的离子,其中ClO-、ClO 两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
(1)t1时刻之前发生的反应是:
(2)t2时,Ca(OH)2与Cl2发生反应的总化学方程式为10Ca(OH)2+10Cl2=2Ca(ClO)2+Ca(ClO3)2+7CaCl2+10H2O,则该石灰乳中含有Ca(OH)2的物质的量是
(3)据分析,生成Ca(ClO3)2的反应是由温度升高引起的,通入Cl2的速度不同,ClO-和ClO
 的比例也不同。若在原石灰乳中通入氯气的速度加快,则反应后
的比例也不同。若在原石灰乳中通入氯气的速度加快,则反应后
(4)请配平化学方程式:KClO3+HCl--KCl+Cl2↑+H2O
Ⅱ.有下列三个在溶液中发生的氧化还原反应:
①3FeCl3+2KI=2FeCl2+2KCl+I2;
②2FeCl2+Cl2=2FeCl3;
③K2Cr2O7+14HCl=2KCl+2CrCl3+7H2O+3Cl2↑
请根据上述反应分析推断后回答下列问题:
(5)FeCl3、I2、Cl2、K2Cr2O7的氧化性由强到弱依次是
(6)在酸性溶液中存在大量的I-,则Cr2O
 、Fe3+、Fe2+、Cl-中能与I-大量共存的离子是
、Fe3+、Fe2+、Cl-中能与I-大量共存的离子是
您最近半年使用:0次



