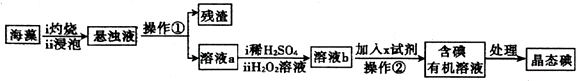
海带中含有丰富的碘,为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
请回答下列问题:
(1)步骤①灼烧海带,除需要三脚架、泥三角外,还需要的仪器是___________ (填字母)。
A 烧杯 B 坩埚 C 表面皿 D 干燥器 E 酒精灯
(2)步骤⑤的实验操作名称是___________ ;步骤⑥的目的是从含碘的苯溶液中分离出碘和回收苯,该步骤的实验操作名称是___________ 。
(3)步骤⑤中,选择用苯来提取碘的理由是:___________ 。
(4)写出步骤④中发生的化学方程式(碘离子由KI提供):___________ 。

请回答下列问题:
(1)步骤①灼烧海带,除需要三脚架、泥三角外,还需要的仪器是
A 烧杯 B 坩埚 C 表面皿 D 干燥器 E 酒精灯
(2)步骤⑤的实验操作名称是
(3)步骤⑤中,选择用苯来提取碘的理由是:
(4)写出步骤④中发生的化学方程式(碘离子由KI提供):
更新时间:2020-12-25 12:32:16
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
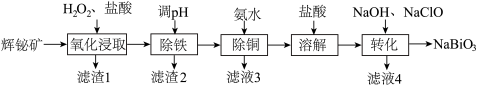
【推荐1】铋(Bi)的化合物广泛应用于电子、医药等领域。由辉铋矿(主要成分为 ,含FeS、CuO、
,含FeS、CuO、 等杂质)制备
等杂质)制备 的工艺流程如下:
的工艺流程如下:
已知:
ⅰ. 难溶于冷水;滤渣1含S;
难溶于冷水;滤渣1含S;
ⅱ.“氧化浸取”时,铋元素转化为 ,硫元素转化为硫单质;
,硫元素转化为硫单质;
iii.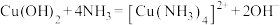 。
。
回答下列问题。
(1)“氧化浸取”步骤中温度升高可以增大速率,但高于50 ℃时浸取速率会下降,其可能的原因是_______ 。
(2)“氧化浸取”时,FeS发生反应的离子方程式为_______ 。
(3)“除铁”步骤中调节pH最好选用的试剂为_______(填字母)。
(4)“转化”时,生成 的反应中氧化剂与氧化产物的物质的量之比为
的反应中氧化剂与氧化产物的物质的量之比为_______ 。
(5) 产品纯度的测定。取
产品纯度的测定。取 产品
产品 ,加入足量稀硫酸和
,加入足量稀硫酸和 稀溶液10 mL使其完全反应(Bi被还原为+3价),再用
稀溶液10 mL使其完全反应(Bi被还原为+3价),再用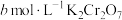 标准溶液滴定溶液中剩余的
标准溶液滴定溶液中剩余的 ,恰好消耗
,恰好消耗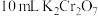 标准溶液。该产品的纯度为
标准溶液。该产品的纯度为_______ (用含 的代数式表示)。
的代数式表示)。
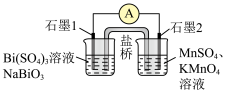
(6)组装为下图装置后发现导线中电流方向为石墨1→石墨2,则该装置的负极为_______ ,石墨2电极上的电极反应式为_______ 。
 ,含FeS、CuO、
,含FeS、CuO、 等杂质)制备
等杂质)制备 的工艺流程如下:
的工艺流程如下:
已知:
ⅰ.
 难溶于冷水;滤渣1含S;
难溶于冷水;滤渣1含S;ⅱ.“氧化浸取”时,铋元素转化为
 ,硫元素转化为硫单质;
,硫元素转化为硫单质;iii.
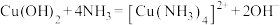 。
。回答下列问题。
(1)“氧化浸取”步骤中温度升高可以增大速率,但高于50 ℃时浸取速率会下降,其可能的原因是
(2)“氧化浸取”时,FeS发生反应的离子方程式为
(3)“除铁”步骤中调节pH最好选用的试剂为_______(填字母)。
| A.稀硫酸 | B.碳酸钠 | C.三氧化二铋 | D.氨水 |
(4)“转化”时,生成
 的反应中氧化剂与氧化产物的物质的量之比为
的反应中氧化剂与氧化产物的物质的量之比为(5)
 产品纯度的测定。取
产品纯度的测定。取 产品
产品 ,加入足量稀硫酸和
,加入足量稀硫酸和 稀溶液10 mL使其完全反应(Bi被还原为+3价),再用
稀溶液10 mL使其完全反应(Bi被还原为+3价),再用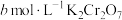 标准溶液滴定溶液中剩余的
标准溶液滴定溶液中剩余的 ,恰好消耗
,恰好消耗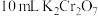 标准溶液。该产品的纯度为
标准溶液。该产品的纯度为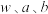 的代数式表示)。
的代数式表示)。(6)组装为下图装置后发现导线中电流方向为石墨1→石墨2,则该装置的负极为

您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】溴被称为“海洋元素”。已知Br2的沸点为59℃,微溶于水,有毒性和强腐蚀性。实验室模拟从海水中提取溴的主要步骤为:
步骤1:将海水蒸发浓缩除去粗盐;
步骤2:将除去粗盐后的母液酸化后,通入适量的氯气,使Br-转化为Br2;
步骤3:向步骤2所得的水溶液中通入热空气或水蒸气,将溴单质吹入盛有二氧化硫水溶液的容器中;
步骤4:再向该容器中通入适量的氯气,使Br-转化为Br2;
步骤5:用四氯化碳萃取溴单质,经分液、蒸馏得粗溴。
(1)步骤3中的反应的离子方程式________ 。
(2)步骤2中已经制得了溴,还要进行步骤3和步骤4的原因是___________ 。
(3)步骤5中萃取和分液所需要的主要玻璃仪器为_________________ 。
(4)用如上图所示的实验装置可精制粗溴。
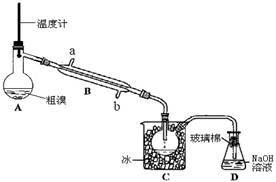
①反应过程中需要对A容器加热,加热的方法是_______________ 。
图中冷却水应从B的________ 口进入(填“a”或“b”)。
②C中加冰的目的是_______________________ 。
步骤1:将海水蒸发浓缩除去粗盐;
步骤2:将除去粗盐后的母液酸化后,通入适量的氯气,使Br-转化为Br2;
步骤3:向步骤2所得的水溶液中通入热空气或水蒸气,将溴单质吹入盛有二氧化硫水溶液的容器中;
步骤4:再向该容器中通入适量的氯气,使Br-转化为Br2;
步骤5:用四氯化碳萃取溴单质,经分液、蒸馏得粗溴。
(1)步骤3中的反应的离子方程式
(2)步骤2中已经制得了溴,还要进行步骤3和步骤4的原因是
(3)步骤5中萃取和分液所需要的主要玻璃仪器为
(4)用如上图所示的实验装置可精制粗溴。

①反应过程中需要对A容器加热,加热的方法是
图中冷却水应从B的
②C中加冰的目的是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】物质的分离、提纯和定量测定是研究物质的方法。
(1)选择下列实验方法分离物质,将分离方法的序号填在横线上。
a.萃取分液b.升华c.结晶d.过滤e.蒸馏f.分液
①从碘水中提取碘单质_____ ;
②分离水和汽油的混合物_____ ;
③从硝酸钾和氯化钠的混合液中获得硝酸钾_____ ;
现有 、
、 和
和 的混合物,选择适当的试剂除去杂质,从而得到纯净的
的混合物,选择适当的试剂除去杂质,从而得到纯净的 晶体,相应的实验流程如图所示。
晶体,相应的实验流程如图所示。
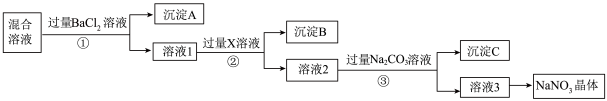
(2)写出实验流程中下列物质的化学式:沉淀A_____ ,试剂X_____ 。
(3)上述实验流程中①②③步均要进行的实验操作是_____ (填操作名称)。
(4)上述实验流程中加入过量 溶液的目的是
溶液的目的是_____ 。
(5)按此实验方案得到的溶液3中肯定含有_____ (填化学式)杂质。为了解决这个问题,可以向溶液3中加入适量的_____ (填化学式)
(1)选择下列实验方法分离物质,将分离方法的序号填在横线上。
a.萃取分液b.升华c.结晶d.过滤e.蒸馏f.分液
①从碘水中提取碘单质
②分离水和汽油的混合物
③从硝酸钾和氯化钠的混合液中获得硝酸钾
现有
 、
、 和
和 的混合物,选择适当的试剂除去杂质,从而得到纯净的
的混合物,选择适当的试剂除去杂质,从而得到纯净的 晶体,相应的实验流程如图所示。
晶体,相应的实验流程如图所示。
(2)写出实验流程中下列物质的化学式:沉淀A
(3)上述实验流程中①②③步均要进行的实验操作是
(4)上述实验流程中加入过量
 溶液的目的是
溶液的目的是(5)按此实验方案得到的溶液3中肯定含有
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
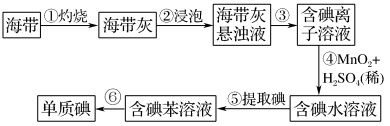
【推荐1】Ⅰ.海带中含有丰富的碘,某学习小组设计并进行以下实验:
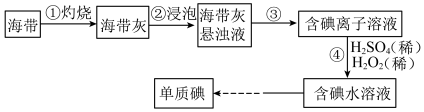
(1)步骤③的实验操作为___________ (填实验名称),此过程使用玻璃棒,玻璃棒的作用是___________ 。
(2)步骤④的离子反应方程式为: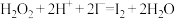 ,该离子反应中的氧化剂是
,该离子反应中的氧化剂是___________ ,还原剂是___________ 。步骤④得到的含碘水溶液中滴加淀粉溶液,溶液呈现蓝色,说明有碘单质产生。
Ⅱ.碘称为“智力元素”。过去食盐中作为加碘剂,但由于空气中氧气的作用,容易引起碘的损失, 被氧气氧化成碘单质(
被氧气氧化成碘单质( ),同时得到强碱性物质。
),同时得到强碱性物质。
(3)写出潮湿环境下 与氧气反应的化学方程式:
与氧气反应的化学方程式:___________ 。
Ⅲ.现在的食盐里改添加性质稳定的 ,以满足人们需要。几种粒子之间有如图所示关系:
,以满足人们需要。几种粒子之间有如图所示关系:
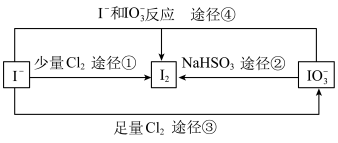
(4)四个途径中属于氧化还原反应的是___________ (填序号)。
(5)在碱性条件下碘酸钾能被氯气氧化为高碘酸钾(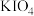 ),反应方程式为:
),反应方程式为: ,写出该反应的离子方程式:
,写出该反应的离子方程式:___________ 。
(6)比较 、
、 和
和 的氧化性强弱:
的氧化性强弱:___________ 。

(1)步骤③的实验操作为
(2)步骤④的离子反应方程式为:
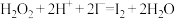 ,该离子反应中的氧化剂是
,该离子反应中的氧化剂是Ⅱ.碘称为“智力元素”。过去食盐中作为加碘剂,但由于空气中氧气的作用,容易引起碘的损失,
 被氧气氧化成碘单质(
被氧气氧化成碘单质( ),同时得到强碱性物质。
),同时得到强碱性物质。(3)写出潮湿环境下
 与氧气反应的化学方程式:
与氧气反应的化学方程式:Ⅲ.现在的食盐里改添加性质稳定的
 ,以满足人们需要。几种粒子之间有如图所示关系:
,以满足人们需要。几种粒子之间有如图所示关系:
(4)四个途径中属于氧化还原反应的是
(5)在碱性条件下碘酸钾能被氯气氧化为高碘酸钾(
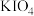 ),反应方程式为:
),反应方程式为: ,写出该反应的离子方程式:
,写出该反应的离子方程式:(6)比较
 、
、 和
和 的氧化性强弱:
的氧化性强弱:
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】海洋植物如海带、海藻中含有丰丰富的碘元素,碘元素以碘离子的形式存在。实.验室里从海带中提取碘的流程如图。
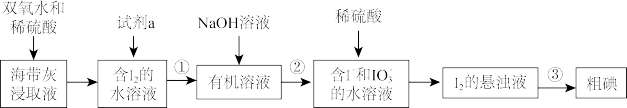
(1)操作①为分液,若试剂a为苯,则有机溶液需从分液漏斗__ (填“上口倒出”或“下口放出”)。
(2)加入双氧水的作用是__ ,操作③的名称是__ 。
(3)I-和IO 在酸性条件下生成I2的离子方程式是
在酸性条件下生成I2的离子方程式是__ 。
(4)图中,含I2的溶液经3步转化为I2的悬浊液,其目的是__ 。

(1)操作①为分液,若试剂a为苯,则有机溶液需从分液漏斗
(2)加入双氧水的作用是
(3)I-和IO
 在酸性条件下生成I2的离子方程式是
在酸性条件下生成I2的离子方程式是(4)图中,含I2的溶液经3步转化为I2的悬浊液,其目的是
您最近半年使用:0次