KMnO4广泛用作氧化剂,可以氧化HCl、FeSO4等。某兴趣小组用Cl2氧化K2MnO4制备KMnO4的装置如下图所示。
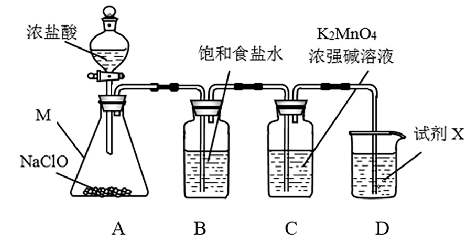
(1)仪器M的名称是_______ 。
(2)装置B的作用是_______ 。
(3)为提高Cl2在装置C中的利用率,在装置A的操作中可采取的措施是_______ 。
(4)试剂X常用浓NaOH溶液,而不用澄清石灰水的主要原因是_______ 。
(5)利用KMnO4测定CuI样品中CuI质量分数(杂质不参与反应)的方法如下:
步骤一:称取CuI样品0.500g,向其中加入足量Fe2(SO4)3溶液,发生反应4Fe3++2CuI=4Fe2++2Cu2++I2。
步骤二:待充分反应后,滴加5.000×10−2mol·L−1KMnO4溶液,发生反应 +5Fe2++8H+=Mn2++5Fe3++4H2O,至恰好完全反应消耗KMnO4溶液20.00mL。
+5Fe2++8H+=Mn2++5Fe3++4H2O,至恰好完全反应消耗KMnO4溶液20.00mL。
计算该样品中碘化亚铜的质量分数(写出计算过程)。_______

(1)仪器M的名称是
(2)装置B的作用是
(3)为提高Cl2在装置C中的利用率,在装置A的操作中可采取的措施是
(4)试剂X常用浓NaOH溶液,而不用澄清石灰水的主要原因是
(5)利用KMnO4测定CuI样品中CuI质量分数(杂质不参与反应)的方法如下:
步骤一:称取CuI样品0.500g,向其中加入足量Fe2(SO4)3溶液,发生反应4Fe3++2CuI=4Fe2++2Cu2++I2。
步骤二:待充分反应后,滴加5.000×10−2mol·L−1KMnO4溶液,发生反应
 +5Fe2++8H+=Mn2++5Fe3++4H2O,至恰好完全反应消耗KMnO4溶液20.00mL。
+5Fe2++8H+=Mn2++5Fe3++4H2O,至恰好完全反应消耗KMnO4溶液20.00mL。计算该样品中碘化亚铜的质量分数(写出计算过程)。
2021高二·江苏扬州·学业考试 查看更多[4]
江苏省扬州市2021年普通高中学业水平检测模拟化学试题(已下线)2020年山东卷化学高考真题变式题16-20江苏省盐城市伍佑中学2022-2023学年高二上学期期中考试化学(必修)试题江苏省宿迁市沭阳县潼阳中学2021-2022学年高二上学期期中考试化学试题
更新时间:2021-01-05 19:19:07
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备氧化铝的主要原料.工业上提取氧化铝的工艺流程如下:
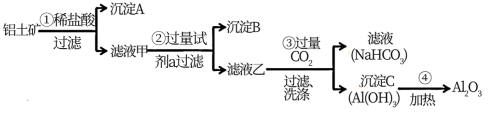
(1)沉淀A、B的成分分别是_______ 、_______ ;
(2)步骤②中的试剂a是_______ ;
(3)试写出步骤③中发生反应的离子方式_______ ;
(4)在实验室模拟上述实验过程中,需要用到一定浓度的盐酸溶液.在配制250mL该盐酸溶液时,某同学转移溶液的操作如图1所示,图中的主要错误是:①_______ ;②_______ 。
(5)准确称取6g铝土矿样品,加入100mL盐酸溶液,充分反应后向滤液中加入10mol•L﹣1试剂a的溶液,产生沉淀的质量与加入试剂a的体积关系如图2所示,则所用盐酸溶液的物质的量浓度为_______ ,样品中Al2O3的百分含量为_______ 。
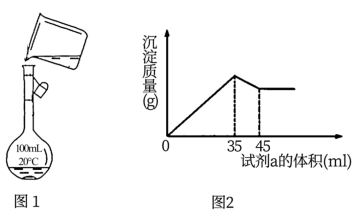

(1)沉淀A、B的成分分别是
(2)步骤②中的试剂a是
(3)试写出步骤③中发生反应的离子方式
(4)在实验室模拟上述实验过程中,需要用到一定浓度的盐酸溶液.在配制250mL该盐酸溶液时,某同学转移溶液的操作如图1所示,图中的主要错误是:①
(5)准确称取6g铝土矿样品,加入100mL盐酸溶液,充分反应后向滤液中加入10mol•L﹣1试剂a的溶液,产生沉淀的质量与加入试剂a的体积关系如图2所示,则所用盐酸溶液的物质的量浓度为

您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐2】1273K时H2O(g)通过红热的铁生产H2,发生如下反应:Fe(s)+H2O(g)⇌FeO(s)+H2(g),反应的平衡常数Kp=1.49.(Kp是以各平衡混合气体分压表示的化学平衡常数。)
(1)计算每生产1.00mol氢气需通入水蒸气的物质的量为_____ 。
(2)1273K时,若反应体系中只有0.30mol的铁并通入1.00mol水蒸气与其反应,试计算反应后各组分的物质的量_______ 。反应后体系是否处于平衡状态,为什么_______ 。
(3)1273K,当1.0mnol水蒸气与0.80mol铁接触时,最后各组分的物质的量是________ 。
(1)计算每生产1.00mol氢气需通入水蒸气的物质的量为
(2)1273K时,若反应体系中只有0.30mol的铁并通入1.00mol水蒸气与其反应,试计算反应后各组分的物质的量
(3)1273K,当1.0mnol水蒸气与0.80mol铁接触时,最后各组分的物质的量是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】用中和滴定法测定烧碱的纯度,若烧碱中不含有与酸反应的杂质,试根据实验回答:
(1)准确称取4.1g烧碱样品,所用主要仪器是____________________ 。
(2)将样品配成250mL待测液,需要的仪器有___________________ 。
(3)取10.00mL待测液,用__________________ 量取。
(4)用0.2010mol·L-1标准盐酸滴定待测烧碱溶液,滴定时_________ 手旋转_________ 式滴定管的玻璃活塞,__________ 手不停地摇动锥形瓶,两眼注视_______ ,直到滴定终点。
(5)根据下列数据,计算待测烧碱溶液的浓度:____________________ 。
(1)准确称取4.1g烧碱样品,所用主要仪器是
(2)将样品配成250mL待测液,需要的仪器有
(3)取10.00mL待测液,用
(4)用0.2010mol·L-1标准盐酸滴定待测烧碱溶液,滴定时
(5)根据下列数据,计算待测烧碱溶液的浓度:
| 滴定次数 | 待测液体积 (mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 10.00 | 0.50 | 20.40 |
| 第二次 | 10.00 | 4.00 | 24.10 |
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】框图所示的转化关系中,甲为生活中常见的金属单质,乙、丙、丁为气体单质,D为家庭中常用物质(部分反应物和生成物及溶剂水已略去)。
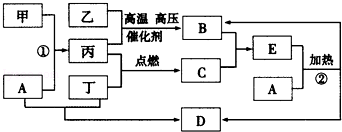
请回答:
(1)E的化学式为_______ ;甲的原子结构示意图为_______ ;
(2)反应①的离子方程式为_______ ;反应②的化学方程式为_______ ;
(3)实验室制取并收集B的操作中,用_______ 法收集B,验证B已收集满的方法是_______ (限答一种)。
(4)实验室制备丁的方程式为_______ ,工业上输送丁的管道出现气体泄漏,如何查漏(用方程式表示)_______ .

请回答:
(1)E的化学式为
(2)反应①的离子方程式为
(3)实验室制取并收集B的操作中,用
(4)实验室制备丁的方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】二氧化锰与浓盐酸混合加热可得到氯气,如图是制取氯气并探究化学性质的装置。
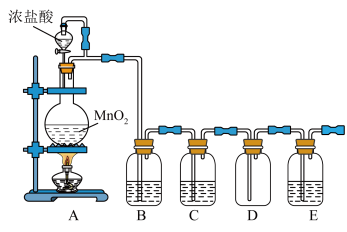
(1)圆底烧瓶中的化学方程式为:___________ 。
(2)若要得到纯净干燥的气体,则装置B的作用是___________ ,C中应盛放的试剂是___________ 。
(3)E中若装有淀粉碘化钾溶液,能观察到的实验现象是___________ 。
(4)此装置的缺点是___________ ,应如何改进:___________ 。

(1)圆底烧瓶中的化学方程式为:
(2)若要得到纯净干燥的气体,则装置B的作用是
(3)E中若装有淀粉碘化钾溶液,能观察到的实验现象是
(4)此装置的缺点是
您最近一年使用:0次