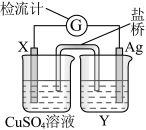
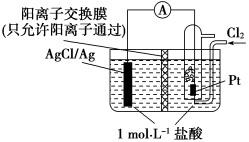
应用电化学原理,回答下列问题:
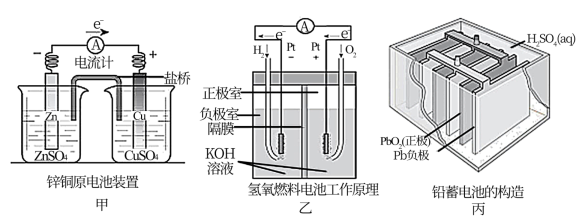
(1)上述三个装置中,负极反应物化学性质上的共同特点是_______ 。
(2)甲中电流计指针偏移时,盐桥(装有含琼胶的KCl饱和溶液)中离子移动的方向是_______ 。
(3)乙中若将H2换成CH4,则负极反应式为_______ 。
(4)丙中铅蓄电池进行充电时,要将外接电源的负极与铅蓄电池_______ 极相连接。
(5)应用原电池反应可以探究氧化还原反应进行的方向和程度。按下图连接装置并加入药品(盐桥中的物质不参与反应),进行实验:
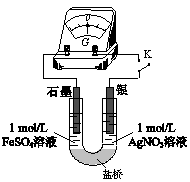
ⅰ.K闭合时,指针偏移。放置一段时间后,指针偏移减小。
ⅱ.随后向U形管左侧逐渐加入浓Fe2(SO4)3溶液,发现电压表指针的变化依次为:偏移减小→回到零点→逆向偏移。
①实验ⅰ中银作_______ 极。
②综合实验ⅰ、ⅱ的现象,得出Ag+和Fe2+反应的离子方程式是_______ 。

(1)上述三个装置中,负极反应物化学性质上的共同特点是
(2)甲中电流计指针偏移时,盐桥(装有含琼胶的KCl饱和溶液)中离子移动的方向是
(3)乙中若将H2换成CH4,则负极反应式为
(4)丙中铅蓄电池进行充电时,要将外接电源的负极与铅蓄电池
(5)应用原电池反应可以探究氧化还原反应进行的方向和程度。按下图连接装置并加入药品(盐桥中的物质不参与反应),进行实验:

ⅰ.K闭合时,指针偏移。放置一段时间后,指针偏移减小。
ⅱ.随后向U形管左侧逐渐加入浓Fe2(SO4)3溶液,发现电压表指针的变化依次为:偏移减小→回到零点→逆向偏移。
①实验ⅰ中银作
②综合实验ⅰ、ⅱ的现象,得出Ag+和Fe2+反应的离子方程式是
更新时间:2021/01/04 09:26:42
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】铜与稀硫酸不反应,某校实验小组的同学在老师的指导下设计了下列装置,实现了铜与稀硫酸的反应。请回答下列问题:
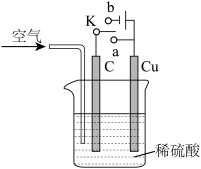
(1)甲同学认为,不通入空气,将 K 与_____ (填“a”或“b”)连接,即可实现。则总反应的离子方程式为_____ 。
(2)乙同学认为在通入空气的同时,将开关 K 与_____ 连通,也可以实现,则电池总反应的化学方程式为_____ 。

(1)甲同学认为,不通入空气,将 K 与
(2)乙同学认为在通入空气的同时,将开关 K 与
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(i)燃料电池是目前正在探索的一种新型电池,目前已经使用的氢氧燃料电池的基本反应是正极:O2+2H2O+4e-=4OH-,回答下列问题:
(1)电解质溶液为____________ 。
(2)负极发生________ 反应(填“氧化”或“还原”)。写出其电极反应式___________ 。
(3)若反应后得到5.4 g液态水,此时氢氧燃料电池转移的电子数为________ 。
(ii)如图所示的装置,在盛有水的烧杯中,铁圈和银圈的连接处吊着一根绝缘的细丝,使之平衡。小心地往烧杯中央滴入CuSO4溶液。

(1)片刻后可观察到的现象是(指悬吊的金属圈)________ 。
A.铁圈和银圈左右摇摆不定 B.保持平衡状态不变
C.铁圈向下倾斜 D.银圈向下倾斜
(2)产生上述现象的原因是___________________________________ 。
(iii)铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式:___________________________ 。
(2)若将(1)中的反应设计成原电池,并写出正、负极电极反应式。
正极反应:______________________ ,负极反应:______________________ 。
(1)电解质溶液为
(2)负极发生
(3)若反应后得到5.4 g液态水,此时氢氧燃料电池转移的电子数为
(ii)如图所示的装置,在盛有水的烧杯中,铁圈和银圈的连接处吊着一根绝缘的细丝,使之平衡。小心地往烧杯中央滴入CuSO4溶液。

(1)片刻后可观察到的现象是(指悬吊的金属圈)
A.铁圈和银圈左右摇摆不定 B.保持平衡状态不变
C.铁圈向下倾斜 D.银圈向下倾斜
(2)产生上述现象的原因是
(iii)铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式:
(2)若将(1)中的反应设计成原电池,并写出正、负极电极反应式。
正极反应:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6 mol·L-1的H2SO4溶液中,乙同学将电极放入6 mol·L-1的NaOH溶液中,如图所示。
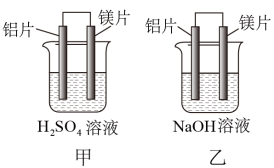
(1)写出甲中正极的电极反应:_______ ,总反应的离子方程式:_______ 。
(2)乙中总反应的离子方程式:_______ 。
(3)甲池溶液中阳离子的移动方向是_______ 。乙池外电路中电子的流动方向是_______ 。甲池中产生气泡的电极是_______ ;乙池外电路中电流的方向是_______ 。
(4)若甲与乙同学均认为“构成原电池的电极材料如果都是金属,则负极材料的金属应比正极材料的金属活泼”,则甲会判断出_______ 金属活动性更强,而乙会判断出_______ 金属活动性更强。
(5)由此实验得出的下列结论中,正确的有_______ 。
A.该实验说明金属活动性顺序已过时,没有实用价值了
B.该实验说明化学研究对象复杂、反应受条件影响较大,因此应具体问题具体分析
C.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
D.镁的金属性不一定比铝的金属性强

(1)写出甲中正极的电极反应:
(2)乙中总反应的离子方程式:
(3)甲池溶液中阳离子的移动方向是
(4)若甲与乙同学均认为“构成原电池的电极材料如果都是金属,则负极材料的金属应比正极材料的金属活泼”,则甲会判断出
(5)由此实验得出的下列结论中,正确的有
A.该实验说明金属活动性顺序已过时,没有实用价值了
B.该实验说明化学研究对象复杂、反应受条件影响较大,因此应具体问题具体分析
C.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
D.镁的金属性不一定比铝的金属性强
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某学生利用图实验装置探究盐桥式原电池的工作原理。(铜元素的相对原子质量为64)

按照实验步骤依此回答下列问题:
(1)导线中电子的流向为_______ 到_______ (用a、b表示)。
(2)写出装置中锌电极上的电极反应式:_______ 。
(3)装置的盐桥中除添加琼脂外,还要添加KCl的饱和溶液,电池工作时,下列对盐桥中的K+、Cl-的移动方向的表述正确的是_______ 。
A.盐桥中的K+向左侧烧杯移动、Cl-向右侧烧杯移动
B.盐桥中的K+向右侧烧杯移动、Cl-向左侧烧杯移动
C.盐桥中的K+、Cl-都向左侧烧杯移动
D盐桥中的K+、Cl-几乎都不移动

按照实验步骤依此回答下列问题:
(1)导线中电子的流向为
(2)写出装置中锌电极上的电极反应式:
(3)装置的盐桥中除添加琼脂外,还要添加KCl的饱和溶液,电池工作时,下列对盐桥中的K+、Cl-的移动方向的表述正确的是
A.盐桥中的K+向左侧烧杯移动、Cl-向右侧烧杯移动
B.盐桥中的K+向右侧烧杯移动、Cl-向左侧烧杯移动
C.盐桥中的K+、Cl-都向左侧烧杯移动
D盐桥中的K+、Cl-几乎都不移动
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】分别按如图甲、乙所示装置进行实验,图中两个烧杯里的溶液均为2L同浓度的稀硫酸,乙中A为电流表。请回答下列问题:
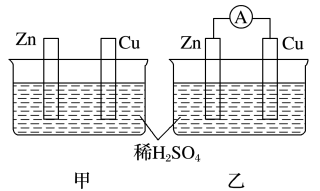
(1)以下叙述中,正确的是_______ (填字母)
A.甲溶液中H+会向锌片移动
B.两烧杯中锌片表面均有气泡产生
C.两烧杯中溶液pH均增大
D.甲中锌片是负极,乙中铜片是正极
E.乙的内电路中电流方向Zn→溶液→Cu
(2)实验时,甲、乙同时开始反应,0~15分钟内,测得甲中锌片质量减少了19.5克,乙中收集到氢气13.44升(已转化为标准状况),则用硫酸浓度的变化表示甲乙两装置的反应速率分别为:v(甲)=_________ mol·L-1·min-1,v(乙)=_________ mol·L-1·min-1,v(甲)___ v(乙)(填>,<或 =),主要原因是__________ 。
(3)变化过程中能量转化的主要形式:甲为_________ ;乙为____________ 。
(4)在乙实验中,如果把硫酸换成硝酸银溶液,请写出铜电极的电极反应方程式:_______ ,此时乙装置中正极的现象是____________ 。

(1)以下叙述中,正确的是
A.甲溶液中H+会向锌片移动
B.两烧杯中锌片表面均有气泡产生
C.两烧杯中溶液pH均增大
D.甲中锌片是负极,乙中铜片是正极
E.乙的内电路中电流方向Zn→溶液→Cu
(2)实验时,甲、乙同时开始反应,0~15分钟内,测得甲中锌片质量减少了19.5克,乙中收集到氢气13.44升(已转化为标准状况),则用硫酸浓度的变化表示甲乙两装置的反应速率分别为:v(甲)=
(3)变化过程中能量转化的主要形式:甲为
(4)在乙实验中,如果把硫酸换成硝酸银溶液,请写出铜电极的电极反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】2010年中科院某所宣布,“大容量钠硫储能电池”已研发成功,(之前,世界上仅日本拥有)。该电池的两极材料分别为钠和硫,负极材料是________ , 正极材料是________________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】人们应用原电池原理制作了多种电池,以满足不同的需要。以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息填空。
(1)铅蓄电池在放电时起原电池作用,铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。负极反应式为____ ;反应一段时间后负极的质量___ (填“增重”或“减少”或“不变”)
(2)燃料电池是一种高效、环境友好的供电装置,如甲烷燃料电池,在碱性条件下该电池的负电极反应式是:____ 。
(3)将铝片和铜片用导线相连,分别插入浓硝酸中(a组)和插入烧碱溶液中(b组),都形成了原电池,在a组原电池中,负极材料为____ ;写出b组插入烧碱溶液中形成原电池的负极反应式:___ 。
(4)FeCl3溶液常用于腐蚀印刷电路铜板,发生反应2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为____ ,电解质溶液为____ ,反应中Cl-移向___ (填“负极”或“正极”),FeCl3溶液发生____ 反应(填“氧化”或“还原”)。
(5)碱性纽扣电池的总反应为Zn+Ag2O=2Ag+ZnO,其正极反应式为____ 。
(1)铅蓄电池在放电时起原电池作用,铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。负极反应式为
(2)燃料电池是一种高效、环境友好的供电装置,如甲烷燃料电池,在碱性条件下该电池的负电极反应式是:
(3)将铝片和铜片用导线相连,分别插入浓硝酸中(a组)和插入烧碱溶液中(b组),都形成了原电池,在a组原电池中,负极材料为
(4)FeCl3溶液常用于腐蚀印刷电路铜板,发生反应2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为
(5)碱性纽扣电池的总反应为Zn+Ag2O=2Ag+ZnO,其正极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氢氧燃料电池是的介色化学理的新型发电装置,下图为电池示意图,该电池电极表面镀一层细细的铂粉,吸附气体的能力强,性质稳定,请回答
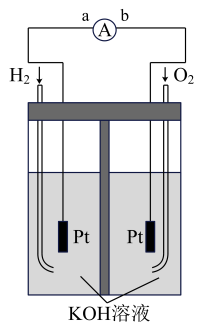
(1)氢氧燃料电量的转化形式是____ ,在导线中电子的流动方向为______ (用a,b表示)
(2)负极反应式为___________
(3)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能,因此大量安全储氢是关键技术之一,金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
I .2Li+H2=2LiH; II. LiH+H2O=LiOH+H2↑
①反应I中的还原剂是______ ,反应II中的氧化剂是______
②由LiH与H2O作用,放出224L(标准状况)H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为____ mol;将产生的电能用来电解饱和食盐水,产生的氢气体积(标准状况)为_____ L

(1)氢氧燃料电量的转化形式是
(2)负极反应式为
(3)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能,因此大量安全储氢是关键技术之一,金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
I .2Li+H2=2LiH; II. LiH+H2O=LiOH+H2↑
①反应I中的还原剂是
②由LiH与H2O作用,放出224L(标准状况)H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图是某同学设计的一个简易的原电池装置,请回答下列问题。
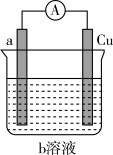
(1)若a电极材料为碳、b溶液为 FeCl3溶液,则正极的电极反应式为___________ ,当有1.6 g负极材料溶解时,转移的电子为___________ mol。
(2)若a电极材料为铁、b溶液为浓硝酸,电流表的指针也会偏转,则电子的流向为___________ →___________ (填电极材料,下同),溶液中的NO 向
向___________ 极移动。

(1)若a电极材料为碳、b溶液为 FeCl3溶液,则正极的电极反应式为
(2)若a电极材料为铁、b溶液为浓硝酸,电流表的指针也会偏转,则电子的流向为
 向
向
您最近一年使用:0次