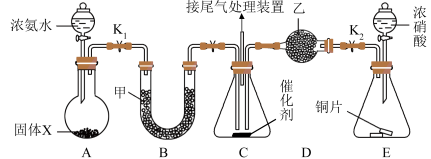
分别进行如下表所示实验,现象和结论均正确的是
| 选项 | 实验 | 现象 | 结论 |
| A | 将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液 | 有气体生成,溶液未呈红色 | 稀硝酸不能将Fe氧化为Fe3+ |
| B | NaAlO2溶液中滴入NaHCO3溶液 | 产生白色沉淀 |  与 与 发生双水解反应 发生双水解反应 |
| C | 向某溶液里滴加NaOH溶液并将湿润的红色石蕊试纸置于试管口 | 试纸颜色没变 | 原溶液中无 |
| D | 将0.1 mol/L MgSO4溶液滴入NaOH溶液里至不再有沉淀产生,再滴加0.1 mol/L CuSO4溶液 | 先有白色沉淀生成,后变为蓝色沉淀 | Ksp[Cu(OH)2]小于Ksp[Mg(OH)2] |
| A.A | B.B | C.C | D.D |
更新时间:2021-01-12 09:24:36
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】将amol铁粉投入含bmolHNO3的稀硝酸中,固体恰好完全溶解,若HNO3的还原产物只有NO,则a∶b不可能为
| A.1∶4 | B.1∶2 | C.1∶3 | D.3∶8 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】将 分别通入无氧、有氧的浓度均为
分别通入无氧、有氧的浓度均为 的
的 溶液和
溶液和 溶液中,除
溶液中,除 溶液(无氧)外,都产生白色沉淀。实验测得各溶液pH变化曲线如图,下列说法正确的是
溶液(无氧)外,都产生白色沉淀。实验测得各溶液pH变化曲线如图,下列说法正确的是
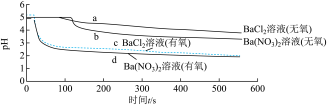
 分别通入无氧、有氧的浓度均为
分别通入无氧、有氧的浓度均为 的
的 溶液和
溶液和 溶液中,除
溶液中,除 溶液(无氧)外,都产生白色沉淀。实验测得各溶液pH变化曲线如图,下列说法正确的是
溶液(无氧)外,都产生白色沉淀。实验测得各溶液pH变化曲线如图,下列说法正确的是
A.曲线a所示溶液pH降低的原因: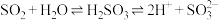 |
B.依据曲线b可推知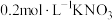 溶液(无氧)能氧化 溶液(无氧)能氧化 |
C.曲线c所示溶液中发生反应的离子方程式为: |
D.曲线d所表示的过程中 是氧化 是氧化 的主要微粒 的主要微粒 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】由下列实验操作所对应的现象得出的结论正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 常温下将Al片放入浓硝酸中 | 无明显变化 | 常温下,Al与浓硝酸不反应 |
| B | 加热盛有NH4Cl固体的试管 | 试管底部固体减少,试管口有晶体凝结 | 加热时NH4Cl固体发生升华 |
| C | 在某未知盐溶液中加入NaOH浓溶液并加热 | 产生能使湿润的红色石蕊试纸变蓝的气体 | 该未知溶液中存在NH |
| D | 在某未知盐溶液中先滴加氯水,再滴加KSCN溶液 | 溶液变红 | 该未知溶液中含有Fe2+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 将Al(OH)3固体粉末加入过量NaOH溶液中,充分搅拌,溶解得到无色溶液 | 既体现碱性又体现酸性 |
| B | 向盛有铜片的试管中加入少量硝酸,一段时间后观察到试管口有红色气体逸出 | 实验所用为浓硝酸 |
| C | 向盛有某溶液的试管中滴加稀氢氧化钠溶液,将湿润的红色石蕊试纸靠近试管口,试纸未变蓝 | 该溶液中不存在NH |
| D | 向a、b两试管中同时加入4mL0.01mol·L-1KMnO4溶液和2mL0.1mol·L-1H2C2O4溶液,再向a试管内加入少量MnSO4,a试管中溶液褪色较快 | MnSO4是KMnO4和H2C2O4反应的催化剂 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】以下通过实验得出的结论中,正确的是( )
| A.取某溶液先加入足量稀盐酸,无沉淀产生,再加入Ba(NO3)2溶液,产生白色沉淀,则该溶液中一定含有SO42- |
| B.已知Cu2O+2H+=Cu2++Cu+H2O。取某红色固体加入足量稀硝酸,固体全部溶解,形成蓝色溶液,则该红色固体中可能含有Cu2O |
| C.在某固体试样加水后的溶液中,加NaOH溶液,没有产生使湿润红色石蕊试纸变蓝的气体,该固体试样不存在NH4+ |
| D.某混合气体依次通入灼热的氧化铜、无水硫酸铜固体、澄清石灰水,观察到氧化铜变红、无水硫酸铜变蓝、澄清石灰水变浑浊,则该混合气体中一定有CO和H2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列离子方程式的书写及评价,均合理的是
| 选项 | 离子方程式 | 评价 |
| A | lmol•L-1的NaA1O2溶液和2.5 mol•L-1的HCl溶液等体积互相均匀混合:2AlO2-+5H+=Al3++Al(OH)3↓+H2O | 正确;AlO2-与Al(OH)3消耗的H+的物质的量之比为2 : 3 |
| B | Ba(HCO3)2溶液与足量的NaOH溶液反应:Ba2++HCO3+OH =BaCO3↓+H2O | 正确;酸式盐与碱反应生成正盐和水 |
| C | 过量SO2通入到NaClO溶液中:SO2+H2O +ClO-=HClO+HSO3- | 正确;:说明酸性:H2SO3强于HClO |
| D | 将2 mol Cl2通入到含1 mol FeI2的溶液中:2Fe2++2I-+2Cl2=2Fe3++4Cl-+ I2 | 正确;C12过量,可将Fe2+、I-均氧化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列各组物质只用胶头滴管和试管不能鉴别的是
| A.KOH溶液与AlCl3溶液 | B.NaAlO2溶液与盐酸 |
| C.NaHCO3溶液与盐酸 | D.Na2CO3溶液与盐酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】25℃时,用图1装置进行实验:向蒸馏水中加入 粉末,一段时间后再加入稀硫酸。测得pH随时间变化的曲线如图2所示。
粉末,一段时间后再加入稀硫酸。测得pH随时间变化的曲线如图2所示。

下列对曲线的分析不正确 的是
 粉末,一段时间后再加入稀硫酸。测得pH随时间变化的曲线如图2所示。
粉末,一段时间后再加入稀硫酸。测得pH随时间变化的曲线如图2所示。
下列对曲线的分析
A.a点时加入的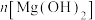 大于c点时加入的 大于c点时加入的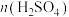 |
B.e点时再加入足量 粉末,可使溶液的pH与b点的相同 粉末,可使溶液的pH与b点的相同 |
C.bc段存在平衡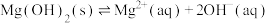 |
D.cd段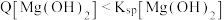 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】有关AgCl的沉淀溶解平衡说法中正确的是
| A.AgCl沉淀生成和溶解不断进行,速率相等 |
| B.AgCl难溶于水,溶液中没有Ag+和Cl- |
| C.升温,AgCl沉淀的溶解度减小 |
| D.AgCl沉淀中加入NaCl固体,AgCl沉淀的溶解度不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】25 ℃时,三种难溶银盐的Ksp与颜色如表所示,下列说法正确的是
| AgCl | Ag2CrO4 | AgI | |
| 颜色 | 白色 | 砖红色 | 黄色 |
| Ksp | 1.8×10-10 | 1.0×10-12 | 8.5×10-17 |
| A.AgCl、Ag2CrO4、AgI饱和溶液中c(Ag+)依次减小 |
| B.Ag2CrO4饱和溶液中c(Ag+)约为1.0×10-6 mol·L-1 |
| C.向AgCl悬浊液上加入足量KI溶液,沉淀将由白色转化为黄色 |
| D.向等浓度的KCl与K2CrO4混合溶液中滴加少量AgNO3溶液,将生成砖红色沉淀 |
您最近一年使用:0次