某化学实验小组探究Fe2+和Fe3+性质时,发现:往FeCl2和KSCN的混合溶液中滴加氯水,溶液变成红色,但当氯水过量时,红色却会褪去。为此,他们设计如图装置进一步探究。
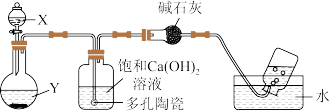
已知:①X为NaClO溶液,Y为FeCl3和KSCN的混合溶液。②持续缓慢滴入NaClO溶液至过量的过程中,圆底烧瓶中红色变浅,有大量气泡产生;Ca(OH)2溶液变浑浊。根据实验现象推测下列说法错误的是

已知:①X为NaClO溶液,Y为FeCl3和KSCN的混合溶液。②持续缓慢滴入NaClO溶液至过量的过程中,圆底烧瓶中红色变浅,有大量气泡产生;Ca(OH)2溶液变浑浊。根据实验现象推测下列说法错误的是
| A.氯水可以将Fe2+氧化成Fe3+ |
| B.烧瓶中还可能产生红褐色沉淀 |
| C.烧瓶中产生的气体中一定含有SO2 |
| D.KSCN中的N元素一定被氧化 |
2021·山西·一模 查看更多[7]
山西省晋中市、大同市2021届高三一模理科综合化学试题(已下线)专题05 金属及其重要化合物-备战2021届高考化学二轮复习题型专练(已下线)重点1 仪器组合型实验方案的设计与评价-2021年高考化学【热点·重点·难点】专练(新高考)江西景德镇市浮梁一中2020-2021学年高二下学期4月月考争优部化学试题(已下线)第1周 周测卷-备战2022年高考化学周测与晚练(新高考专用)(已下线)考向35 实验的方案设计与评价-备战2022年高考化学一轮复习考点微专题福建省福州第三中学2021-2022学年高三上学期第五次质量检测化学试题
更新时间:2021-01-31 21:16:26
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列离子方程式正确的是
| A.工业上制漂白粉: Cl2+ 2OH- =Cl-+ ClO-+ H2O |
B.向硅酸钠溶液中通入过量二氧化碳: SiO + 2CO2+ 2H2O = H2SiO3↓+2HCO + 2CO2+ 2H2O = H2SiO3↓+2HCO |
C.明矾溶液与过量氨水混合: Al3++ 4NH3+ 2H2O = AlO +4NH +4NH |
| D.硫化钠溶液与氯化铁溶液反应: 2Fe3+ +3S2-= Fe2S3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下图横坐标、纵坐标分别表示一定条件下氧化剂的氧化性、还原剂的还原性由弱到强的变化,1、2、3点表示横纵坐标对应微粒在水溶液中反应的产物。下列说法正确的是
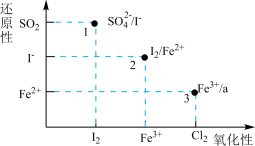

| A.反应1中还原剂和氧化剂化学计量数比为1:1 |
B.反应2的离子方程式为 |
C.反应3的产物a是 |
D.从图可推得 不能氧化 不能氧化 、 、 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】为确定下列置于空气中的物质是否变质,所选检验试剂(括号内)不能达到目的的是
| A.Na2SO3溶液(BaCl2溶液) | B.FeSO4溶液(KSCN溶液) |
| C.漂白粉(稀硝酸) | D.NaOH溶液[Ba(OH)2溶液] |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列物质反应后一定有+3价铁生成的是( )
① Fe(过量)在O2燃烧; ② Fe与过量稀H2SO4反应;③ 铁与铜的混合物与氯化铁溶液混合,有固体剩余;④ FeO和Fe2O3的混合物溶于盐酸中。
① Fe(过量)在O2燃烧; ② Fe与过量稀H2SO4反应;③ 铁与铜的混合物与氯化铁溶液混合,有固体剩余;④ FeO和Fe2O3的混合物溶于盐酸中。
| A.① ②③④ | B.①④ | C.② ③ | D.④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某学生运用所学知识研究物质的性质:将一块金属钠和一块锌片分别放在表面皿上,研究它们在空气中的稳定性。该学生采用的研究方法是
①假说法 ②实验法 ③分类法 ④比较法
①假说法 ②实验法 ③分类法 ④比较法
| A.①② | B.①③ | C.②③ | D.②④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】为了预防传染性疾病,不少地方都采用了“84”消毒液进行消毒。“84”消毒液(有效成分为NaClO)可用于消毒和漂白。下列对相关实验现象的分析,不正确 的是


| 实验 | I | II | III |
| 滴管中的液体 | 1mL的蒸馏水 | 1mL0.0002mol•L-1的H2SO4 | 1mL2mol•L-1的H2SO4 |
| 实验现象 | 混合后溶液的pH=9.9,短时间内未褪色,一段时间后蓝色褪去 | 混合后溶液的pH=5.0,蓝色迅速褪去,无气体产生 | 混合后溶液的pH=3.2,蓝色迅速褪去,并产生大量气体,使湿润的淀粉碘化钾试纸变蓝 |
| A.对比实验I和II,II中蓝色迅速褪去的原因是发生了反应:ClO-+H+=HClO |
| B.对比实验II和III,溶液的pH可能会影响ClO-的氧化性或Cl-的还原性 |
| C.实验III中产生的气体是Cl2,由HClO分解得到:2HClO=Cl2↑+H2O |
| D.加酸可以提高“84”消毒液的漂白效果,但需合适的pH才能安全使用 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】某小组对Fe2+和Ag+的反应进行了如下探究实验:
(已知:Ag2SO4为白色微溶物;反应过程中测得温度几乎无变化)
下列说法正确的是
操作 | 现象 | Ag+ 浓度变化曲线 | |
实验Ⅰ | 向1 mL 0.1 mol/L FeSO4溶液中加入1 mL 0.1 mol/L AgNO3溶液 | 几分钟后,出现大量灰黑色浑浊 |
|
实验Ⅱ | 先向试管中加入几滴Fe2(SO4)3溶液,然后重复实验Ⅰ的操作 | 现象与实验Ⅰ相同 |
下列说法正确的是
| A.实验Ⅰ只发生反应:Fe2++Ag+⇌Fe3++Ag,灰黑色浑浊是Ag |
| B.图中c(Ag+)由a→b急速变化的可能原因是反应放热 |
| C.图中c(Ag+)由a→b急速变化的可能原因是生成的Ag起催化作用 |
| D.图中c(Ag+)由a→b急速变化的可能原因是生成的Fe3+起催化作用 |
您最近一年使用:0次



 、
、 、
、 、
、
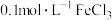 溶液:
溶液: 、
、 、
、 、
、
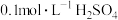 溶液:
溶液: 、
、 、
、
 溶液:
溶液: 、
、 、
、


