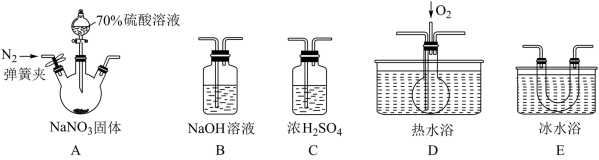
亚硝酸和亚硝酸盐在生产、医药等领域有着广泛应用。某校化学兴趣小组用下图所示仪器(夹持装置已省略)及药品,探究硫酸与亚硝酸钠反应生成气体的成分。已知 和NO液化温度分别为21℃和-152℃。
和NO液化温度分别为21℃和-152℃。
请回答下列问题:
(1)反应前通入氮气的目的是___________ 。装置的连接顺序(按左→右连接)为A→___________ →___________ →___________ →B。
(2)在关闭弹簧夹,打开分液漏斗活塞、滴入70%硫酸溶液后,A中产生红棕色气体。确认A中产生的气体含有 依据的现象是
依据的现象是___________ 。
(3)装置A中反应的化学方程式为___________ 。
(4)如果没有装置C,对实验结论造成的影响是___________ 。
 和NO液化温度分别为21℃和-152℃。
和NO液化温度分别为21℃和-152℃。
请回答下列问题:
(1)反应前通入氮气的目的是
(2)在关闭弹簧夹,打开分液漏斗活塞、滴入70%硫酸溶液后,A中产生红棕色气体。确认A中产生的气体含有
 依据的现象是
依据的现象是(3)装置A中反应的化学方程式为
(4)如果没有装置C,对实验结论造成的影响是
更新时间:2021-01-08 15:20:34
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】为探究铜与稀硝酸反应的气体产物,进行如下实验,实验装置如图所示。
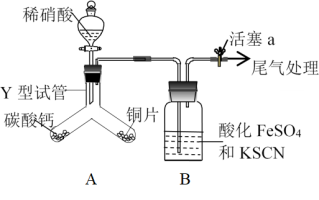
已知:FeSO4+NO=[Fe(NO)]SO4该反应较缓慢,待生成一定量[Fe(NO)]2+时突显明显棕色。
(1)盛装稀硝酸的仪器名称为:_______
(2)实验开始前,如何检验A装置的气密性:_______
(3)实验开始时先将Y形试管向盛有碳酸钙的支管倾斜,缓慢滴入稀硝酸,该实验操作的目的是_______ 。
(4)若装置A中有NO2气体生成,则装置B中的实验现象为_______ 。
(5)若装置A中铜与稀硝酸反应只生成NO气体,写出该反应的离子方程式_______ ,装置B中的实验现象为_______ 。
(6)已知NO2与H2O反应生成HNO2和另一种常见的强酸,写出其反应的化学方程式_______ 。

已知:FeSO4+NO=[Fe(NO)]SO4该反应较缓慢,待生成一定量[Fe(NO)]2+时突显明显棕色。
(1)盛装稀硝酸的仪器名称为:
(2)实验开始前,如何检验A装置的气密性:
(3)实验开始时先将Y形试管向盛有碳酸钙的支管倾斜,缓慢滴入稀硝酸,该实验操作的目的是
(4)若装置A中有NO2气体生成,则装置B中的实验现象为
(5)若装置A中铜与稀硝酸反应只生成NO气体,写出该反应的离子方程式
(6)已知NO2与H2O反应生成HNO2和另一种常见的强酸,写出其反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】图是铜与稀硝酸反应的两个实验装置图,请按要求回答问题:

(1)铜与稀硝酸反应的离子方程式为_____________________________________________ 。
(2)I实验装置中能否证明铜与稀硝酸反应生成的是NO气体_______ (选填“能”或“不能”), 简述理由_____________________________ 。
(3)若用Ⅱ实验装置进行实验,以证明铜与稀硝酸反应生成的气体是NO,则检查气密性的操作是______________________________________________________________________________ 。
(4)在Ⅱ实验装置的烧杯中加入一定体积的稀硝酸,打开止水夹,用注射器慢慢抽取干燥管内的空气,稀硝酸沿着干燥管慢慢上升,直到充满整个干燥管,停止抽拉注射器,关闭止水夹,此时观察干燥管内的现象是________________________________________ ;反应停止后,打开止水夹,用注射器抽取干燥管内的气体(事先已将注射器内原有的空气推出),关闭止水夹后取下注射器,并抽取一定量的空气,此时观察到的现象是____________________________________________ 。
(5)上述实验完成后,将注射器内的气体通入到NaOH溶液中,其目的是_______________ 。

(1)铜与稀硝酸反应的离子方程式为
(2)I实验装置中能否证明铜与稀硝酸反应生成的是NO气体
(3)若用Ⅱ实验装置进行实验,以证明铜与稀硝酸反应生成的气体是NO,则检查气密性的操作是
(4)在Ⅱ实验装置的烧杯中加入一定体积的稀硝酸,打开止水夹,用注射器慢慢抽取干燥管内的空气,稀硝酸沿着干燥管慢慢上升,直到充满整个干燥管,停止抽拉注射器,关闭止水夹,此时观察干燥管内的现象是
(5)上述实验完成后,将注射器内的气体通入到NaOH溶液中,其目的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】物质A经如图所示的过程转化为含氧酸D,请回答下列问题:







(1)若A在常温下为固体单质,B是能使品红溶液褪色的有刺激性气味的无色气体,D为强酸。写出D+碳→B的化学方程式______ 。
(2)若A在常温下为气体单质,将装满气体C的试管倒扣在水槽中,溶液最终充满试管容积的 ,另外
,另外 容积为无色气体。D的浓溶液在常温下可与铜反应并生成C气体,请写出该反应的离子方程式
容积为无色气体。D的浓溶液在常温下可与铜反应并生成C气体,请写出该反应的离子方程式_____ 。
(3)若A在常温下为非金属气态氢化物,B遇到空气变成红棕色。写出B生成C的化学方程式______ 。
(4)若A在常温下为固体单质,与A同族的某元素的化合物M可用于制造高性能的现代通讯材料光导纤维,易与M发生化学反应的酸是______ 。







(1)若A在常温下为固体单质,B是能使品红溶液褪色的有刺激性气味的无色气体,D为强酸。写出D+碳→B的化学方程式
(2)若A在常温下为气体单质,将装满气体C的试管倒扣在水槽中,溶液最终充满试管容积的
 ,另外
,另外 容积为无色气体。D的浓溶液在常温下可与铜反应并生成C气体,请写出该反应的离子方程式
容积为无色气体。D的浓溶液在常温下可与铜反应并生成C气体,请写出该反应的离子方程式(3)若A在常温下为非金属气态氢化物,B遇到空气变成红棕色。写出B生成C的化学方程式
(4)若A在常温下为固体单质,与A同族的某元素的化合物M可用于制造高性能的现代通讯材料光导纤维,易与M发生化学反应的酸是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】用如图方法回收废旧CPU中的单质Au(金)、Ag和Cu。

已知:①浓硝酸不能单独将Au溶解;
②HAuCl4=H++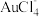 。
。
(1)酸溶时选稀、浓硝酸均可,写出稀HNO3溶解Cu的离子方程式:_______ 。
(2)HNO3-NaCl与王水[V(浓硝酸)∶V浓盐酸=1∶3溶金原理相同,请将溶金反应的化学方程式补充完整:______
Au+_______NaCl+_______HNO3=HAuCl4+_______NO+_______NaNO3+_______
(3)若用Zn粉将溶液中的1 mol HAuCl4完全还原,则参加反应的Zn的物质的量是_______ mol。
(4)用适当浓度的盐酸、NaCl溶液、氨水与铁粉,可按照如图方法从酸溶后的溶液中回收Cu和Ag(图中标注的试剂和物质均不同)。
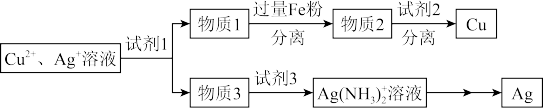
已知AgCl沉淀可溶于氨水:AgCl+2NH3=Ag(NH3) +Cl-
+Cl-
①试剂1是_______ ,②物质2是_______ 。

已知:①浓硝酸不能单独将Au溶解;
②HAuCl4=H++
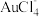 。
。(1)酸溶时选稀、浓硝酸均可,写出稀HNO3溶解Cu的离子方程式:
(2)HNO3-NaCl与王水[V(浓硝酸)∶V浓盐酸=1∶3溶金原理相同,请将溶金反应的化学方程式补充完整:
Au+_______NaCl+_______HNO3=HAuCl4+_______NO+_______NaNO3+_______
(3)若用Zn粉将溶液中的1 mol HAuCl4完全还原,则参加反应的Zn的物质的量是
(4)用适当浓度的盐酸、NaCl溶液、氨水与铁粉,可按照如图方法从酸溶后的溶液中回收Cu和Ag(图中标注的试剂和物质均不同)。
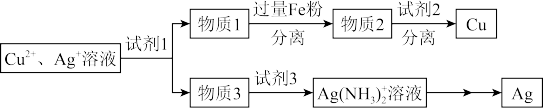
已知AgCl沉淀可溶于氨水:AgCl+2NH3=Ag(NH3)
 +Cl-
+Cl-①试剂1是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】氨氧化法是工业生产中制取硝酸的主要途径。某兴趣小组在实验室利用如下装置模拟氨氧化法制硝酸,通过观察装置 中溶液颜色变化检验硝酸的生成。
中溶液颜色变化检验硝酸的生成。

已知: 和
和 溶液不反应,
溶液不反应, 。
。
回答下列问题:
(1)组装好装置后,下一步应进行的操作为___________ 。装置B中的试剂名称为___________ 。
(2)实验时,点燃C中的酒精灯应在鼓入空气之___________ (填“前”或“后”),装置C中发生反应的化学方程式为___________ 。
(3)装置D的作用为___________ 。反应开始后,装置E中可观察到的现象为___________ 。
(4)将装置 替换为装置
替换为装置 更好,原因是
更好,原因是___________ 。
 中溶液颜色变化检验硝酸的生成。
中溶液颜色变化检验硝酸的生成。
已知:
 和
和 溶液不反应,
溶液不反应, 。
。回答下列问题:
(1)组装好装置后,下一步应进行的操作为
(2)实验时,点燃C中的酒精灯应在鼓入空气之
(3)装置D的作用为
(4)将装置
 替换为装置
替换为装置 更好,原因是
更好,原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】PdCl2广泛用作催化剂和一些物质的检测试剂。由Pd(NH3)2Cl2制备PdCl2工艺流程如图所示。

(1)肼(N2H4)可以被看作二元弱碱,结合质子生成N2H5+或N2H62+。肼与少量稀硫酸混合后,得到产物的化学式为_____________ 。
(2)对工艺流程图中的滤液处理办法最好的是:______
a.返到提钯废液中,循环使用 b.转化为无毒物质后排放 c.深埋于地下
(3)王水溶钯时,Pd被氧化为H2PdCl4。同时得到唯一还原产物亚硝酰氯(NOCl)。反应消耗的HCl与HNO3的物质的量之比为_____ 。
(4)赶硝,是将残余的NO3-浓度降低到不大于0.04%。实验数据记录如下:

处理1吨Pd,需要用到HCl和MxOy的总体积至少为_______ m3(合理选择表格里相关数据计算)。
(5)煅烧过程发生分解反应,化学方程式为:_______________________________ 。
(6)浸有磷钼酸铵溶液的氯化钯试纸遇微量CO立即变成蓝色。原理较为复杂,第一步是CO还原PdCl2得到Pd单质,同时有常见的氧化物生成。 写出反应原理中第一步的化学方程式:_________________________________

(1)肼(N2H4)可以被看作二元弱碱,结合质子生成N2H5+或N2H62+。肼与少量稀硫酸混合后,得到产物的化学式为
(2)对工艺流程图中的滤液处理办法最好的是:
a.返到提钯废液中,循环使用 b.转化为无毒物质后排放 c.深埋于地下
(3)王水溶钯时,Pd被氧化为H2PdCl4。同时得到唯一还原产物亚硝酰氯(NOCl)。反应消耗的HCl与HNO3的物质的量之比为
(4)赶硝,是将残余的NO3-浓度降低到不大于0.04%。实验数据记录如下:

处理1吨Pd,需要用到HCl和MxOy的总体积至少为
(5)煅烧过程发生分解反应,化学方程式为:
(6)浸有磷钼酸铵溶液的氯化钯试纸遇微量CO立即变成蓝色。原理较为复杂,第一步是CO还原PdCl2得到Pd单质,同时有常见的氧化物生成。 写出反应原理中第一步的化学方程式:
您最近一年使用:0次



