请回答下列问题:
(1)据报道,科研人员应用电子计算机模拟出来类似 的物质
的物质 ,试推测下列有关
,试推测下列有关 的说法正确的是
的说法正确的是___________ 。
a. 易溶于水
易溶于水
b. 是一种分子晶体,有较高的熔点和硬度
是一种分子晶体,有较高的熔点和硬度
c. 的熔点高于
的熔点高于
d. 的稳定性比
的稳定性比 的强
的强
(2)已知碘晶胞结构如图所示,请回答下列问题:
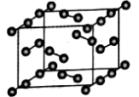
①碘晶体属于___________ 晶体。
②碘晶体熔化过程中克服的作用力为___________ 。
③假设碘晶胞中立方体的边长为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则碘单质的密度为
,则碘单质的密度为___________ 。
(1)据报道,科研人员应用电子计算机模拟出来类似
 的物质
的物质 ,试推测下列有关
,试推测下列有关 的说法正确的是
的说法正确的是a.
 易溶于水
易溶于水b.
 是一种分子晶体,有较高的熔点和硬度
是一种分子晶体,有较高的熔点和硬度c.
 的熔点高于
的熔点高于
d.
 的稳定性比
的稳定性比 的强
的强(2)已知碘晶胞结构如图所示,请回答下列问题:

①碘晶体属于
②碘晶体熔化过程中克服的作用力为
③假设碘晶胞中立方体的边长为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则碘单质的密度为
,则碘单质的密度为
20-21高二·全国·课时练习 查看更多[3]
(人教版2019)选择性必修2 第三章 晶体结构与性质 第二节 分子晶体与共价晶体 第1课时 分子晶体鲁科版2019选择性必修2第3章 不同聚集状态的物质与性质 第2节 几种简单的晶体结构模型 第4课时 分子晶体晶体结构的复杂性(已下线)【知识图鉴】单元讲练测选择性必修2第三章01讲核心
更新时间:2021-02-01 22:15:06
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】获得晶体的途径
(1)实验探究
(2)获得晶体的三条途径
①_____________ 物质凝固。
②_____________ 物质冷却不经液态直接________ (凝华)。
③_____________ 从溶液中析出。
(1)实验探究
实验内容 | 实验操作及现象 |
获取硫黄晶体 | 硫黄粉 熔融态硫 熔融态硫 |
获取碘晶体 |  加热时,烧杯内产生大量 |
获取氯化钠晶体 | 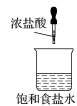 在烧杯底部慢慢析出立方体的 |
①
②
③
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】硅因为具有半导体的性质被认为是一种比较特殊的非金属元素,它的单质是硬度较大的非金属单质。铬单质为钢灰色金属,是自然界硬度最大的金属。
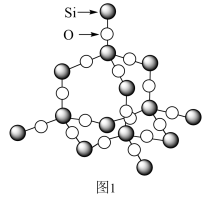
(1)若铬的一种同位素原子核内有28个中子,试写出该同位素原子的原子符号,写出基态铬原子的核外电子排布_______ 。
(2)与硅同周期的金属第一电离能由大到小排列:_______ 。与硅同周期的非金属电负性由小到大排列:_______ 。
(3)图2为二氧化硅的晶胞示意图,由图可知,二氧化硅是_______ (选填“原子晶体”、“分子晶体”或“离子晶体”,下同)。与硅同主族的元素碳的氧化物干冰是_______ 。1mol二氧化硅晶体所含有的σ键个数为_______ 。1mol的乙炔含有π键的个数为_______ 。
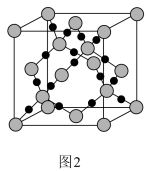
(4)已知二氧化硅的晶胞参数为anm,计算SiO2的密度_______ g/cm3。(列出计算式)

(1)若铬的一种同位素原子核内有28个中子,试写出该同位素原子的原子符号,写出基态铬原子的核外电子排布
(2)与硅同周期的金属第一电离能由大到小排列:
(3)图2为二氧化硅的晶胞示意图,由图可知,二氧化硅是

(4)已知二氧化硅的晶胞参数为anm,计算SiO2的密度
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】D、E、X、Y、Z是周期表中的前20号元素,且原子序数逐渐增大,它们的最简单氢化物分子的空间结构依次是正四面体、三角锥形、正四面体、角形(V形)、直线型,回答下列问题:
(1)Y的最高价氧化物的化学式为______________ 。
(2)上述5种元素中,能形成酸性最强的含氧酸的元素是____________ (填元素符号),写出该元素的任意3种含氧酸的化学式:_______________________ 。
(3)D和Y形成的化合物,其分子的空间构型为________________ 。
(4)D和X形成的化合物,其化学键类型属_______________ ,其晶体类型属________ 。
(5)金属镁和E的单质在高温下反应得到的产物是__________ ,此产物与水反应生成两种碱,该反应的化学方程式是___________________________ 。
(6)试比较D和X的最高价氧化物熔点的高低,并说明理由:________________ 。
(1)Y的最高价氧化物的化学式为
(2)上述5种元素中,能形成酸性最强的含氧酸的元素是
(3)D和Y形成的化合物,其分子的空间构型为
(4)D和X形成的化合物,其化学键类型属
(5)金属镁和E的单质在高温下反应得到的产物是
(6)试比较D和X的最高价氧化物熔点的高低,并说明理由:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】钛、铁、钴、镍等金属及其化合物在科学研究和工业生产中应用十分广泛。回答下列问题:
(1)基态钴原子的价层电子排布式为___________ ,铁、钴、镍的基态原子核外未成对电子数最少的是___________ (填元素名称)。
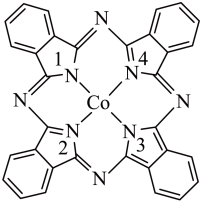
(2)酞菁钴分子的结构简式如图所示,中心离子为钴离子,酞菁钴分子中与钴离子通过配位键结合的氮原子的编号是___________ ;酞菁钴分子中所含三种非金属元素的电负性由大到小的顺序为___________ (用相应的元素符号表示);碳原子的杂化轨道类型为___________ 。
(3)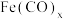 ,常温下呈液态,熔点为
,常温下呈液态,熔点为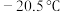 。沸点为103℃。易溶于非极性溶剂,据此可判断
。沸点为103℃。易溶于非极性溶剂,据此可判断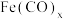 晶体属于
晶体属于___________ (填晶体类型),若配合物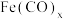 的中心原子价电子数与配体提供电子数之和为18,则
的中心原子价电子数与配体提供电子数之和为18,则
___________ 。
(4)在相同条件下。 比
比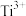 的水解能力更强,原因是
的水解能力更强,原因是___________ 。
(1)基态钴原子的价层电子排布式为
(2)酞菁钴分子的结构简式如图所示,中心离子为钴离子,酞菁钴分子中与钴离子通过配位键结合的氮原子的编号是

(3)
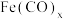 ,常温下呈液态,熔点为
,常温下呈液态,熔点为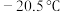 。沸点为103℃。易溶于非极性溶剂,据此可判断
。沸点为103℃。易溶于非极性溶剂,据此可判断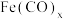 晶体属于
晶体属于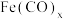 的中心原子价电子数与配体提供电子数之和为18,则
的中心原子价电子数与配体提供电子数之和为18,则
(4)在相同条件下。
 比
比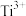 的水解能力更强,原因是
的水解能力更强,原因是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】回答下列问题:
(1)某种金属互化物具有自范性,原子在三维空间呈周期性有序排列,该金属互化物属于______ (填“晶体”或“非晶体”),可通过______ 方法鉴别。
(2) 基态核外电子排布式为
基态核外电子排布式为______
(3)苯胺(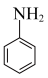 )与甲苯(
)与甲苯(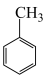 )的相对分子质量相近,但苯胺的沸点高于甲苯,其原因是
)的相对分子质量相近,但苯胺的沸点高于甲苯,其原因是______ 。
(4) 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为______ 。
(5)某含铬化合物立方晶胞如图所示。与钙原子最近且等距离的氧原子有______ 个;钙和氧的最近距离为 ,NA为阿伏加德罗常数值,则该晶体密度为
,NA为阿伏加德罗常数值,则该晶体密度为______  (用含
(用含 、
、 的代数式表示)。
的代数式表示)。
(1)某种金属互化物具有自范性,原子在三维空间呈周期性有序排列,该金属互化物属于
(2)
 基态核外电子排布式为
基态核外电子排布式为(3)苯胺(
 )与甲苯(
)与甲苯( )的相对分子质量相近,但苯胺的沸点高于甲苯,其原因是
)的相对分子质量相近,但苯胺的沸点高于甲苯,其原因是(4)
 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为(5)某含铬化合物立方晶胞如图所示。与钙原子最近且等距离的氧原子有
 ,NA为阿伏加德罗常数值,则该晶体密度为
,NA为阿伏加德罗常数值,则该晶体密度为 (用含
(用含 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
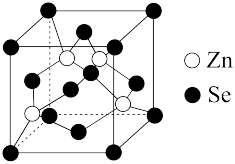
【推荐3】硒( )在电子工业中可用于光电管、太阳能电池,硒元素可形成多种化合物。
)在电子工业中可用于光电管、太阳能电池,硒元素可形成多种化合物。
(1)单质硒的熔点为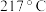 ,它属于
,它属于___________ 晶体。
(2)基态硒原子中,核外电子占据的最高能级的符号是___________ 。
(3)与硒元素相邻的同周期元素有砷和溴,这三种元素的第一电离能由小到大的顺序为___________ (用元素符号表示)。
(4) 的立体构型是
的立体构型是___________ ;与 互为等电子体的分子有
互为等电子体的分子有___________ (写一种物质的化学式即可)。
(5) 水溶液比
水溶液比 水溶液的酸性强,原因是
水溶液的酸性强,原因是___________ 。
(6)硒化锌是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为___________ 。
 )在电子工业中可用于光电管、太阳能电池,硒元素可形成多种化合物。
)在电子工业中可用于光电管、太阳能电池,硒元素可形成多种化合物。(1)单质硒的熔点为
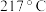 ,它属于
,它属于(2)基态硒原子中,核外电子占据的最高能级的符号是
(3)与硒元素相邻的同周期元素有砷和溴,这三种元素的第一电离能由小到大的顺序为
(4)
 的立体构型是
的立体构型是 互为等电子体的分子有
互为等电子体的分子有(5)
 水溶液比
水溶液比 水溶液的酸性强,原因是
水溶液的酸性强,原因是(6)硒化锌是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为

您最近一年使用:0次



