下列说法正确的是
| A.升高温度,活化分子百分数增加,化学反应速率一定增大 |
| B.使用催化剂,活化能升高,反应速率加快 |
| C.活化分子间所发生的碰撞为有效碰撞 |
| D.加入反应物,使活化分子百分数增加,化学反应速率增大 |
19-20高二下·湖南湘潭·期中 查看更多[3]
新疆喀什市2023-2024学年高二上学期期中考试化学试题(已下线)2.1.3 活化能(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)湖南省湘潭电机子弟中学2019-2020学年高二下学期期中考试化学(理)试题
更新时间:2021-02-08 20:06:10
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】工业合成氨是人类科学技术的一项重大突破。其合成原理为:
 ,下列说法不正确的是
,下列说法不正确的是

 ,下列说法不正确的是
,下列说法不正确的是| A.增大压强,活化分子百分含量不变,单位体积内活化分子增多,反应速率加快 |
| B.该反应在低温下能自发进行 |
| C.为了防止混有的杂质使催化剂“中毒”,原料气必须经过净化 |
| D.能用勒夏特列原理解释通常采用500℃有利于氨的合成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.用含有少量硫酸铜的稀硫酸跟锌粒反应,能加快产生氢气,说明Cu2+具有催化能力 |
| B.增大浓度会加快化学反应速率,是因为增加了反应物单位体积内活化分子的百分数 |
| C.等体积、pH都为3的酸HA和HB分别与足量的锌反应,HA放出的氢气多,说明酸性:HA<HB |
| D.碱性锌锰电池是一种常见的二次电池 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】一定温度下,某反应达到了化学平衡,其反应过程对应的能量变化如图。下列说法不正确的是


| A.Ea 为正反应活化能,Ea'为逆反应活化能 |
| B.该反应为放热反应,△H=Ea-Ea' |
| C.温度升高,降低反应活化能,化学反应速率增大 |
| D.所有活化分子的平均能量高于所有分子的平均能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
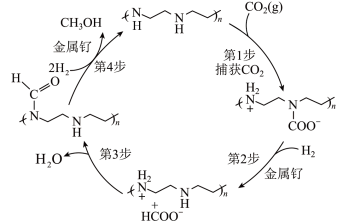
【推荐2】科学家致力于将大气中过多的 转化为有益于人类的物质,一种从空气中捕获
转化为有益于人类的物质,一种从空气中捕获 转化为甲醇的反应历程如图所示。下列说法错误的是
转化为甲醇的反应历程如图所示。下列说法错误的是
 转化为有益于人类的物质,一种从空气中捕获
转化为有益于人类的物质,一种从空气中捕获 转化为甲醇的反应历程如图所示。下列说法错误的是
转化为甲醇的反应历程如图所示。下列说法错误的是
A.该过程的总反应为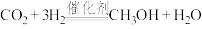 |
B.第1步反应的原子利用率为 |
| C.第4步反应中有极性键和非极性键的断裂和形成 |
| D.金属钌通过降低该反应的活化能提高反应速率 |
您最近一年使用:0次

 ;②
;② ,其反应过程能量如图所示,下列说法正确的是
,其反应过程能量如图所示,下列说法正确的是

 ,反应②速率大于反应①,气体B很难大量积累
,反应②速率大于反应①,气体B很难大量积累

