(1)下列说法正确的是_______ (填字母序号)。
A.化学反应的实质就是旧化学键的断裂,新化学键的形成,在化学反应中,反应物转化为生成物的同时,必然伴随着能量的变化
B.钢铁生锈腐蚀时,铁被氧化
C.放热反应发生时,不一定要加热。但吸热反应必须要加热才能发生
(2)在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气完全燃烧的热化学方程式表示为_______ 。
(3)目前工业上有一种方法是用CO2来生产甲醇:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)。如图1表示该反应进行过程中能量的变化(单位为:kJ·mol-1),该反应是△H_______ 0(选填“>”“=”或“<”)。

(4)图2装置属于原电池的是_____ (填序号)。在选出的原电池中,_____ 是负极,发生____ (选填“氧化”或“还原”)反应,正极的现象____ 。此原电池反应的化学方程式为_____ 。
A.化学反应的实质就是旧化学键的断裂,新化学键的形成,在化学反应中,反应物转化为生成物的同时,必然伴随着能量的变化
B.钢铁生锈腐蚀时,铁被氧化
C.放热反应发生时,不一定要加热。但吸热反应必须要加热才能发生
(2)在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气完全燃烧的热化学方程式表示为
(3)目前工业上有一种方法是用CO2来生产甲醇:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)。如图1表示该反应进行过程中能量的变化(单位为:kJ·mol-1),该反应是△H

(4)图2装置属于原电池的是
更新时间:2021-02-20 22:31:33
|
相似题推荐
【推荐1】从能量变化和反应快慢等角度研究反应具有重要意义。下列实验可以检验反应中的能量变化。
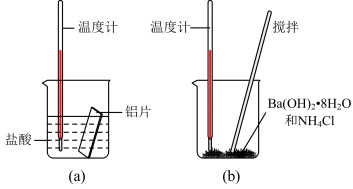
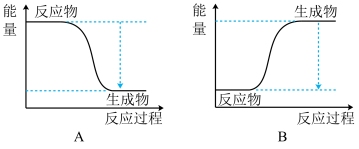
(1)下图能正确表示实验(a)反应中能量变化的是___________ (填序号)。
实验(b)中发生反应的化学方程式为___________ 。
(2)若将实验(a)中的反应设计成原电池,正极反应为___________ ;若转移了0.6mol电子,参加反应的负极材料是___________ g。
(3)一定温度下,将3mol A气体和1mol B气体通入2L容积固定的密闭容器中,发生如下反应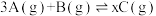 ,反应1min时测得剩余1.8mol A,C的浓度为0.4
,反应1min时测得剩余1.8mol A,C的浓度为0.4 ,则1min内,B的平均反应速率为
,则1min内,B的平均反应速率为___________  ;若反应经2min达到平衡,平衡时C的浓度
;若反应经2min达到平衡,平衡时C的浓度___________ 0.8 (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。

(1)下图能正确表示实验(a)反应中能量变化的是

实验(b)中发生反应的化学方程式为
(2)若将实验(a)中的反应设计成原电池,正极反应为
(3)一定温度下,将3mol A气体和1mol B气体通入2L容积固定的密闭容器中,发生如下反应
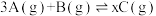 ,反应1min时测得剩余1.8mol A,C的浓度为0.4
,反应1min时测得剩余1.8mol A,C的浓度为0.4 ,则1min内,B的平均反应速率为
,则1min内,B的平均反应速率为 ;若反应经2min达到平衡,平衡时C的浓度
;若反应经2min达到平衡,平衡时C的浓度 (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。
您最近半年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐2】甲烷和氯气都是重要的化工原料。
I.CH4在光照条件下与C12反应,可得到各种氯代甲烷。
(1)CH4氯代的机理为自由基(带有单电子的原子或原子团,如C1·、·CH3)反应,包括以下几步:
写出由CH3Cl生成CH2Cl2过程中链传递的方程式:_______ ,_______ 。
(2)丙烷氯代反应中链传递的一步反应能量变化如下。

推知−CH3中C−H键能比-CH2-中C−H键能_______ (填“大”或“小”)。
II.甲烷重整制合成气,主要反应如下:
i.CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH1
ii.CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH2
各反应平衡常数与温度的关系如图。
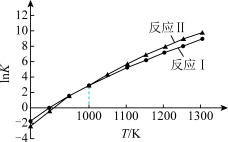
(3)①假设ΔH、ΔS不随温度变化,平衡常数与温度间存在的关系为:lnK1−lnK2= (
( −
− ),R为正常数。则ΔH1
),R为正常数。则ΔH1_______ 0(填“>”或“<”);ΔH1_______ ΔH2(填“>”或“<”)。
②通过调整投料比可调控平衡时合成气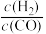 的值。1000K,平衡时
的值。1000K,平衡时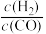 =2,则
=2,则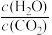 =
=_______ ,应控制投料比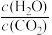 =
=_______ 。
III.氯碱工业是化工产业的重要基础,其装置示意图如图。

(4)X为_______ ,Y为_______ 。(写化学式)
(5)淡盐水中含少量的HClO,阴极区生成NaOH的物质的量小于氢气的两倍,下列关于造成NaOH的物质的量小于氢气的两倍的原因中合理的是_______ (填序号)。
a.Cl-在电极上放电,产生HClO
b.有H+穿过阳离子交换膜
c.阳离子交换膜破损导致OH-向阳极区迁移
d.O2在阴极放电
I.CH4在光照条件下与C12反应,可得到各种氯代甲烷。
(1)CH4氯代的机理为自由基(带有单电子的原子或原子团,如C1·、·CH3)反应,包括以下几步:
| I.链引发 | II.链传递 | III.链终止 |
Cl2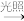 2Cl∙ 2Cl∙ | Cl∙+CH4→∙CH3+HCl ∙CH3+Cl2→CH3Cl+Cl∙ …… | 2Cl∙→Cl2 Cl∙+∙CH3→CH3Cl …… |
写出由CH3Cl生成CH2Cl2过程中链传递的方程式:
(2)丙烷氯代反应中链传递的一步反应能量变化如下。

推知−CH3中C−H键能比-CH2-中C−H键能
II.甲烷重整制合成气,主要反应如下:
i.CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH1
ii.CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH2
各反应平衡常数与温度的关系如图。

(3)①假设ΔH、ΔS不随温度变化,平衡常数与温度间存在的关系为:lnK1−lnK2=
 (
( −
− ),R为正常数。则ΔH1
),R为正常数。则ΔH1②通过调整投料比可调控平衡时合成气
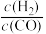 的值。1000K,平衡时
的值。1000K,平衡时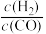 =2,则
=2,则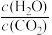 =
=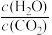 =
=III.氯碱工业是化工产业的重要基础,其装置示意图如图。

(4)X为
(5)淡盐水中含少量的HClO,阴极区生成NaOH的物质的量小于氢气的两倍,下列关于造成NaOH的物质的量小于氢气的两倍的原因中合理的是
a.Cl-在电极上放电,产生HClO
b.有H+穿过阳离子交换膜
c.阳离子交换膜破损导致OH-向阳极区迁移
d.O2在阴极放电
您最近半年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
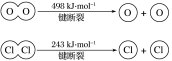
【推荐3】(1)某实验小组同学进行如图所示实验,以检验化学反应中的能量变化。
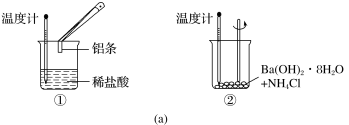
实验发现,反应后①中的温度升高,②中的温度降低。由此判断铝条与盐酸的反应是__ (填“吸热”或“放热”,下同)反应,Ba(OH)2·8H2O与NH4Cl的反应是__ 反应。反应__ (填“①”或“②”)的能量变化可用图(b)表示。
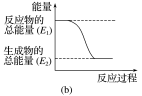
(2)已知:4HCl+O2=2Cl2+2H2O,该反应中,4mol HCl被氧化,放出115.6kJ的热量,则断开1mol H-O键与断开1mol H-Cl键所需能量相差约为__ kJ。

实验发现,反应后①中的温度升高,②中的温度降低。由此判断铝条与盐酸的反应是

(2)已知:4HCl+O2=2Cl2+2H2O,该反应中,4mol HCl被氧化,放出115.6kJ的热量,则断开1mol H-O键与断开1mol H-Cl键所需能量相差约为

您最近半年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐1】Ⅰ.在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ·mol -1表示。请认真观察图像,然后回答问题。
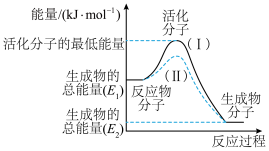
(1)图中反应的ΔH=___________ (用含E1、E2的代数式表示)。
(2)下列反应中,符合示意图描述的反应的是___________ (填字母)。
a.铝与盐酸反应 b.生石灰溶于水 c.盐酸与碳酸氢钠反应
d.高温煅烧石灰石 e.浓硫酸溶于水 f.3H(g)+N(g)→NH3(g)
(3)曲线Ⅱ改变的条件是___________ ,从有效碰撞的角度解释其可以加快反应速率的原因___________ 。
(4)已知N2(g) +2O2(g)=2NO2(g) ΔH = +67.7 kJ ·mol-1,
N2H4(g) +O2(g)= N2 (g) +2H2O(g) ΔH =-534 kJ·mol-1,
则N2H4(g) 与NO2(g)完全反应生成N2(g)和H2O(g)的热化学方程式为___________ 。
(5)氨气是一种重要的物质,可用于制取化肥和硝酸等。已知H-H键、N- H键、N ≡N键的键能分别是436 kJ·mol-1、391 kJ·mol-1、946 kJ·mol-1,写出合成氨的热化学方程式:___________ ;1molN2完全反应时,正反应活化能为335 kJ·mol-1,则其逆反应的活化能为___________ kJ·mol-1;若0.5molN2和足量的H2在一定条件下充分反应吸收或放出的热量___________ (填大于、小于或等于)生成1molNH3所吸收或放出的热量。
(6)已知:在101 kPa时,16g CH3OH(l)与足量氧气反应,生成液态水,并放出363kJ的热量,表示甲醇燃烧热的热化学方程式为___________ 。
Ⅱ.中和热的测定:
测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。
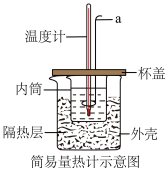
(7)仪器a的名称为___________ 。
(8)取50mL NaOH溶液和30mL硫酸溶液进行实验,实验数据如表。
①请填写表中的空白:
②近似认为0.50mol/L NaOH溶液和0.50mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g·℃)。则中和热ΔH=___________ (取小数点后一位)。
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是___________ (填字母)。
a.实验装置保温、隔热效果差
b.配制0.50mol/LNaOH溶液时俯视刻度线读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定硫酸溶液的温度
e.用量筒量取NaOH溶液的体积时仰视读数

(1)图中反应的ΔH=
(2)下列反应中,符合示意图描述的反应的是
a.铝与盐酸反应 b.生石灰溶于水 c.盐酸与碳酸氢钠反应
d.高温煅烧石灰石 e.浓硫酸溶于水 f.3H(g)+N(g)→NH3(g)
(3)曲线Ⅱ改变的条件是
(4)已知N2(g) +2O2(g)=2NO2(g) ΔH = +67.7 kJ ·mol-1,
N2H4(g) +O2(g)= N2 (g) +2H2O(g) ΔH =-534 kJ·mol-1,
则N2H4(g) 与NO2(g)完全反应生成N2(g)和H2O(g)的热化学方程式为
(5)氨气是一种重要的物质,可用于制取化肥和硝酸等。已知H-H键、N- H键、N ≡N键的键能分别是436 kJ·mol-1、391 kJ·mol-1、946 kJ·mol-1,写出合成氨的热化学方程式:
(6)已知:在101 kPa时,16g CH3OH(l)与足量氧气反应,生成液态水,并放出363kJ的热量,表示甲醇燃烧热的热化学方程式为
Ⅱ.中和热的测定:
测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。

(7)仪器a的名称为
(8)取50mL NaOH溶液和30mL硫酸溶液进行实验,实验数据如表。
①请填写表中的空白:
| 温度 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差平均值(t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是
a.实验装置保温、隔热效果差
b.配制0.50mol/LNaOH溶液时俯视刻度线读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定硫酸溶液的温度
e.用量筒量取NaOH溶液的体积时仰视读数
您最近半年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐2】(1)在25℃、101kPa下,4g甲烷完全燃烧生成CO2和液态H2O,放出220kJ的热量,写出表示甲烷燃烧热的热化学方程式:__ 。
(2)2Zn(s)+O2(g)=2ZnO(s) ΔH1=-702.2kJ/mol
2Hg(1)+O2(g)=2HgO(s) ΔH2=-181.4kJ/mol
由此可知ZnO(s)+Hg(1)=Zn(s)+HgO(s) ΔH3=__ 。
(3)已知2SO2(g)+O2(g)⇌2SO3(g)反应过程的能量变化如图所示。已知1molSO2(g)氧化为lmolSO3(g)的ΔH=-99kJ/mol,请回答下列问题:

①图中ΔH=__ kJ/mol;
②降低温度,该反应K值__ ,SO2转化率__ ;化学反应速率__ (以上均填“增大”“减小”或“不变”)。
(2)2Zn(s)+O2(g)=2ZnO(s) ΔH1=-702.2kJ/mol
2Hg(1)+O2(g)=2HgO(s) ΔH2=-181.4kJ/mol
由此可知ZnO(s)+Hg(1)=Zn(s)+HgO(s) ΔH3=
(3)已知2SO2(g)+O2(g)⇌2SO3(g)反应过程的能量变化如图所示。已知1molSO2(g)氧化为lmolSO3(g)的ΔH=-99kJ/mol,请回答下列问题:

①图中ΔH=
②降低温度,该反应K值
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】X、Y、Z、W代表原子序数依次增大的四种短周期元素,X原子核内没有中子,在周期表中,Z与Y﹑W均相邻,Y﹑Z和W三种元素的原子最外层电子数之和为17,且Z﹑W最外层电子数相同。
(1)用电子式表示X与Y所组成化合物的形成过程_________________ 。
(2)W在周期表中的位置是____________________ 。
(3)已知,在101kPa时,X单质在1.00molO2中完全燃烧生成2.00mol液态H2O,放出571.6kJ的热量,则表示X单质燃烧热的热化学方程式为__________ 。
(1)用电子式表示X与Y所组成化合物的形成过程
(2)W在周期表中的位置是
(3)已知,在101kPa时,X单质在1.00molO2中完全燃烧生成2.00mol液态H2O,放出571.6kJ的热量,则表示X单质燃烧热的热化学方程式为
您最近半年使用:0次
解答题-原理综合题
|
较易
(0.85)
真题
解题方法
【推荐1】磷酸二氢钾在工农业生产及国防工业等领域都有广泛的应用。某研究小组用质量分数为85%的磷酸与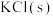 反应制备
反应制备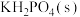 ,反应方程式为
,反应方程式为 一定条件下的实验结果如图1所示。
一定条件下的实验结果如图1所示。
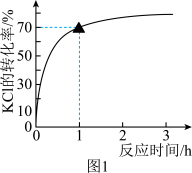
回答问题:
(1)该条件下,反应至1h时KCl的转化率为_______ 。
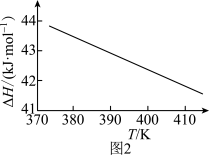
(2)该制备反应的 随温度变化关系如图2所示。该条件下反应为
随温度变化关系如图2所示。该条件下反应为_______ 反应(填“吸热”或“放热”),且反应热随温度升高而_______ 。
(3)该小组为提高转化率采用的措施中有:使用浓磷酸作反应物、向系统中不断通入水蒸气等。它们能提高转化率的原因是:不使用稀磷酸_______ ;通入水蒸气_______ 。
(4)298K时,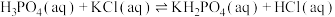 的平衡常数
的平衡常数
_______ 。(已知 的
的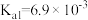 )
)
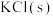 反应制备
反应制备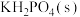 ,反应方程式为
,反应方程式为 一定条件下的实验结果如图1所示。
一定条件下的实验结果如图1所示。
回答问题:
(1)该条件下,反应至1h时KCl的转化率为
(2)该制备反应的
 随温度变化关系如图2所示。该条件下反应为
随温度变化关系如图2所示。该条件下反应为
(3)该小组为提高转化率采用的措施中有:使用浓磷酸作反应物、向系统中不断通入水蒸气等。它们能提高转化率的原因是:不使用稀磷酸
(4)298K时,
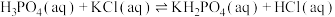 的平衡常数
的平衡常数
 的
的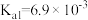 )
)
您最近半年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐2】按要求回答下列问题:
(1)下列变化中属于吸热反应的是_______ 。
①铝片与稀盐酸的反应 ②将胆矾加热变为白色粉末 ③干冰汽化 ④氯酸钾分解制氧气 ⑤甲烷在氧气中的燃烧反应
(2)反应C(s)+H2O(g) CO(g)+H2(g)在一个容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
CO(g)+H2(g)在一个容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是_______ 。
①增加C的量
②将容器的体积缩小一半
③保持体积不变,充入N2使体系压强增大
④保持压强不变,充入N2使容器体积变大
(3)在体积为1L的密闭容器中,充入1molCO2和3molH2,一定条件下反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图:
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图:

①从3min到9min,v(CO2)=_______ (结果保留两位有效数字);a点时v(正)_______ v(逆)(填>、<或=)。
②若已知生成标准状况下2.24LCH3OH(g)时放出热量为4.9kJ,而上述反应的实际放热量总小于49kJ,其原因是_______ 。
(4)微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理如图所示。
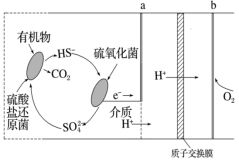
①该微生物燃料电池,负极为_______ (填“a”或“b”)。
②该电池正极电极反应式为_______ 。
③当电路中有0.5mol电子发生转移,则有_______ mol的H+通过质子交换膜。
(1)下列变化中属于吸热反应的是
①铝片与稀盐酸的反应 ②将胆矾加热变为白色粉末 ③干冰汽化 ④氯酸钾分解制氧气 ⑤甲烷在氧气中的燃烧反应
(2)反应C(s)+H2O(g)
 CO(g)+H2(g)在一个容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
CO(g)+H2(g)在一个容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是①增加C的量
②将容器的体积缩小一半
③保持体积不变,充入N2使体系压强增大
④保持压强不变,充入N2使容器体积变大
(3)在体积为1L的密闭容器中,充入1molCO2和3molH2,一定条件下反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图:
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图:
①从3min到9min,v(CO2)=
②若已知生成标准状况下2.24LCH3OH(g)时放出热量为4.9kJ,而上述反应的实际放热量总小于49kJ,其原因是
(4)微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理如图所示。

①该微生物燃料电池,负极为
②该电池正极电极反应式为
③当电路中有0.5mol电子发生转移,则有
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】化学反应常伴随热效应。某些反应(如中和反应)的热量变化,其数值Q可通过量热装置测量反应前后体系温度变化,用公式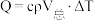 计算获得。
计算获得。
(1)热量的测定:取50 mL 0.5 mol/L盐酸、50 mL 0.55 mol/L NaOH溶液和如图所示装置进行中和热的测定实验。

①从实验装置上看,图中缺少的一种玻璃仪器是___________ 。
②测得反应前后体系的温度值(℃)分别为 、
、 ,则该过程放出的热量为
,则该过程放出的热量为___________ J(c和 分别取
分别取 和
和 )。
)。
③如果改用60 mL 1.0 mol/L盐酸跟50 mL 1.1 mol/L NaOH溶液进行反应,则与上述实验相比,所放热量___________ (填“增加”“减少”或“不变”);所求中和热数值___________ (填“增加”“减少”或“不变”)。
(2)借鉴(1)的方法,甲同学测量放热反应 焓变
焓变 (忽略温度对焓变的影响,下同)。实验结果见下表。
(忽略温度对焓变的影响,下同)。实验结果见下表。
①温度:b___________ c(填“>”“<”或“=”)。
②
___________ (选择表中一组数据计算)。结果表明,该方法可行。
(3)乙同学也借鉴(1)的方法,测量反应A: 的焓变。
的焓变。
查阅资料:配制 溶液时需加入酸。
溶液时需加入酸。
①提出猜想:Fe粉与 溶液混合,在反应A进行的过程中,可能存在Fe粉和酸的反应。
溶液混合,在反应A进行的过程中,可能存在Fe粉和酸的反应。
验证猜想:用pH试纸测得 溶液的pH不大于1;向少量
溶液的pH不大于1;向少量 溶液中加入Fe粉,溶液颜色变浅的同时有气泡冒出,说明存在反应A和
溶液中加入Fe粉,溶液颜色变浅的同时有气泡冒出,说明存在反应A和___________ (用离子方程式表示)。
实验小结:猜想成立,不能直接测反应A的焓变。
教师指导:鉴于以上问题,特别是气体生成带来的干扰,需要设计出实验过程中无气体生成的实验方案。
②优化设计:乙同学根据相关原理,重新设计了优化的实验方案,获得了反应A的焓变。该方案为______________________ 。
(4)化学能可转化为热能,写出其在生产或生活中的一种应用___________ 。
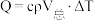 计算获得。
计算获得。(1)热量的测定:取50 mL 0.5 mol/L盐酸、50 mL 0.55 mol/L NaOH溶液和如图所示装置进行中和热的测定实验。

①从实验装置上看,图中缺少的一种玻璃仪器是
②测得反应前后体系的温度值(℃)分别为
 、
、 ,则该过程放出的热量为
,则该过程放出的热量为 分别取
分别取 和
和 )。
)。③如果改用60 mL 1.0 mol/L盐酸跟50 mL 1.1 mol/L NaOH溶液进行反应,则与上述实验相比,所放热量
(2)借鉴(1)的方法,甲同学测量放热反应
 焓变
焓变 (忽略温度对焓变的影响,下同)。实验结果见下表。
(忽略温度对焓变的影响,下同)。实验结果见下表。| 序号 | 反应试剂 | 体系温度/℃ | ||
| 反应前 | 反应后 | |||
| i |   溶液100mL 溶液100mL | 1.20g Fe粉 | a | b |
| ii | 0.56g Fe粉 | a | c | |
②

(3)乙同学也借鉴(1)的方法,测量反应A:
 的焓变。
的焓变。查阅资料:配制
 溶液时需加入酸。
溶液时需加入酸。①提出猜想:Fe粉与
 溶液混合,在反应A进行的过程中,可能存在Fe粉和酸的反应。
溶液混合,在反应A进行的过程中,可能存在Fe粉和酸的反应。验证猜想:用pH试纸测得
 溶液的pH不大于1;向少量
溶液的pH不大于1;向少量 溶液中加入Fe粉,溶液颜色变浅的同时有气泡冒出,说明存在反应A和
溶液中加入Fe粉,溶液颜色变浅的同时有气泡冒出,说明存在反应A和实验小结:猜想成立,不能直接测反应A的焓变。
教师指导:鉴于以上问题,特别是气体生成带来的干扰,需要设计出实验过程中无气体生成的实验方案。
②优化设计:乙同学根据相关原理,重新设计了优化的实验方案,获得了反应A的焓变。该方案为
(4)化学能可转化为热能,写出其在生产或生活中的一种应用
您最近半年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐1】回答下列问题
(1)向某体积固定的密闭容器中加入0.3 A、0.1
A、0.1 C和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体的压强没有变化。请回答:
C和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体的压强没有变化。请回答:
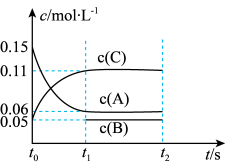
①该密闭容器的体积为_______ 升。
②若t1=15,则t0-t1内用C表示反应速率v(C) =_______ ;
③写出该反应的化学方程式:_______ 。
(2)已知断裂几种化学键要吸收的能量如下:
已知CO2、O2、H2O的结构式分别为O=C=O,O=O,H-O-H。1molCH4在O2中完全燃烧生成气态CO2和气态水时_______ (填“吸收”或 “放出”)热量。
(3)燃料电池是一种高效、环境友好的供电装置,如图为氢气燃料电池的工作原理示意图,a、b均为惰性电极。

①使用时,空气从_______ 口通入(填“A”或“B”);
②a极的电极反应为:_______ 。
(1)向某体积固定的密闭容器中加入0.3
 A、0.1
A、0.1 C和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体的压强没有变化。请回答:
C和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体的压强没有变化。请回答:
①该密闭容器的体积为
②若t1=15,则t0-t1内用C表示反应速率v(C) =
③写出该反应的化学方程式:
(2)已知断裂几种化学键要吸收的能量如下:
| 化学键 | C-H | O=O | C=O | H-O |
| 断裂1mol键吸收的能量/kJ | 415 | 497 | 745 | 463 |
(3)燃料电池是一种高效、环境友好的供电装置,如图为氢气燃料电池的工作原理示意图,a、b均为惰性电极。

①使用时,空气从
②a极的电极反应为:
您最近半年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】研究化学反应的原理,对掌握物质的应用有重要的意义。
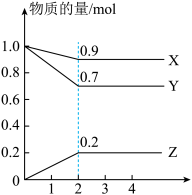
(1)某温度时,在2L容器中X、Y、Z三种物质的量随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式为___________ 。反应开始至2min,Z的平均反应速率为___________ 。
(2)硅是太阳能电池的重要材料。“精炼硅”反应历程中的能量变化如下图所示:
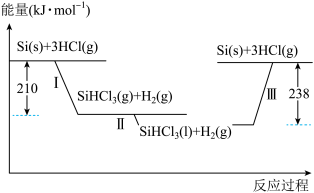
反应I的热化学方程式为___________ 。反应III为___________ (选填“吸热”或“放热”)反应。
(3)FeCl3常用于腐蚀印刷电路铜板(2FeCl3 +Cu=2FeCl2+CuCl2)请将此反应设计成原电池,该原电池负极的电极材料为___________ ,正极的电极材料为___________ ,电解质溶液为___________ ,负极的电极反应式为___________ 。
(1)某温度时,在2L容器中X、Y、Z三种物质的量随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式为

(2)硅是太阳能电池的重要材料。“精炼硅”反应历程中的能量变化如下图所示:

反应I的热化学方程式为
(3)FeCl3常用于腐蚀印刷电路铜板(2FeCl3 +Cu=2FeCl2+CuCl2)请将此反应设计成原电池,该原电池负极的电极材料为
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】高锰酸钾( )是一种常用的氧化剂。回答下列问题:
)是一种常用的氧化剂。回答下列问题:
Ⅰ.某实验小组用未知浓度的酸性 溶液滴定0.1000
溶液滴定0.1000  的标准草酸(
的标准草酸( )溶液,测定
)溶液,测定 溶液的浓度(
溶液的浓度( ,
,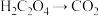 )。实验步骤如下:
)。实验步骤如下:
准确量取20.00 mL标准草酸溶液于锥形瓶中,并加入适量硫酸,用未知浓度的 溶液进行滴定,记录所用体积,平行滴定三次。消耗
溶液进行滴定,记录所用体积,平行滴定三次。消耗 溶液体积如下表所示:
溶液体积如下表所示:
(1) 溶液应装入
溶液应装入______ (填“酸式”或“碱式”)滴定管中。
(2)滴定终点的现象是______ 。
(3)该 溶液的物质的量浓度为
溶液的物质的量浓度为______ ;若锥形瓶用草酸溶液润洗,会导致测定结果______ (填“偏大”或“偏小”)。
Ⅱ.该实验小组运用所学电化学知识设计了如图装置。

(4)盐桥的作用除了形成闭合回路、将反应物隔开外,还能______ 。
(5)闭合开关K并反应一段时间后,盛放酸性 溶液的烧杯中的实验现象为
溶液的烧杯中的实验现象为______ ;该电池的负极电极反应式为______ 。
 )是一种常用的氧化剂。回答下列问题:
)是一种常用的氧化剂。回答下列问题:Ⅰ.某实验小组用未知浓度的酸性
 溶液滴定0.1000
溶液滴定0.1000  的标准草酸(
的标准草酸( )溶液,测定
)溶液,测定 溶液的浓度(
溶液的浓度( ,
,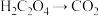 )。实验步骤如下:
)。实验步骤如下:准确量取20.00 mL标准草酸溶液于锥形瓶中,并加入适量硫酸,用未知浓度的
 溶液进行滴定,记录所用体积,平行滴定三次。消耗
溶液进行滴定,记录所用体积,平行滴定三次。消耗 溶液体积如下表所示:
溶液体积如下表所示:实验编号 | 初始读数/mL | 最终读数/mL |
1 | 1.20 | 21.15 |
2 | 1.21 | 24.25 |
3 | 2.11 | 22.16 |
(1)
 溶液应装入
溶液应装入(2)滴定终点的现象是
(3)该
 溶液的物质的量浓度为
溶液的物质的量浓度为Ⅱ.该实验小组运用所学电化学知识设计了如图装置。

(4)盐桥的作用除了形成闭合回路、将反应物隔开外,还能
(5)闭合开关K并反应一段时间后,盛放酸性
 溶液的烧杯中的实验现象为
溶液的烧杯中的实验现象为
您最近半年使用:0次



