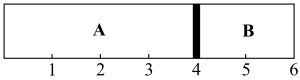
根据所学知识,回答下列问题:
(1)标准状况下,1.7 g NH3的体积为___ L;它与标准状况下____ L CH4含有的氢原子数目相同。
(2)等质量的CO和N2所含分子数之比为____ 。
(3)将11.7 g NaCl固体配成10 L溶液,从中取出50 mL,这50 mL溶液中NaCl的物质的量浓度为____ mol·L-1
(4)34 g某二价金属的氯化物中含有0.5 mol Cl-,则该金属氯化物的摩尔质量为_____ g·mol-1,该金属的相对原子质量为_____ 。
(5)已知SO2、O2混合气体的质量共11.2 g,在标准状况下的体积为4.48 L,则混合气体中SO2的物质的量为_____ 。
(1)标准状况下,1.7 g NH3的体积为
(2)等质量的CO和N2所含分子数之比为
(3)将11.7 g NaCl固体配成10 L溶液,从中取出50 mL,这50 mL溶液中NaCl的物质的量浓度为
(4)34 g某二价金属的氯化物中含有0.5 mol Cl-,则该金属氯化物的摩尔质量为
(5)已知SO2、O2混合气体的质量共11.2 g,在标准状况下的体积为4.48 L,则混合气体中SO2的物质的量为
更新时间:2021-03-01 13:30:41
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】设阿伏加德罗常数的值为6.02×1023。
(1)0.3 mol NH3分子中所含原子数目与___________ 个H2O分子中所含原子数目相等。
(2)在0.5L含有质量为10.8克Al3+的Al2(SO4)3溶液中所含SO 的物质的量浓度为
的物质的量浓度为____ 。
(3)同温、同压下,有五种物质:①6g H2,②0.5 mol CO2,③1.204×1024个氯化氢分子,④147g硫酸,⑤92g乙醇(C2H5OH)。它们的物质的量最大的是______ (填序号,下同),含有原子个数最多的是___ ,质量最大的是___ 。
(4)9.5 g某二价金属氯化物(ACl2)中含有0.2 mol Cl-,则ACl2的摩尔质量是_______ ;A的相对原子质量是______ ;ACl2的化学式是______ 。
(1)0.3 mol NH3分子中所含原子数目与
(2)在0.5L含有质量为10.8克Al3+的Al2(SO4)3溶液中所含SO
 的物质的量浓度为
的物质的量浓度为(3)同温、同压下,有五种物质:①6g H2,②0.5 mol CO2,③1.204×1024个氯化氢分子,④147g硫酸,⑤92g乙醇(C2H5OH)。它们的物质的量最大的是
(4)9.5 g某二价金属氯化物(ACl2)中含有0.2 mol Cl-,则ACl2的摩尔质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】在一定条件下,mgNH4HCO3完全分解生成NH3、CO2、H2O(g)。按要求填空。
(1)若所得混合气体对H2的相对密度为d,则混合气体的物质的量为________ ,NH4HCO3的摩尔质量为________ (用含m、d的代数式表示);
(2)若所得混合气体的密度折合成标准状况为ρ g·L-1,则混合气体的平均摩尔质量为____________ ;
(3)在该条件下,所得NH3、CO2、H2O(g)的体积分数分别为a%、b%、c%,则混合气体的平均相对分子质量为____________________________________________________ 。
(1)若所得混合气体对H2的相对密度为d,则混合气体的物质的量为
(2)若所得混合气体的密度折合成标准状况为ρ g·L-1,则混合气体的平均摩尔质量为
(3)在该条件下,所得NH3、CO2、H2O(g)的体积分数分别为a%、b%、c%,则混合气体的平均相对分子质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】将36.6 g NaOH固体溶于水配成200 mL溶液,其密度为1.219 g·mL-1。
(1)该溶液中NaOH的物质的量浓度为____________ 。
(2)ω % 表示质量百分比浓度、c表示物质的量浓度、ρ表示溶液的密度、M表示溶质的式量,ω % =_____________ (用含有ρ、c、M的字母写出相应的表达式)。
(3)从该溶液中取出10 mL,其中NaOH的物质的量浓度为_______ ,NaOH的质量百分比浓度为_______ ,含NaOH的质量为_______ 。
(1)该溶液中NaOH的物质的量浓度为
(2)ω % 表示质量百分比浓度、c表示物质的量浓度、ρ表示溶液的密度、M表示溶质的式量,ω % =
(3)从该溶液中取出10 mL,其中NaOH的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】取过氧化氢(H2O2)样品10mL,加水配成250mL溶液,从中取出25mL,加稀硫酸酸化后,逐滴加入0.1mol·Lˉ1的KMnO4溶液。当反应完全时,消耗KMnO4溶液20.00mL。反应的方程式为:2KMnO4+5H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O。请回答下列问题:
(1)所配制的250mL溶液中,H2O2的物质的量浓度是_____________ 。
(2)若原过氧化氢样品的密度为1.1 g·cm-3,则其溶质的质量分数为_______ 。
(3)滴入0.1 mol·Lˉ1KMnO4溶液反应完全后,反应中转移电子的数目为_______ 。
(1)所配制的250mL溶液中,H2O2的物质的量浓度是
(2)若原过氧化氢样品的密度为1.1 g·cm-3,则其溶质的质量分数为
(3)滴入0.1 mol·Lˉ1KMnO4溶液反应完全后,反应中转移电子的数目为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】在含有H+、Mg2+、Al3+简单阳离子的100mL溶液中,逐滴滴加5mol·L-1的NaOH溶液到过量,生成沉淀的质量与加入的NaOH溶液的体积关系如图所示。由图中数据分析计算:
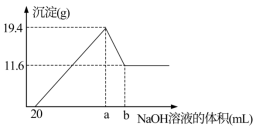
(1)沉淀减少时发生的离子方程式:___________ 。
(2)a点的数值为:___________ mL。

(1)沉淀减少时发生的离子方程式:
(2)a点的数值为:
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】(1)在质量分数为28%的KOH水溶液中,OH-与H2O数目之比是________ 。
(2)由硫酸钾、硫酸铁和硫酸组成的混合溶液,其中c(H+)=0.1 mol/L,c(Fe3+)=0.3 mol/L,c(SO42-)=0.6 mol/L,则c(K+)为________ 。
(3)相同物质的量浓度的氯化钠、氯化镁、氯化铝溶液,分别与硝酸银溶液反应,当生成沉淀的质量之比为3∶2∶1时,消耗三种盐溶液的体积比为________ 。
(4)某状况下a L氨气(此时气体摩尔体积为Vm)溶解在一定量的水中形成b mL氨水溶液,所得溶液的密度为ρ g/mL,则该氨水的物质的量浓度可表示为________ mol/L;氨水的质量分数为________ 。
(5)已知1.505×1023个X气体分子的质量是8 g,则X气体的摩尔质量是________ 。
(2)由硫酸钾、硫酸铁和硫酸组成的混合溶液,其中c(H+)=0.1 mol/L,c(Fe3+)=0.3 mol/L,c(SO42-)=0.6 mol/L,则c(K+)为
(3)相同物质的量浓度的氯化钠、氯化镁、氯化铝溶液,分别与硝酸银溶液反应,当生成沉淀的质量之比为3∶2∶1时,消耗三种盐溶液的体积比为
(4)某状况下a L氨气(此时气体摩尔体积为Vm)溶解在一定量的水中形成b mL氨水溶液,所得溶液的密度为ρ g/mL,则该氨水的物质的量浓度可表示为
(5)已知1.505×1023个X气体分子的质量是8 g,则X气体的摩尔质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】某纯净的天然碱可看做二氧化碳和氢氧化钠反应的产物。取6.64g天然碱用酒精灯充分加热至恒重,将生成的气体依次通过过量的浓硫酸、过量澄清石灰水后,浓硫酸增重0.9g,澄清石灰水中生成沉淀1g。
(1)充分加热后,剩余固体重______ g;
(2)该天然碱成分中除含有碳酸钠外,还含有_________ (填化学式);
(3)6.64g天然碱中,含碳酸钠的物质的量为_________ mol;
(4)该天然碱的化学式为______________ 。
(1)充分加热后,剩余固体重
(2)该天然碱成分中除含有碳酸钠外,还含有
(3)6.64g天然碱中,含碳酸钠的物质的量为
(4)该天然碱的化学式为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】以物质的量为中心的相关计算,已知阿状伽德罗常数为NA.
(1)相同物质的量的CO2和O2其分子数之比为_______________ ,原子数之比为_____________ 氧原子数之比为____________________ 。
(2)73.0g HCl气体中含有_______________ 个原子,标况下体积约为___________ L。
(3)23.75g某+2价金属的氯化物(MCl2)中含有3.01 ×1023个Cl-,则M的摩尔质量为______________ 。
(1)相同物质的量的CO2和O2其分子数之比为
(2)73.0g HCl气体中含有
(3)23.75g某+2价金属的氯化物(MCl2)中含有3.01 ×1023个Cl-,则M的摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】物质的量是高中化学计算的核心:
(1)相同物质的量的NH3和H2S的质量比___ ,分子个数比为___ ,同温同压下的体积比__ ,所含氢原子的个数比为____ .
(2)现有m g某气体,它的一个分子由四原子构成,它的摩尔质量为M g/mol.设阿伏伽德罗常数为NA,则:
①该气体的物质的量为____ mol.
②该气体中所含的原子总数为____ 个.
③该气体在标准状况下的体积为___ L.
(1)相同物质的量的NH3和H2S的质量比
(2)现有m g某气体,它的一个分子由四原子构成,它的摩尔质量为M g/mol.设阿伏伽德罗常数为NA,则:
①该气体的物质的量为
②该气体中所含的原子总数为
③该气体在标准状况下的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
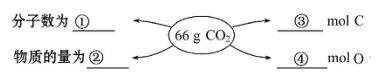
【推荐3】回答下列问题:
(1)在①②③④处的横线上填写适当的内容。_____________ 、____________ 、____________ 、_________
(2)在质量分数为28%的KOH水溶液中,K+与H2O的数目之比是___________
(3)2 mol O3和3 mol O2的质量之比为_______________
(4)在标准状况下,体积为8.96 L的CO和CO2的混合气体共14.4 g。
①CO的质量为___________ g。
②CO的体积为______________ L。
③在标准状况下,该混合气体中,碳与氧两种原子的数目之比为_____________
(1)在①②③④处的横线上填写适当的内容。

(2)在质量分数为28%的KOH水溶液中,K+与H2O的数目之比是
(3)2 mol O3和3 mol O2的质量之比为
(4)在标准状况下,体积为8.96 L的CO和CO2的混合气体共14.4 g。
①CO的质量为
②CO的体积为
③在标准状况下,该混合气体中,碳与氧两种原子的数目之比为
您最近一年使用:0次