学习化学应该明确“从生活中来,到生活中去”道理。在生产生活中,我们会遇到各种各样的化学物质和化学反应。请按要求填空
(1)计算机芯片的主要成分是___ (填名称),节日的烟花是利用___ 。
(2)请你写出工业上用氯气和消石灰反应制取漂白粉的化学反应方程式:___ 。
(3)玉石的主要成分基本都属于硅酸盐,如某种翡翠的主要成分为NaAlSi2O6,将其表示为氧化物形式可写为___ 。
(4)沾有水的铁质器皿在加热时会发黑,该反应的化学方程式是___ 。
(5)补铁剂中的Fe2+易被氧化成Fe3+,服用时医生常建议同时服用维生素C,这是利用维生素C的___ 。
(1)计算机芯片的主要成分是
(2)请你写出工业上用氯气和消石灰反应制取漂白粉的化学反应方程式:
(3)玉石的主要成分基本都属于硅酸盐,如某种翡翠的主要成分为NaAlSi2O6,将其表示为氧化物形式可写为
(4)沾有水的铁质器皿在加热时会发黑,该反应的化学方程式是
(5)补铁剂中的Fe2+易被氧化成Fe3+,服用时医生常建议同时服用维生素C,这是利用维生素C的
更新时间:2021-03-03 18:47:00
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】化学让生活更美好。他一直在践行,如消除饮用水中的有毒物质,保证人民的生活质量。
(1)饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在过量NaOH溶液的条件下用铝粉将
的浓度,可以在过量NaOH溶液的条件下用铝粉将 还原为N2,写出其其离子方程式为:
还原为N2,写出其其离子方程式为:______________________________________________ 。
上述反应中,_________ 元素的化合价升高,则该元素的原子_______ (填“得到”或“失去”)电子。当有1mol N2生成时,反应中转移电子的数目为____________ 。
(2)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学方程式为__________________________________________________ 。(已知,氯气在石灰乳中发生歧化反应,其中一种产物是Ca(ClO)2)
(3)KA1(SO4)2•12H2O的俗名为_________ ,因其溶于水生成_____________ (化学式)可以吸附杂质,从而达到净水作用。
(1)饮用水中的
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在过量NaOH溶液的条件下用铝粉将
的浓度,可以在过量NaOH溶液的条件下用铝粉将 还原为N2,写出其其离子方程式为:
还原为N2,写出其其离子方程式为:上述反应中,
(2)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学方程式为
(3)KA1(SO4)2•12H2O的俗名为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】利用氯元素价类二维图可以从不同角度研究含氯物质的性质及其转化关系。图中①⑩均含氯元素。回答下列问题:

(1)④的化学式为_______ ,⑦的酸性比碳酸_______ (填“强”或“弱”)。
(2)比较等浓度的⑥和⑦溶液的酸性强弱_______ (填“可以”或“不可以”)用 试纸分别测定。
试纸分别测定。
(3)工业制漂白粉是将①通入_______ 中(填名称)制成的,漂白粉放置时间长了就会失效,写出漂白粉失效的化学方程式_______ ,_______ 。
(4)某一淡黄色粉末与⑥相似,也具有漂白性,这种粉末能与⑤反应生成⑧,请写出该反应的化学方程式_______ 。

(1)④的化学式为
(2)比较等浓度的⑥和⑦溶液的酸性强弱
 试纸分别测定。
试纸分别测定。(3)工业制漂白粉是将①通入
(4)某一淡黄色粉末与⑥相似,也具有漂白性,这种粉末能与⑤反应生成⑧,请写出该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】硅单质及其化合物用途广泛,请回答下列问题:
(1)制备硅半导体材料必须先得到高纯硅。三氯硅烷 还原法是当前制备高纯硅的主要方法,生产过程示意图如下:
还原法是当前制备高纯硅的主要方法,生产过程示意图如下:

写出由纯 制备高纯硅的化学反应方程式
制备高纯硅的化学反应方程式_______ 。
(2)下列有关材料的说法正确的是_______。
(3)硅酸钠水溶液俗称水玻璃,取少量硅酸钠溶液于试管中,逐滴加入盐酸,振荡。写出实验现象及化学方程式_______ 。
(4)在人体器官受到损伤时,需要使用一种新型无机非金属材料来植入体内,这种材料是_______ (填字母)。
A.高温结构陶瓷 B.生物陶瓷 C.导电陶瓷
(1)制备硅半导体材料必须先得到高纯硅。三氯硅烷
 还原法是当前制备高纯硅的主要方法,生产过程示意图如下:
还原法是当前制备高纯硅的主要方法,生产过程示意图如下:
写出由纯
 制备高纯硅的化学反应方程式
制备高纯硅的化学反应方程式(2)下列有关材料的说法正确的是_______。
| A.单质硅化学性质稳定,但可以被强碱溶液腐蚀 |
| B.盐酸可以与硅反应,故采用盐酸为抛光液抛光单晶硅 |
| C.普通玻璃是由纯碱、石灰石和石英砂制成的,其熔点很高 |
D.混凝土桥墩中含有 |
(4)在人体器官受到损伤时,需要使用一种新型无机非金属材料来植入体内,这种材料是
A.高温结构陶瓷 B.生物陶瓷 C.导电陶瓷
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按照要求,回答下列问题:
(1)硅酸盐材料是传统无机非金属材料,下列产品属于硅酸盐的是___________ (填序号)。
①玻璃 ②陶瓷 ③水晶 ④硅芯片 ⑤水泥 ⑥光导纤维 ⑦钻石
(2)下列变化中属于吸热反应的是___________ 。
①铝片与稀盐酸的反应 ②将胆矾加热变为白色粉末 ③甲烷在氧气中的燃烧反应 ④Ba(OH)2·8H2O与NH4Cl反应 ⑤煅烧石灰石 ⑥NH4NO3固体溶于水
(3)已知部分共价键的键能如下:E(N≡N)=946 kJ/mol,E(H-H)=436 kJ/mol,E(N-H)=391kJ/mol。根据以上数据写出工业合成氨的热化学反应方程式:___________ 。
(4)在25℃、101 kPa下,液态甲醇(CH3OH))的燃烧热为726.5 kJ/mol,已知:H2O (l)=H2O(g) △H=+44 kJ/mol,写出甲醇燃烧生成水蒸气的热化学方程式___________ 。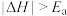 。在右图中补充该反应过程的能量变化示意图
。在右图中补充该反应过程的能量变化示意图___________ 。
(1)硅酸盐材料是传统无机非金属材料,下列产品属于硅酸盐的是
①玻璃 ②陶瓷 ③水晶 ④硅芯片 ⑤水泥 ⑥光导纤维 ⑦钻石
(2)下列变化中属于吸热反应的是
①铝片与稀盐酸的反应 ②将胆矾加热变为白色粉末 ③甲烷在氧气中的燃烧反应 ④Ba(OH)2·8H2O与NH4Cl反应 ⑤煅烧石灰石 ⑥NH4NO3固体溶于水
(3)已知部分共价键的键能如下:E(N≡N)=946 kJ/mol,E(H-H)=436 kJ/mol,E(N-H)=391kJ/mol。根据以上数据写出工业合成氨的热化学反应方程式:
(4)在25℃、101 kPa下,液态甲醇(CH3OH))的燃烧热为726.5 kJ/mol,已知:H2O (l)=H2O(g) △H=+44 kJ/mol,写出甲醇燃烧生成水蒸气的热化学方程式
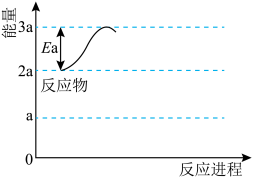
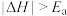 。在右图中补充该反应过程的能量变化示意图
。在右图中补充该反应过程的能量变化示意图
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】硅单质及其化合物应用范围很广。请回答下列问题:
(1)制备硅半导体材料必须先得到高纯硅。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程示意图如下:

①写出由石英砂和焦炭在高温下制备粗硅的化学反应方程式:_____________ 。
②整个制备过程必须严格控制无水无氧。SiHCl3 遇水剧烈反应生成H2SiO3、HCl 和另一种气体,写出配平的化学反应方程式:_____________ ;H2 还原SiHCl3 过程中若混入O2,可能引起的后果是______________ 。
(2)下列有关硅材料的说法正确的是_____________ (填字母代号)。
A.氮化硅硬度大、熔点高,可用于制作高温陶瓷和轴承
B.石英坩埚耐高温性强,可用于加热熔融氢氧化钠
C.神舟10 号飞船所用太阳能电池板可将光能转换为电能,所用转换材料单晶硅也可以制作电脑芯片
D.普通玻璃是由纯碱、石灰石和石英砂制成的,其熔点很高
E.盐酸可以与硅反应,故可采用盐酸为抛光液抛光单晶硅
F.玛瑙饰品的主要成分与建筑材料砂子相同
(1)制备硅半导体材料必须先得到高纯硅。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程示意图如下:

①写出由石英砂和焦炭在高温下制备粗硅的化学反应方程式:
②整个制备过程必须严格控制无水无氧。SiHCl3 遇水剧烈反应生成H2SiO3、HCl 和另一种气体,写出配平的化学反应方程式:
(2)下列有关硅材料的说法正确的是
A.氮化硅硬度大、熔点高,可用于制作高温陶瓷和轴承
B.石英坩埚耐高温性强,可用于加热熔融氢氧化钠
C.神舟10 号飞船所用太阳能电池板可将光能转换为电能,所用转换材料单晶硅也可以制作电脑芯片
D.普通玻璃是由纯碱、石灰石和石英砂制成的,其熔点很高
E.盐酸可以与硅反应,故可采用盐酸为抛光液抛光单晶硅
F.玛瑙饰品的主要成分与建筑材料砂子相同
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】有一种矿石,经测定含有镁、硅、氧三种元素且它们的质量比为12∶7∶16。
(1)用盐的组成表示其化学式:___________ 。
(2)用氧化物的组成表示其化学式:_______ 。
(3)该矿石的成分属于________ (填物质的分类)。
(4)写出该矿石(氧化物形式)与盐酸反应的化学方程式:______ 。
(1)用盐的组成表示其化学式:
(2)用氧化物的组成表示其化学式:
(3)该矿石的成分属于
(4)写出该矿石(氧化物形式)与盐酸反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求填空
(1)检验SO42-所需要用的试剂_______________________________ 。
(2)三硅酸镁(Mg2Si3O8·11H2O)用氧化物表示_______________________ 。
(3)除去NaHCO3溶液中少量的Na2CO3杂质相应的离子方程式为_________________ 。
(4)用氨气检验氯气泄漏的方程式:_______________ 。
(5)请配平以下化学方程式:
____ Al+____ NaNO3+____ NaOH= ____ NaAlO2+____ N2↑+___ H2O
若反应过程中转移 5 mol 电子,则生成标准状况下 N2 的体积为_________ L。
(1)检验SO42-所需要用的试剂
(2)三硅酸镁(Mg2Si3O8·11H2O)用氧化物表示
(3)除去NaHCO3溶液中少量的Na2CO3杂质相应的离子方程式为
(4)用氨气检验氯气泄漏的方程式:
(5)请配平以下化学方程式:
若反应过程中转移 5 mol 电子,则生成标准状况下 N2 的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)钾云母的化学式为K2H4Al6Si6O24,其简单氧化物表示形式为_____________ 。
(2)长石的化学式为KAlSi3Ox,x=_______ 。
(3)SiO2是玻璃的主要成分之一,SiO2与氢氧化钠溶液反应的化学方程式为_____________________ 。
(4)向明矾水溶液中滴加过量氨水,现象是_________________ ,反应的离子方程式_______________ ,再向其中加入过量NaOH溶液,反应的化学方程式为______________________ 。
(2)长石的化学式为KAlSi3Ox,x=
(3)SiO2是玻璃的主要成分之一,SiO2与氢氧化钠溶液反应的化学方程式为
(4)向明矾水溶液中滴加过量氨水,现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】请列举铁与硝酸反应的各种情况,写出相关的离子方程式_______ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某合金(仅含铜、铁)中铜和铁的物质的量之和为 ,其中
,其中 的物质的量分数为b,将其全部投入
的物质的量分数为b,将其全部投入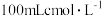 的稀硝酸中,加热使其充分反应(假设
的稀硝酸中,加热使其充分反应(假设 是唯一的还原产物)。
是唯一的还原产物)。
(1)若金属全部溶解,则溶液中___________ (填“一定”或“不一定”)含有 。
。
(2)若产生标准状况下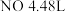 ,则反应转移的电子总数为
,则反应转移的电子总数为___________  。
。
(3)若溶液中金属离子只有 、
、 时,则c≥
时,则c≥___________ (用含a和b的式子表示)。
 ,其中
,其中 的物质的量分数为b,将其全部投入
的物质的量分数为b,将其全部投入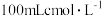 的稀硝酸中,加热使其充分反应(假设
的稀硝酸中,加热使其充分反应(假设 是唯一的还原产物)。
是唯一的还原产物)。(1)若金属全部溶解,则溶液中
 。
。(2)若产生标准状况下
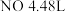 ,则反应转移的电子总数为
,则反应转移的电子总数为 。
。(3)若溶液中金属离子只有
 、
、 时,则c≥
时,则c≥
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I、下表是生活生产中常见的物质.表中列出了它们的一种主要成分(其中加碘盐是氯化钠中添加适量的 ,其他成分未列出)
,其他成分未列出)
(1)请你对表中①~⑦的主要成分进行分类,既不是电解质又不是非电解质的是___________ (填序号)。
(2)写出④在水中的电离方程式______________________ 。
(3)写出用④治疗胃酸(主要成分为盐酸)过多涉及的离子方程式:______________________ 。
(4)已知①中 和
和 的混合气体
的混合气体 共
共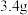 ,则①中
,则①中 的质量为
的质量为___________ g。
II.铁的化学性质比较活泼,常温下铁可以与稀硝酸发生反应,反应的化学方程式为 。
。
(5)该反应中还原产物为___________ ,每生成 (标准状况下)的
(标准状况下)的 转移的电子个数为
转移的电子个数为___________ .
(6)请用双线桥标出电子转移方向和数目的情况______________________ 。
 ,其他成分未列出)
,其他成分未列出)名称 | 水煤气 | 葡萄糖 | 醋酸 | 小苏打 | 生石灰 | 铁丝 | 加碘盐 |
主要成分 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
(2)写出④在水中的电离方程式
(3)写出用④治疗胃酸(主要成分为盐酸)过多涉及的离子方程式:
(4)已知①中
 和
和 的混合气体
的混合气体 共
共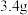 ,则①中
,则①中 的质量为
的质量为II.铁的化学性质比较活泼,常温下铁可以与稀硝酸发生反应,反应的化学方程式为
 。
。(5)该反应中还原产物为
 (标准状况下)的
(标准状况下)的 转移的电子个数为
转移的电子个数为(6)请用双线桥标出电子转移方向和数目的情况
您最近一年使用:0次






 和
和

