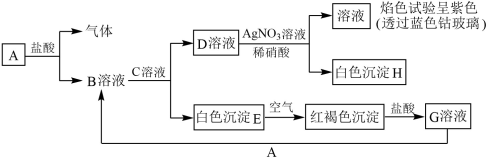
甲、乙两同学欲用NaOH溶液、铁屑、稀H2SO4试剂制取纯净的Fe(OH)2,根据如图所示的装置进行实验。请回答下列问题。
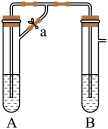
(1)在试管A里加入的试剂是_______ 。
(2)同学甲:先夹紧止水夹a,使A管开始反应,在B管中观察到的现象是_______ 。
(3)同学乙:打开a,使A管中反应一段时间再夹紧止水夹a,实验中在B中发生反应的离子方程式为_______ 。
(4)同学乙打开a的目的_______ ;_______ (填甲或乙)同学实验可成功。

(1)在试管A里加入的试剂是
(2)同学甲:先夹紧止水夹a,使A管开始反应,在B管中观察到的现象是
(3)同学乙:打开a,使A管中反应一段时间再夹紧止水夹a,实验中在B中发生反应的离子方程式为
(4)同学乙打开a的目的
更新时间:2021-03-02 19:55:00
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】如图所示,此装置可用来制取和观察Fe(OH)2在空气中被氧化的颜色变化。实验时必须使用铁屑和6mol·L-1的硫酸,其他试剂任选。填写下列空白:
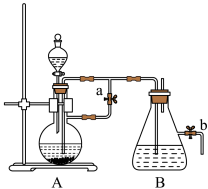
(1)B中盛有一定量的NaOH溶液,A中应预先加入的药品是___ 。A中反应的离子方程式是___ 。
(2)实验开始时先将止水夹a___ (填“打开”或“关闭”)。
(3)简述生成Fe(OH)2的操作过程____ 。
(4)实验完毕,打开b处止水夹,放入一部分空气,此时B瓶中发生反应的化学方程式 为___ 。

(1)B中盛有一定量的NaOH溶液,A中应预先加入的药品是
(2)实验开始时先将止水夹a
(3)简述生成Fe(OH)2的操作过程
(4)实验完毕,打开b处止水夹,放入一部分空气,此时B瓶中发生反应的化学方程式 为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】其同学设计如图装置(气密性已检查)制备Fe(OH)2白色沉淀。
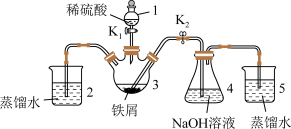
(1)仪器1的名称________ 。装置5的作用________ 。
(2)实验开始时,关闭 ,打开
,打开 ,反应一段时间后,再打开
,反应一段时间后,再打开 ,关闭
,关闭 ,发现3中的溶液不能进入4,请作一处改进,使溶液能进入4中,
,发现3中的溶液不能进入4,请作一处改进,使溶液能进入4中,________ 。

(1)仪器1的名称
(2)实验开始时,关闭
 ,打开
,打开 ,反应一段时间后,再打开
,反应一段时间后,再打开 ,关闭
,关闭 ,发现3中的溶液不能进入4,请作一处改进,使溶液能进入4中,
,发现3中的溶液不能进入4,请作一处改进,使溶液能进入4中,
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】下面是制备Fe(OH)2白色沉淀的几种方案。请回答下列问题:
(1)用不含Fe3+的FeSO4溶液与不含O2的蒸馏水配制的NaOH溶液反应制备Fe(OH)2。
①用硫酸亚铁晶体配制上述FeSO4溶液时还需要加入铁粉,其目的是_________________ (用离子方程式表示)。
②除去蒸馏水中溶解的O2常采用___________ 的方法。
③生成Fe(OH)2白色沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,发生反应的离子方程式___________ 。
(2)在如图所示的装置中,用NaOH溶液、铁粉、稀H2SO4等试剂制备。

①仪器a的名称是___________ 。
②关闭K3,打开K1和K2,向仪器c中加入适量稀硫酸,关闭K2,写出装置c中发生反应的离子方程式___________ 。同时c中有气体产生,该气体的作用是___________ 。
③当仪器b中产生均匀气泡后的操作是___________ 。写出仪器c、d中可能出现的实验现象___________ 。
(1)用不含Fe3+的FeSO4溶液与不含O2的蒸馏水配制的NaOH溶液反应制备Fe(OH)2。
①用硫酸亚铁晶体配制上述FeSO4溶液时还需要加入铁粉,其目的是
②除去蒸馏水中溶解的O2常采用
③生成Fe(OH)2白色沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,发生反应的离子方程式
(2)在如图所示的装置中,用NaOH溶液、铁粉、稀H2SO4等试剂制备。

①仪器a的名称是
②关闭K3,打开K1和K2,向仪器c中加入适量稀硫酸,关闭K2,写出装置c中发生反应的离子方程式
③当仪器b中产生均匀气泡后的操作是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】某工厂的工业废水中含有大量的 和较多的
和较多的 。为了减少污染并变废为宝,工厂计划从该废水中回收
。为了减少污染并变废为宝,工厂计划从该废水中回收 和金属铜。请根据以下流程图,回答下列问题。
和金属铜。请根据以下流程图,回答下列问题。
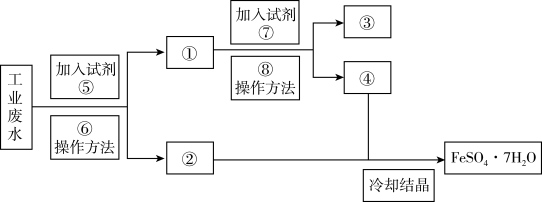
(1)鉴别溶液④中的金属阳离子时,应滴加的试剂依次是___________ ,现象依次是___________ ;请写出该鉴别过程中属于氧化还原反应的离子方程式:___________ 。
(2)若取2mL溶液④加入试管中,然后滴加氢氧化钠溶液,产生的现象是___________ ,此过程涉及反应的化学方程式是___________ 。
 和较多的
和较多的 。为了减少污染并变废为宝,工厂计划从该废水中回收
。为了减少污染并变废为宝,工厂计划从该废水中回收 和金属铜。请根据以下流程图,回答下列问题。
和金属铜。请根据以下流程图,回答下列问题。
(1)鉴别溶液④中的金属阳离子时,应滴加的试剂依次是
(2)若取2mL溶液④加入试管中,然后滴加氢氧化钠溶液,产生的现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】过氧化钙 对环境友好,能杀菌消毒净化空气。实验室用大理石为原料制备过氧化钙,反应为
对环境友好,能杀菌消毒净化空气。实验室用大理石为原料制备过氧化钙,反应为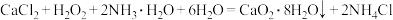 。
。
一、制
I.取适量大理石(含有铁的氧化物等杂质)溶于盐酸,搅拌,至大理石基本完全溶解。
Ⅱ.加水稀释,滴加6%过氧化氢溶液,并用 氨水调节
氨水调节 ,煮沸后趁热过滤,除去
,煮沸后趁热过滤,除去 。
。
Ⅲ.向热滤液中滴加碳酸铵溶液和少量浓氨水,加热搅拌一段时间。
Ⅳ.___________、过滤、洗涤后,将得到的固体置于烧杯中,逐滴加盐酸溶解,产生气泡,并再次煮沸。
二、制
Ⅴ.将Ⅳ所得溶液与过氧化氢、浓氨水混合,放置半小时后抽滤,洗涤, 烘干。
烘干。
回答下列问题:
(1)步骤I中使用的主要玻璃仪器有___________ 。
(2)步骤Ⅱ中除去二价铁的相关离子方程式为___________ ;煮沸后需趁热过滤,目的是___________ ;若在该步骤中使用热抽滤漏斗(见下图),比普通过滤的优点是___________ (写两条)。
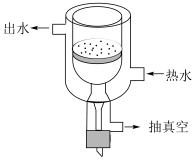
(3)步骤Ⅲ得到的固体主要是___________ (写化学式)。
(4)步骤Ⅳ经“___________ 、过滤、洗涤”,得到纯净固体后加盐酸,如果不进行再次煮沸,可能造成的影响是___________ 。
(5)关于步骤V的操作,下列方案最合理的是___________ (填序号)。
① 溶液
溶液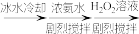
②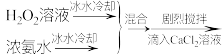
③
 对环境友好,能杀菌消毒净化空气。实验室用大理石为原料制备过氧化钙,反应为
对环境友好,能杀菌消毒净化空气。实验室用大理石为原料制备过氧化钙,反应为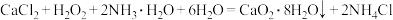 。
。一、制

I.取适量大理石(含有铁的氧化物等杂质)溶于盐酸,搅拌,至大理石基本完全溶解。
Ⅱ.加水稀释,滴加6%过氧化氢溶液,并用
 氨水调节
氨水调节 ,煮沸后趁热过滤,除去
,煮沸后趁热过滤,除去 。
。Ⅲ.向热滤液中滴加碳酸铵溶液和少量浓氨水,加热搅拌一段时间。
Ⅳ.___________、过滤、洗涤后,将得到的固体置于烧杯中,逐滴加盐酸溶解,产生气泡,并再次煮沸。
二、制

Ⅴ.将Ⅳ所得溶液与过氧化氢、浓氨水混合,放置半小时后抽滤,洗涤,
 烘干。
烘干。回答下列问题:
(1)步骤I中使用的主要玻璃仪器有
(2)步骤Ⅱ中除去二价铁的相关离子方程式为

(3)步骤Ⅲ得到的固体主要是
(4)步骤Ⅳ经“
(5)关于步骤V的操作,下列方案最合理的是
①
 溶液
溶液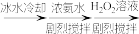
②
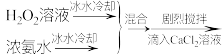
③

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】以高硫铝土矿(主要成分为Al2O3、Fe2O3、SiO2,少量FeS2和金属硫酸盐)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如下:
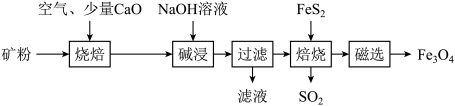
(1)粉碎高硫铝土矿石的目的是______ 。
(2)焙烧时发生氧化还原反应:______ FeS2+______O2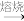 ______Fe2O3+______SO2↑,配平该方程式。
______Fe2O3+______SO2↑,配平该方程式。
(3)碱浸时发生反应的化学方程式为______ 。
(4)过滤后向滤液中通入过量的CO2气体,反应的离子方程式为______ 。
(5)“过滤”得到的滤渣中含有大量的Fe2O3。Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,理论上完全反应消耗的n(FeS2):n(Fe2O3)=______ 。

(1)粉碎高硫铝土矿石的目的是
(2)焙烧时发生氧化还原反应:
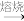 ______Fe2O3+______SO2↑,配平该方程式。
______Fe2O3+______SO2↑,配平该方程式。(3)碱浸时发生反应的化学方程式为
(4)过滤后向滤液中通入过量的CO2气体,反应的离子方程式为
(5)“过滤”得到的滤渣中含有大量的Fe2O3。Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,理论上完全反应消耗的n(FeS2):n(Fe2O3)=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上常利用含硫废水生产Na2S2O3·5H2O,实验室可用如下装置(略去部分夹持仪器)模拟生产过程。
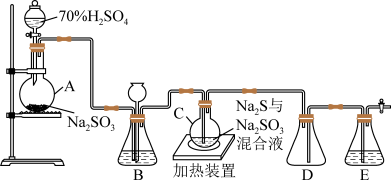
烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq)(I)
2H2S(aq) + SO2(g) = 3S(s)+ 2H2O(l) (II)
S(s)+Na2SO3(aq) Na2S2O3(aq) (III)
Na2S2O3(aq) (III)
回答下列问题:
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若_______ ,则整个装置气密性良好。装置E中为_______ 溶液。
(2)为提高产品纯度,应使烧瓶C中Na2S和 Na2SO3恰好完全反应,则烧瓶C中 Na2S和Na2SO3物质的量之比为_______ 。
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择_______ 溶液。
(4)实验中,为使SO2缓慢进入烧瓶C,采用的操作是_______ 。
(5)已知反应(III)相对较慢,则烧瓶C中反应达到终点的现象是_______ 。
(6)烧瓶C中的实验一般控制在碱性环境下进行,否则产品发黄,用离子反应方程式表示其原因:_______ 。

烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq)(I)
2H2S(aq) + SO2(g) = 3S(s)+ 2H2O(l) (II)
S(s)+Na2SO3(aq)
 Na2S2O3(aq) (III)
Na2S2O3(aq) (III)回答下列问题:
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若
(2)为提高产品纯度,应使烧瓶C中Na2S和 Na2SO3恰好完全反应,则烧瓶C中 Na2S和Na2SO3物质的量之比为
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择
(4)实验中,为使SO2缓慢进入烧瓶C,采用的操作是
(5)已知反应(III)相对较慢,则烧瓶C中反应达到终点的现象是
(6)烧瓶C中的实验一般控制在碱性环境下进行,否则产品发黄,用离子反应方程式表示其原因:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】【化学---选修2:化学与技术】
MnO2和锌是制造干电池的主要原料。
电解法生产MnO2传统的工艺主要流程为:软锰矿加煤还原焙烧;用硫酸浸出焙烧料;浸出液(主要含Mn2+)经净化后再进行电解。
90年代后期发明了生产MnO2和锌的新工艺,主要是采用软锰矿(主要成分为MnO2,含少量Al2O3和SiO2杂质)和闪锌矿(主要成分为ZnS,含少量FeS、CuS、CdS杂质)为主要原料,经过除杂后,得到含Zn2+、Mn2+离子的溶液,再通过电解同时获得MnO2和锌。简化流程框图如下(中间产物的固体部分已经略去):
软锰矿、闪锌矿 滤液A
滤液A Zn2+、Mn2+、Fe2+、Al3+
Zn2+、Mn2+、Fe2+、Al3+
ZnSO4、MnSO4溶液 Zn+MnO2+产品D
Zn+MnO2+产品D
已知各种金属离子完全沉淀的pH如下表:
回答下列问题:
(1)步骤①中,软锰矿、闪锌矿粉与硫酸溶液共热时析出硫的反应为氧化还原反应,例如:MnO2+ZnS+2H2SO4=MnSO4+ZnSO4+S↓+2H2O,请写出MnO2在酸性溶液中分别和CuS和FeS发生反应的化学方程式:__________________________、_____________________________。
(2)步骤②加入金属锌是为了回收金属,回收金属的主要成份为___________(用化学符号表示)
(3)步骤③物质C由多种物质组成,其中含有两种固体,其中一种为MnO2,其作用是___
____________________,另外一种固体物质可为___________。
(4)步骤④中电解过程中MnO2在______极析出,该电极上发生的反应方程式为________________。产品D的化学式为_________________,该物质对整个生产的意义是___________________________。
MnO2和锌是制造干电池的主要原料。
电解法生产MnO2传统的工艺主要流程为:软锰矿加煤还原焙烧;用硫酸浸出焙烧料;浸出液(主要含Mn2+)经净化后再进行电解。
90年代后期发明了生产MnO2和锌的新工艺,主要是采用软锰矿(主要成分为MnO2,含少量Al2O3和SiO2杂质)和闪锌矿(主要成分为ZnS,含少量FeS、CuS、CdS杂质)为主要原料,经过除杂后,得到含Zn2+、Mn2+离子的溶液,再通过电解同时获得MnO2和锌。简化流程框图如下(中间产物的固体部分已经略去):
软锰矿、闪锌矿
 滤液A
滤液A Zn2+、Mn2+、Fe2+、Al3+
Zn2+、Mn2+、Fe2+、Al3+
ZnSO4、MnSO4溶液
 Zn+MnO2+产品D
Zn+MnO2+产品D已知各种金属离子完全沉淀的pH如下表:
| Zn2+ | Mn2+ | Fe2+ | Fe3+ | Al3+ | |
| pH | 8.0 | 10.1 | 9.0 | 3.2 | 4.7 |
(1)步骤①中,软锰矿、闪锌矿粉与硫酸溶液共热时析出硫的反应为氧化还原反应,例如:MnO2+ZnS+2H2SO4=MnSO4+ZnSO4+S↓+2H2O,请写出MnO2在酸性溶液中分别和CuS和FeS发生反应的化学方程式:__________________________、_____________________________。
(2)步骤②加入金属锌是为了回收金属,回收金属的主要成份为___________(用化学符号表示)
(3)步骤③物质C由多种物质组成,其中含有两种固体,其中一种为MnO2,其作用是___
____________________,另外一种固体物质可为___________。
(4)步骤④中电解过程中MnO2在______极析出,该电极上发生的反应方程式为________________。产品D的化学式为_________________,该物质对整个生产的意义是___________________________。
您最近一年使用:0次