【化学---选修2:化学与技术】
MnO2和锌是制造干电池的主要原料。
电解法生产MnO2传统的工艺主要流程为:软锰矿加煤还原焙烧;用硫酸浸出焙烧料;浸出液(主要含Mn2+)经净化后再进行电解。
90年代后期发明了生产MnO2和锌的新工艺,主要是采用软锰矿(主要成分为MnO2,含少量Al2O3和SiO2杂质)和闪锌矿(主要成分为ZnS,含少量FeS、CuS、CdS杂质)为主要原料,经过除杂后,得到含Zn2+、Mn2+离子的溶液,再通过电解同时获得MnO2和锌。简化流程框图如下(中间产物的固体部分已经略去):
软锰矿、闪锌矿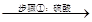 滤液A
滤液A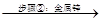 Zn2+、Mn2+、Fe2+、Al3+
Zn2+、Mn2+、Fe2+、Al3+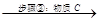
ZnSO4、MnSO4溶液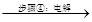 Zn+MnO2+产品D
Zn+MnO2+产品D
已知各种金属离子完全沉淀的pH如下表:
回答下列问题:
(1)步骤①中,软锰矿、闪锌矿粉与硫酸溶液共热时析出硫的反应为氧化还原反应,例如:MnO2+ZnS+2H2SO4=MnSO4+ZnSO4+S↓+2H2O,请写出MnO2在酸性溶液中分别和CuS和FeS发生反应的化学方程式:__________________________、_____________________________。
(2)步骤②加入金属锌是为了回收金属,回收金属的主要成份为___________(用化学符号表示)
(3)步骤③物质C由多种物质组成,其中含有两种固体,其中一种为MnO2,其作用是___
____________________,另外一种固体物质可为___________。
(4)步骤④中电解过程中MnO2在______极析出,该电极上发生的反应方程式为________________。产品D的化学式为_________________,该物质对整个生产的意义是___________________________。
MnO2和锌是制造干电池的主要原料。
电解法生产MnO2传统的工艺主要流程为:软锰矿加煤还原焙烧;用硫酸浸出焙烧料;浸出液(主要含Mn2+)经净化后再进行电解。
90年代后期发明了生产MnO2和锌的新工艺,主要是采用软锰矿(主要成分为MnO2,含少量Al2O3和SiO2杂质)和闪锌矿(主要成分为ZnS,含少量FeS、CuS、CdS杂质)为主要原料,经过除杂后,得到含Zn2+、Mn2+离子的溶液,再通过电解同时获得MnO2和锌。简化流程框图如下(中间产物的固体部分已经略去):
软锰矿、闪锌矿
 滤液A
滤液A Zn2+、Mn2+、Fe2+、Al3+
Zn2+、Mn2+、Fe2+、Al3+
ZnSO4、MnSO4溶液
 Zn+MnO2+产品D
Zn+MnO2+产品D已知各种金属离子完全沉淀的pH如下表:
| Zn2+ | Mn2+ | Fe2+ | Fe3+ | Al3+ | |
| pH | 8.0 | 10.1 | 9.0 | 3.2 | 4.7 |
(1)步骤①中,软锰矿、闪锌矿粉与硫酸溶液共热时析出硫的反应为氧化还原反应,例如:MnO2+ZnS+2H2SO4=MnSO4+ZnSO4+S↓+2H2O,请写出MnO2在酸性溶液中分别和CuS和FeS发生反应的化学方程式:__________________________、_____________________________。
(2)步骤②加入金属锌是为了回收金属,回收金属的主要成份为___________(用化学符号表示)
(3)步骤③物质C由多种物质组成,其中含有两种固体,其中一种为MnO2,其作用是___
____________________,另外一种固体物质可为___________。
(4)步骤④中电解过程中MnO2在______极析出,该电极上发生的反应方程式为________________。产品D的化学式为_________________,该物质对整个生产的意义是___________________________。
更新时间:2016-12-09 15:18:26
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)已知CuO具有氧化性,能够和氨气反应生成两种单质和一种生活中常见的化合物,请写出在加热条件下CuO和 反应的化学方程式:
反应的化学方程式:_______ 。
(2)在一定条件下,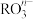 和
和 可发生反应:
可发生反应: ,在上述过程中
,在上述过程中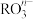 被
被_______ (填“氧化”或“还原”),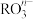 中R的化合价是
中R的化合价是_______ 价。
(3)某一反应体系有反应物和生成物共五种物质: 、
、 、
、 、
、 、
、 已知该反应中
已知该反应中 只发生过程:
只发生过程: 。
。
①该反应中的氧化剂是_______ (填化学式,下同)
②该反应中,发生还原反应的过程是:_______ →_______ 。
(4) ,用双线桥表示反应电子转移方向和数目
,用双线桥表示反应电子转移方向和数目_______ 。
(1)已知CuO具有氧化性,能够和氨气反应生成两种单质和一种生活中常见的化合物,请写出在加热条件下CuO和
 反应的化学方程式:
反应的化学方程式:(2)在一定条件下,
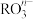 和
和 可发生反应:
可发生反应: ,在上述过程中
,在上述过程中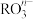 被
被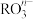 中R的化合价是
中R的化合价是(3)某一反应体系有反应物和生成物共五种物质:
 、
、 、
、 、
、 、
、 已知该反应中
已知该反应中 只发生过程:
只发生过程: 。
。①该反应中的氧化剂是
②该反应中,发生还原反应的过程是:
(4)
 ,用双线桥表示反应电子转移方向和数目
,用双线桥表示反应电子转移方向和数目
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】氯胺是由氯气遇到氨气反应生成的一类化合物,是常用的饮用水二级消毒剂,主要包括一氯胺、二氯胺和三氯胺(NH2Cl、NHCl2和NCl3)。
(1)氯胺作饮用水消毒剂是因为水解生成具有强烈杀菌作用的物质,该物质的结构式为________ ,二氯胺与水反应的化学方程式为_____________ 。将0.01 mol NCl3通入100 mL 0.5 mol/L Na2SO3溶液中,转移电子的物质的量为_______ mol。
(2)已知部分化学键的键能和化学反应的能量变化如下表和下图所示。

则反应过程中的△H2=____ kJ·mol-1,表中的x=_____ 。
(3)在密闭容器中反应NH3(g)+Cl2(g) NH2Cl(g)+HCl(g)达到平衡,通过热力学定律计算,不同温度下理论上NH2Cl的体积分数随
NH2Cl(g)+HCl(g)达到平衡,通过热力学定律计算,不同温度下理论上NH2Cl的体积分数随 的变化如下图所示。
的变化如下图所示。

①a、b、c三点对应平衡常数的大小关系是(分别用Ka、Kb、Kc表示)_________ 。b点时,该反应的平衡常数为________ ;
②T2℃,Q点对应的速率:
__________  (填“>”、“<”或“=”);
(填“>”、“<”或“=”);
③在氨氯比一定时,提高NH3的转化率的方法是__________ (任写1种);
④若产物都是气体,实验测得NH2C1的体积分数始终比理论值低,原因可能是______________ 。
(1)氯胺作饮用水消毒剂是因为水解生成具有强烈杀菌作用的物质,该物质的结构式为
(2)已知部分化学键的键能和化学反应的能量变化如下表和下图所示。
| 化学键 | N-H | N-Cl | H-Cl |
键能 | 391.3 | x | 431.8 |

则反应过程中的△H2=
(3)在密闭容器中反应NH3(g)+Cl2(g)
 NH2Cl(g)+HCl(g)达到平衡,通过热力学定律计算,不同温度下理论上NH2Cl的体积分数随
NH2Cl(g)+HCl(g)达到平衡,通过热力学定律计算,不同温度下理论上NH2Cl的体积分数随 的变化如下图所示。
的变化如下图所示。
①a、b、c三点对应平衡常数的大小关系是(分别用Ka、Kb、Kc表示)
②T2℃,Q点对应的速率:

 (填“>”、“<”或“=”);
(填“>”、“<”或“=”);③在氨氯比一定时,提高NH3的转化率的方法是
④若产物都是气体,实验测得NH2C1的体积分数始终比理论值低,原因可能是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】氯化亚铜难溶于水,溶于浓盐酸和氨水,不溶于乙醇,在潮湿的空气中易被氧化。某兴趣小组模拟工业用SO2还原Na2[CuCl4]溶液制备CuCl的装置如图所示。回答下列问题:
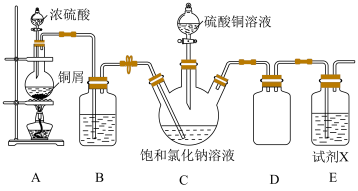
(1)装置A中盛放铜屑的仪器名称是___________ ;写出装置A中发生反应的化学反应方程式:___________ 。
(2)装置D的作用是___________ ;将硫酸铜溶液滴入饱和氯化钠溶液中会形成Na2[CuCl4],其中[CuCl4]2-的配位键中提供孤电子对的是___________ (填化学符号);装置C中SO2与[CuCl4]2-反应的离子方程式为___________ 。
(3)高温条件下,亚铜离子比铜离子稳定,原因是___________ ;CuSO4在高温条件下发生分解反应生成的砖红色固体为___________ (填化学式)。

(1)装置A中盛放铜屑的仪器名称是
(2)装置D的作用是
(3)高温条件下,亚铜离子比铜离子稳定,原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】磷酸铁(FePO4)常用作电极材料。以硫铁矿(主要成分是FeS2,含少量Al2O3、SiO2和Fe3O4)为原料制备磷酸铁的流程如下:

已知几种金属离子沉淀的pH如下表所示:
请回答下列问题:
(1)滤渣3的主要成分是___________ (写出化学式 );
(2)用FeS还原Fe3+的目的是___________ 加入FeO的作用是___________ (用离子方程式表示);
(3)试剂R宜选择___________ (填字母);
A.高锰酸钾 B.稀硝酸 C.双氧水 D.次氯酸钠
(4)检验“氧化”之后溶液是否含Fe2+的操作是___________ ;
(5)已知沉淀溶解平衡: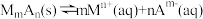 ,
,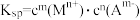 。常温下,
。常温下,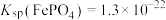 ,“沉铁”中为了使
,“沉铁”中为了使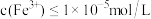 ,
,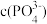 最小为
最小为___________ mol/L。

已知几种金属离子沉淀的pH如下表所示:
| 金属氢氧化物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀的pH | 2.3 | 7.5 | 4.0 |
| 完全沉淀的pH | 4.1 | 9.7 | 5.2 |
请回答下列问题:
(1)滤渣3的主要成分是
(2)用FeS还原Fe3+的目的是
(3)试剂R宜选择
A.高锰酸钾 B.稀硝酸 C.双氧水 D.次氯酸钠
(4)检验“氧化”之后溶液是否含Fe2+的操作是
(5)已知沉淀溶解平衡:
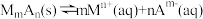 ,
,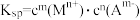 。常温下,
。常温下,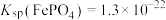 ,“沉铁”中为了使
,“沉铁”中为了使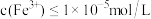 ,
,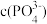 最小为
最小为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】NiCO3常用于催化剂、电镀、陶瓷等工业。现用某含镍电镀废渣(含Cu、Zn、Fe、Cr等杂质)制取NiCO3的过程如图所示:

(1)流程中的试剂X(某钠盐)的化学式是___________ 。
(2)“氧化”时需保持滤液在40℃左右,用6%的H2O2溶液氧化。控制温度不超过40℃的原因是______ (用化学方程式表示)。
(3)Fe2+也可以用NaClO3氧化,生成的Fe3+在较小pH条件下水解,最终形成黄钠铁矾[Na2Fe6(SO4)4(OH)12]沉淀而被除去,如图是pH—温度关系图,图中阴影部分为黄钠铁矾稳定存在的区域,下列说法不正确的是________ (填字母)。

a.黄钠铁矾[Na2Fe6(SO4)4(OH)12]中铁为+2价
b.pH过低或过高均不利于生成黄钠铁矾,其原因相同
c.氯酸钠在氧化Fe2+时,1 mol NaClO3得到的电子数为6NA
d.工业生产中温度常保持在85~95 ℃,加入Na2SO4后生成黄钠铁矾,此时溶液的pH约为1.2~1.8。
(4)加入Na2CO3溶液时,确认Ni2+已经完全沉淀的实验方法是_______________ 。
(5)某小组利用NiCO3制取镍氢电池的正极材料碱式氧化镍(NiOOH),过程如图:

①已知 25℃时,Ksp[Ni(OH)2]=2×10-15,当调节 pH≥9 时,溶液中残留的c(Ni2+)________ mol/L。
②写出在空气中加热Ni(OH)2制取NiOOH的化学方程式________________ 。
③镍氢电池电解液为30%的KOH,负极为MH(即吸氢材料M吸附氢原子)。充电时也可实现Ni(OH)2转化为NiOOH。请写出放电时该电池的总反应式______________ 。

(1)流程中的试剂X(某钠盐)的化学式是
(2)“氧化”时需保持滤液在40℃左右,用6%的H2O2溶液氧化。控制温度不超过40℃的原因是
(3)Fe2+也可以用NaClO3氧化,生成的Fe3+在较小pH条件下水解,最终形成黄钠铁矾[Na2Fe6(SO4)4(OH)12]沉淀而被除去,如图是pH—温度关系图,图中阴影部分为黄钠铁矾稳定存在的区域,下列说法不正确的是

a.黄钠铁矾[Na2Fe6(SO4)4(OH)12]中铁为+2价
b.pH过低或过高均不利于生成黄钠铁矾,其原因相同
c.氯酸钠在氧化Fe2+时,1 mol NaClO3得到的电子数为6NA
d.工业生产中温度常保持在85~95 ℃,加入Na2SO4后生成黄钠铁矾,此时溶液的pH约为1.2~1.8。
(4)加入Na2CO3溶液时,确认Ni2+已经完全沉淀的实验方法是
(5)某小组利用NiCO3制取镍氢电池的正极材料碱式氧化镍(NiOOH),过程如图:

①已知 25℃时,Ksp[Ni(OH)2]=2×10-15,当调节 pH≥9 时,溶液中残留的c(Ni2+)
②写出在空气中加热Ni(OH)2制取NiOOH的化学方程式
③镍氢电池电解液为30%的KOH,负极为MH(即吸氢材料M吸附氢原子)。充电时也可实现Ni(OH)2转化为NiOOH。请写出放电时该电池的总反应式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】碘酸铜[ ]微溶于水,是一种常见的化工原料,在电化学领域发挥着重要作用。某研究小组设计了制备碘酸铜并测定其溶度积(
]微溶于水,是一种常见的化工原料,在电化学领域发挥着重要作用。某研究小组设计了制备碘酸铜并测定其溶度积( )的实验,流程如下:
)的实验,流程如下:
第一步:碘酸铜固体的制备

第二步:配制不同浓度 的碘酸铜饱和溶液
的碘酸铜饱和溶液
取制备好的碘酸铜固体和 的蒸馏水,形成悬浊液,按下表数据,用___________量取一定量的
的蒸馏水,形成悬浊液,按下表数据,用___________量取一定量的 溶液和
溶液和 溶液,将上述混合液搅拌约
溶液,将上述混合液搅拌约 ,用___________,将所得溶液分别用编号过的3个___________收集。
,用___________,将所得溶液分别用编号过的3个___________收集。
第三步:碘酸铜溶度积( )的测定
)的测定
构建以Zn、 (
( )作负极,Cu、碘酸铜饱和溶液作正极的原电池,测定该原电池的电动势E,通过公式计算可得溶液中
)作负极,Cu、碘酸铜饱和溶液作正极的原电池,测定该原电池的电动势E,通过公式计算可得溶液中 的浓度,通过计算可以得到该条件下碘酸铜溶度积(
的浓度,通过计算可以得到该条件下碘酸铜溶度积( )的数值,进行3次平行实验,所得数据取平均值。电动势公式如下(其中,
)的数值,进行3次平行实验,所得数据取平均值。电动势公式如下(其中, 和
和 数据可由文献查阅):
数据可由文献查阅):

请回答:
(1)下列有关说法不正确 的是___________。
(2)第二步实验,加入 溶液的目的是
溶液的目的是___________ ;其中实验编号2、3加入 溶液的体积分别是
溶液的体积分别是
___________ 、
___________ 。
(3)第一步实验的步骤Ⅰ,如何判断反应基本完全?___________
(4)从下列选项中选择合理的仪器和操作,将第二步实验过程补充完整“_______”上填写一件最关键的仪器 ,“_______”内填写一种操作 ,均用字母表示]。_______ 、_______ 、_______ 。
a.量筒;b.移液管;c.天平;d.三角漏斗;e.分液漏斗;f.干燥的小烧杯;g.湿润的小烧杯
A.过滤;B,称重;C.分液;D.溶解
(5)已知: ,请用含a、b的式子列出
,请用含a、b的式子列出 的计算式:
的计算式:___________ 。
 ]微溶于水,是一种常见的化工原料,在电化学领域发挥着重要作用。某研究小组设计了制备碘酸铜并测定其溶度积(
]微溶于水,是一种常见的化工原料,在电化学领域发挥着重要作用。某研究小组设计了制备碘酸铜并测定其溶度积( )的实验,流程如下:
)的实验,流程如下:第一步:碘酸铜固体的制备

第二步:配制不同浓度
 的碘酸铜饱和溶液
的碘酸铜饱和溶液取制备好的碘酸铜固体和
 的蒸馏水,形成悬浊液,按下表数据,用___________量取一定量的
的蒸馏水,形成悬浊液,按下表数据,用___________量取一定量的 溶液和
溶液和 溶液,将上述混合液搅拌约
溶液,将上述混合液搅拌约 ,用___________,将所得溶液分别用编号过的3个___________收集。
,用___________,将所得溶液分别用编号过的3个___________收集。第三步:碘酸铜溶度积(
 )的测定
)的测定构建以Zn、
 (
( )作负极,Cu、碘酸铜饱和溶液作正极的原电池,测定该原电池的电动势E,通过公式计算可得溶液中
)作负极,Cu、碘酸铜饱和溶液作正极的原电池,测定该原电池的电动势E,通过公式计算可得溶液中 的浓度,通过计算可以得到该条件下碘酸铜溶度积(
的浓度,通过计算可以得到该条件下碘酸铜溶度积( )的数值,进行3次平行实验,所得数据取平均值。电动势公式如下(其中,
)的数值,进行3次平行实验,所得数据取平均值。电动势公式如下(其中, 和
和 数据可由文献查阅):
数据可由文献查阅):
| 实验编号 | 1 | 2 | 3 |
 溶液的体积/mL 溶液的体积/mL | 0 | 1.00 | 2.00 |
 溶液的体积/mL 溶液的体积/mL | 2.00 | x | y |
所加 的浓度 的浓度 | 0 | 5.00 | 10.00 |
测定电池电动势 | |||
计算 的浓度 的浓度 | |||
 |
(1)下列有关说法
A.第一步实验的步骤Ⅰ,搅拌并加热 的目的是使反应更加完全 的目的是使反应更加完全 |
| B.第一步实验的步骤Ⅱ,为提高洗涤速率,应少量分批用蒸馏水洗涤,并用玻璃棒轻轻搅拌 |
| C.第二步实验,若配制的碘酸铜溶液未饱和,测得的碘酸铜溶度积偏小 |
| D.第三步实验,实验所用的碘酸铜饱和溶液的体积必须相同,否则对实验数据大小影响很大 |
 溶液的目的是
溶液的目的是 溶液的体积分别是
溶液的体积分别是

(3)第一步实验的步骤Ⅰ,如何判断反应基本完全?
(4)从下列选项中选择合理的仪器和操作,将第二步实验过程补充完整“_______”上填写
a.量筒;b.移液管;c.天平;d.三角漏斗;e.分液漏斗;f.干燥的小烧杯;g.湿润的小烧杯
A.过滤;B,称重;C.分液;D.溶解
(5)已知:
 ,请用含a、b的式子列出
,请用含a、b的式子列出 的计算式:
的计算式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】以氧化铝为原料,通过碳热还原法可合成氮化铝(AlN);通过电解法可制取铝。电解铝时阳极产生的CO2可通过二氧化碳甲烷化再利用。
(1) 已知:2Al2O3(s)= 4Al(g) +3O2(g) ΔH1=+3351 kJ·molˉ1;
2C(s)+O2(g)= 2CO(g) ΔH2=-221 kJ·molˉ1 ;
2Al(g)+N2(g)= 2AlN(s) ΔH3=-318 kJ·molˉ1
碳热还原Al2O3合成AlN(可逆反应)的总热化学方程式是______________________ ,该反应自发进行的条件___________ ,随着温度升高,反应物Al2O3的平衡转化率将__________ (填“增大”、“不变”或“减小”);一定温度下,在压强为p的反应体系中,平衡时CO的物质的量浓度为c;若温度不变,反应体系的压强减小为0. 5p,则平衡时CO的物质的量浓度__________ 。
A.小于0.5c B.大于0.5c,小于c C.等于c D.大于c
(2) 据文献报道,CO2可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是___________________________ 。
(1) 已知:2Al2O3(s)= 4Al(g) +3O2(g) ΔH1=+3351 kJ·molˉ1;
2C(s)+O2(g)= 2CO(g) ΔH2=-221 kJ·molˉ1 ;
2Al(g)+N2(g)= 2AlN(s) ΔH3=-318 kJ·molˉ1
碳热还原Al2O3合成AlN(可逆反应)的总热化学方程式是
A.小于0.5c B.大于0.5c,小于c C.等于c D.大于c
(2) 据文献报道,CO2可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是
您最近一年使用:0次
【推荐2】以CO2为原料制备甲醇等能源物质具有较好的发展前景。因此,研发CO2利用技术,降低空气中CO2含量成为研究热点。
(1)在催化剂的作用下,氢气还原CO2的过程中可同时发生反应Ⅰ、Ⅱ。(已知活化能: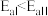 )
)
Ⅰ.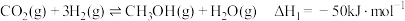
Ⅱ.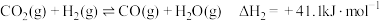
①则 的△H3=
的△H3=___________ kJ/mol,其中反应Ⅰ能自发进行的条件是___________ 。
②保持温度T不变时,在容积不变的密闭容器中,充入一定量的CO2及H2,起始及达到平衡时,容器内各气体的物质的量及总压强数据如表所示:
若反应Ⅰ、Ⅱ均达到平衡,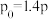 ,则表中m=
,则表中m=___________ ;反应Ⅰ的平衡常数Kp=___________ (用含p的代数式表示)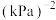 。
。
(2)在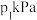 下,向恒压反应器中通入
下,向恒压反应器中通入 、
、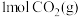 ,
, 的平衡转化率及CH3OH(g)的平衡产率随温度变化的关系如图。
的平衡转化率及CH3OH(g)的平衡产率随温度变化的关系如图。
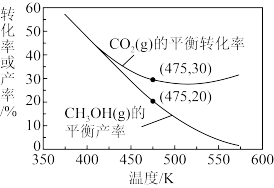
已知:CH3OH的产率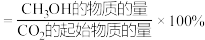
①下列说法正确的是______ (填标号)。
A.反应过程中,容器内压强不再变化,说明反应Ⅰ达到平衡
B.反应过程中,气体密度保持不变,说明反应Ⅰ达到平衡
C.平衡后再向容器中通入一定量的H2能提高CO2的平衡转化率
②图中500 K以后,CO2的平衡转化率随温度升高而增大的原因是______ 。
(3)工业上常用电解法将CO2合成为羧酸以实现资源化处理。以Pt为电极、质子惰性有机溶剂为电解液的装置,可将CO2转化为草酸(H2C2O4),其阴极的电极反应式为______ 。
(1)在催化剂的作用下,氢气还原CO2的过程中可同时发生反应Ⅰ、Ⅱ。(已知活化能:
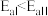 )
)Ⅰ.
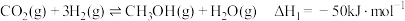
Ⅱ.
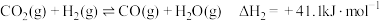
①则
 的△H3=
的△H3=②保持温度T不变时,在容积不变的密闭容器中,充入一定量的CO2及H2,起始及达到平衡时,容器内各气体的物质的量及总压强数据如表所示:
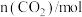 | 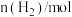 | 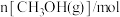 | 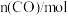 | 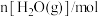 | 总压强/kPa | |
| 起始 | 0.5 | 0.9 | 0 | 0 | 0 |  |
| 平衡 | m | 0.3 | p |
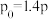 ,则表中m=
,则表中m=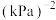 。
。(2)在
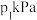 下,向恒压反应器中通入
下,向恒压反应器中通入 、
、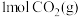 ,
, 的平衡转化率及CH3OH(g)的平衡产率随温度变化的关系如图。
的平衡转化率及CH3OH(g)的平衡产率随温度变化的关系如图。
已知:CH3OH的产率
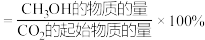
①下列说法正确的是
A.反应过程中,容器内压强不再变化,说明反应Ⅰ达到平衡
B.反应过程中,气体密度保持不变,说明反应Ⅰ达到平衡
C.平衡后再向容器中通入一定量的H2能提高CO2的平衡转化率
②图中500 K以后,CO2的平衡转化率随温度升高而增大的原因是
(3)工业上常用电解法将CO2合成为羧酸以实现资源化处理。以Pt为电极、质子惰性有机溶剂为电解液的装置,可将CO2转化为草酸(H2C2O4),其阴极的电极反应式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某实验小组为探究CuSO4与Na2SO3反应后的产物,做如下探究实验。
【查阅资料】
(1)Cu2O为砖红色固体,不溶于水;
(2)Cu2SO3为黄色固体,不溶于水;
(3)[Cu(SO3)2]3-为无色配合离子、[Cu(NH3)2]+为无色配合离子、[Cu(NH3)4]2+为深蓝色配合离子。
【实验探究】
实验1:①向2mL0.2mol•L-1的CuSO4溶液中滴加0.2mol•L-1的Na2SO3溶液,开始出现黄色沉淀,但无气体产生。
②继续加入Na2SO3溶液,最终沉淀消失。经检验,溶液中生成[Cu(SO3)2]3-离子。
实验2:向90℃2mL0.2mol•L-1的CuSO4溶液中滴加0.2mol•L-1的Na2SO3溶液,直接生成砖红色沉淀。
实验3:向2mL0.2mol•L-1的Na2SO3溶液中滴加0.2mol•L-1的CuSO4溶液,开始阶段有蓝色沉淀出现。
(1)某同学认为实验1黄色沉淀中有少量Cu(OH)2,该同学认为是CuSO4、Na2SO3相互促进水解产生的,用离子方程式表示生成Cu(OH)2沉淀的过程:_______ 。
(2)若要进一步检验黄色沉淀中有Cu(OH)2,可采用的具体实验方法为_______ 。
(3)经检验,实验2所得溶液中有大量SO 、HSO
、HSO 生成。该实验中Cu2+表现氧化性,写出该实验中反应的离子方程式:
生成。该实验中Cu2+表现氧化性,写出该实验中反应的离子方程式:_______ 。
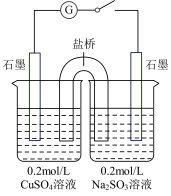
(4)某同学设计了如图所示的电化学装置,探究CuSO4与Na2SO3的反应。该装置中左侧烧杯中的石墨电极做_______ (填“正”或“负”)极,右侧烧杯中发生反应的电极反应式为_______ 。设计实验检验右侧烧杯中生成的阴离子,写出具体操作、现象和结论:_______ 。
【查阅资料】
(1)Cu2O为砖红色固体,不溶于水;
(2)Cu2SO3为黄色固体,不溶于水;
(3)[Cu(SO3)2]3-为无色配合离子、[Cu(NH3)2]+为无色配合离子、[Cu(NH3)4]2+为深蓝色配合离子。
【实验探究】
实验1:①向2mL0.2mol•L-1的CuSO4溶液中滴加0.2mol•L-1的Na2SO3溶液,开始出现黄色沉淀,但无气体产生。
②继续加入Na2SO3溶液,最终沉淀消失。经检验,溶液中生成[Cu(SO3)2]3-离子。
实验2:向90℃2mL0.2mol•L-1的CuSO4溶液中滴加0.2mol•L-1的Na2SO3溶液,直接生成砖红色沉淀。
实验3:向2mL0.2mol•L-1的Na2SO3溶液中滴加0.2mol•L-1的CuSO4溶液,开始阶段有蓝色沉淀出现。
(1)某同学认为实验1黄色沉淀中有少量Cu(OH)2,该同学认为是CuSO4、Na2SO3相互促进水解产生的,用离子方程式表示生成Cu(OH)2沉淀的过程:
(2)若要进一步检验黄色沉淀中有Cu(OH)2,可采用的具体实验方法为
(3)经检验,实验2所得溶液中有大量SO
 、HSO
、HSO 生成。该实验中Cu2+表现氧化性,写出该实验中反应的离子方程式:
生成。该实验中Cu2+表现氧化性,写出该实验中反应的离子方程式:(4)某同学设计了如图所示的电化学装置,探究CuSO4与Na2SO3的反应。该装置中左侧烧杯中的石墨电极做

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】氯气是一种重要的化工原料,自来水的消毒、农药的生产、药物的合成等都需要用到氯气。
I.工业上通常采用电解法制氯气:观察下图,回答:

(1)若饱和食盐水中含有酚酞,通电后_____ (填a或b)侧先变红。
(2)电解反应的化学方程式为_______________________ 。
II. 某学生设计如下图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应),据此回答下列问题:

(1)在A装置中用固体二氧化锰与浓盐酸在加热条件下制取氯气,反应化学方程式为_________________________________________
(2)漂白粉将在U形管中产生,其化学方程式是__________________________________ 。
(3)C装置的作用是_____________________ 。
(4)此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应。
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是_________________________________ 。
②试判断另一个副反应(用化学方程式表示)_______________________________________ 。为避免此副反应的发生,可将装置作何改进_____________________________________ 。
(5)家庭中使用漂白粉时,为了增强漂白能力,可加入少量的物质是______________ 。
A.食盐 B.食醋 C.烧碱 D.纯碱
I.工业上通常采用电解法制氯气:观察下图,回答:

(1)若饱和食盐水中含有酚酞,通电后
(2)电解反应的化学方程式为
II. 某学生设计如下图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应),据此回答下列问题:

(1)在A装置中用固体二氧化锰与浓盐酸在加热条件下制取氯气,反应化学方程式为
(2)漂白粉将在U形管中产生,其化学方程式是
(3)C装置的作用是
(4)此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应。
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是
②试判断另一个副反应(用化学方程式表示)
(5)家庭中使用漂白粉时,为了增强漂白能力,可加入少量的物质是
A.食盐 B.食醋 C.烧碱 D.纯碱
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】FePO4是一种难溶于水的白色固体,可用金属防腐剂,也可用于制备电动汽车电池的正极材料LiFePO4。实验室利用FeSO4•7H2O和H3PO4(弱酸)制备FePO4 、LiFePO4流程如下图:

回答下列问题:
(1)“溶解”时H3PO4不宜过量太多的原因是__________ 。
(2)①洗涤FePO4沉淀的操作是__________ ;
②若经多次洗涤后所得“FePO4”仍呈棕色,则“FePO4”最可能混有的杂质是_____ 。
(3)“反应1”时总反应的离子方程式是_____________ 。
(4)“反应2”时总反应的化学方程式是:2LiOH + 6H2C2O4 + 2FePO4=2LiFePO4 + 7CO2 + 5X +7H2O ,其中X的化学式为____ ;每生成1molLiFePO4,该反应转移_______ mole-。
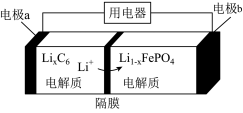
(5)LiFePO4电池稳定性高、安全、对环境友好,该电池的总反应式是:LiFePO4 + C6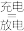 Li1﹣xFePO4 + LixC6,其放电时工作原理如图所示。
Li1﹣xFePO4 + LixC6,其放电时工作原理如图所示。
则:充电时,a极的电极反应式为_____________ ;
放电时,b极的电极反应式为_______________ 。

回答下列问题:
(1)“溶解”时H3PO4不宜过量太多的原因是
(2)①洗涤FePO4沉淀的操作是
②若经多次洗涤后所得“FePO4”仍呈棕色,则“FePO4”最可能混有的杂质是
(3)“反应1”时总反应的离子方程式是
(4)“反应2”时总反应的化学方程式是:2LiOH + 6H2C2O4 + 2FePO4=2LiFePO4 + 7CO2 + 5X +7H2O ,其中X的化学式为

(5)LiFePO4电池稳定性高、安全、对环境友好,该电池的总反应式是:LiFePO4 + C6
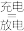 Li1﹣xFePO4 + LixC6,其放电时工作原理如图所示。
Li1﹣xFePO4 + LixC6,其放电时工作原理如图所示。则:充电时,a极的电极反应式为
放电时,b极的电极反应式为
您最近一年使用:0次
【推荐3】氯化钴(CoCl2)固体为蓝色,吸水后变为粉红色至红色,有潮解性,能溶于水,常用作分析试剂湿度和水分的指示剂。某兴趣小组查阅有关资料后在实验室以Co2O3为主要原料制备氯化钴。
有关资料:Ⅰ.Co2O3不溶于水,不与水反应,具有较强氧化性。
Ⅱ.Co2O3在不同温度下被 还原的产物如下表:
还原的产物如下表:
回答下列问题:
(1)有同学查阅资料得知,向Co2O3固体滴加浓盐酸会生成氯化钴,进行实验时发现还产生了黄绿色有刺激性气体的气体,反应的化学方程式为_______ 。
小组同学因此舍弃该制备方法。
(2)经讨论后,确定了实验方案:
Ⅰ.制备 :Ⅱ.净化
:Ⅱ.净化 ;Ⅲ.
;Ⅲ. 热还原制备CoO;Ⅳ.还原产物用盐酸酸溶;Ⅴ.酸溶液提取
热还原制备CoO;Ⅳ.还原产物用盐酸酸溶;Ⅴ.酸溶液提取 ;Ⅵ.检验产品纯度。
;Ⅵ.检验产品纯度。
小组同学称取 制备CoO,制备CoO用到的装置如图所示(夹持装置已略去)。
制备CoO,制备CoO用到的装置如图所示(夹持装置已略去)。 _______ →h。
②加热瓷舟前应进行的操作为_______ 。
③同学甲认为可控温电加热管的温度应该控制在200℃,同学乙认为温度为250℃也不会对 的纯度造成影响,他的理由是
的纯度造成影响,他的理由是_______ 。
(3)瓷舟中的CoO冷却后溶于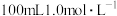 盐酸,此过程中无气体产生,将酸溶液经
盐酸,此过程中无气体产生,将酸溶液经_______ (填操作名称),得到 晶体。
晶体。
(4)将 晶体中
晶体中_______ 气流中加热去除结晶水,置于干燥器中冷却后称其质量为2.6500g。
(5)小组同学将所得晶体溶于水,加入足量 溶液,所得白色沉淀的质量为5.7400g。经计算存在误差,则产生上述误差的原因可能为
溶液,所得白色沉淀的质量为5.7400g。经计算存在误差,则产生上述误差的原因可能为_______ 。
有关资料:Ⅰ.Co2O3不溶于水,不与水反应,具有较强氧化性。
Ⅱ.Co2O3在不同温度下被
 还原的产物如下表:
还原的产物如下表:| 温度/℃ | 125 | 200 | 250 |
| 还原产物 |  |  |  |
(1)有同学查阅资料得知,向Co2O3固体滴加浓盐酸会生成氯化钴,进行实验时发现还产生了黄绿色有刺激性气体的气体,反应的化学方程式为
小组同学因此舍弃该制备方法。
(2)经讨论后,确定了实验方案:
Ⅰ.制备
 :Ⅱ.净化
:Ⅱ.净化 ;Ⅲ.
;Ⅲ. 热还原制备CoO;Ⅳ.还原产物用盐酸酸溶;Ⅴ.酸溶液提取
热还原制备CoO;Ⅳ.还原产物用盐酸酸溶;Ⅴ.酸溶液提取 ;Ⅵ.检验产品纯度。
;Ⅵ.检验产品纯度。小组同学称取
 制备CoO,制备CoO用到的装置如图所示(夹持装置已略去)。
制备CoO,制备CoO用到的装置如图所示(夹持装置已略去)。 
②加热瓷舟前应进行的操作为
③同学甲认为可控温电加热管的温度应该控制在200℃,同学乙认为温度为250℃也不会对
 的纯度造成影响,他的理由是
的纯度造成影响,他的理由是(3)瓷舟中的CoO冷却后溶于
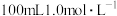 盐酸,此过程中无气体产生,将酸溶液经
盐酸,此过程中无气体产生,将酸溶液经 晶体。
晶体。(4)将
 晶体中
晶体中(5)小组同学将所得晶体溶于水,加入足量
 溶液,所得白色沉淀的质量为5.7400g。经计算存在误差,则产生上述误差的原因可能为
溶液,所得白色沉淀的质量为5.7400g。经计算存在误差,则产生上述误差的原因可能为
您最近一年使用:0次



