向2L密闭容器中通入amol气体A和bmol气体B,在一定条件下发生反应:xA(g)+yB(g) pC(g)+qD(g)。已知:平均反应速率v(C)=
pC(g)+qD(g)。已知:平均反应速率v(C)= v(A);反应2min时,A的物质的量减少
v(A);反应2min时,A的物质的量减少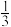 amol,B的物质的量减少
amol,B的物质的量减少 mol,有amolD生成。回答下列问题:
mol,有amolD生成。回答下列问题:
(1)反应2min内,v(B)=______ 。
(2)化学方程式中,x=______ ,q=______ 。
(3)反应平衡时,D为2amol,则B的转化率为______ 。
 pC(g)+qD(g)。已知:平均反应速率v(C)=
pC(g)+qD(g)。已知:平均反应速率v(C)= v(A);反应2min时,A的物质的量减少
v(A);反应2min时,A的物质的量减少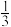 amol,B的物质的量减少
amol,B的物质的量减少 mol,有amolD生成。回答下列问题:
mol,有amolD生成。回答下列问题:(1)反应2min内,v(B)=
(2)化学方程式中,x=
(3)反应平衡时,D为2amol,则B的转化率为
19-20高一下·湖北武汉·期中 查看更多[4]
湖北省武汉市外国语学校2019-2020学年高一下学期期中考试化学试题河北省张家口市宣化第一中学2020-2021学年高一下学期期中考试化学试题(已下线)6.2.2 化学反应的限度-2021-2022学年高一化学课后培优练(人教版2019必修第二册)新疆疏勒县第一中学2020--2021学年高二下学期期末考试化学试题
更新时间:2021-03-03 18:11:46
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】在2L的容器内,反应N2+3H2  2NH3 刚开始时,N2的物质的量为1.5mol,H2的物质的量为2.5 mol,3min后测得NH3浓度为0.6mol/L,问:
2NH3 刚开始时,N2的物质的量为1.5mol,H2的物质的量为2.5 mol,3min后测得NH3浓度为0.6mol/L,问:
(1)该反应的平衡常数表达式及平衡常数的值_________ ?
(2)此时间内,氮气、氢气、氨气的速率分别是多少_________ ?
 2NH3 刚开始时,N2的物质的量为1.5mol,H2的物质的量为2.5 mol,3min后测得NH3浓度为0.6mol/L,问:
2NH3 刚开始时,N2的物质的量为1.5mol,H2的物质的量为2.5 mol,3min后测得NH3浓度为0.6mol/L,问:(1)该反应的平衡常数表达式及平衡常数的值
(2)此时间内,氮气、氢气、氨气的速率分别是多少
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】把2 mol X气体和1 mol Y气体混合于2 L密闭容器中,发生如下反应:3X(g)+Y(g)  nZ(g)+2W(g),2 min末生成0.2 mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol/(L·min),试计算:
nZ(g)+2W(g),2 min末生成0.2 mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol/(L·min),试计算:
(1)前2 min内,用X表示的平均反应速率=_______ ;
(2)2 min末时Y的转化率=________ ;
(3)化学方程式中Z的化学计量数n=_______ ;
 nZ(g)+2W(g),2 min末生成0.2 mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol/(L·min),试计算:
nZ(g)+2W(g),2 min末生成0.2 mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol/(L·min),试计算:(1)前2 min内,用X表示的平均反应速率=
(2)2 min末时Y的转化率=
(3)化学方程式中Z的化学计量数n=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】将0.1molMnO2粉末加入到50mL过氧化氢溶液(H2O2,ρ=1.1g·mL-1)中,在标准状况下放出气体的体积和时间的关系如图所示。

(1)放出一半气体所需的时间为________ 。
(2)反应放出 体积气体所需的时间约为
体积气体所需的时间约为________ 。
(3)解释反应速率变化的原因:_____ 。
(4)计算H2O2初始状态的浓度______ 。

(1)放出一半气体所需的时间为
(2)反应放出
 体积气体所需的时间约为
体积气体所需的时间约为(3)解释反应速率变化的原因:
(4)计算H2O2初始状态的浓度
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】把0.4 mol X气体和0.6 mol Y气体混合于2 L密闭容器中,使它们发生如下反应:4 X(g)+5 Y(g)=n Z(g)+6 W (g)。2 min 末已生成0.3 mol W,若测知以Z的浓度变化表示的反应速率为0.05 mol/(L·min),
(1)则这2 min内v(X) =_______ v(W) =_______
(2)2 min末时Y的浓度_______
(3)化学反应方程式中n的值是_______
(4)2min末时,已用去的X占原来总物质的量分数为_______
(1)则这2 min内v(X) =
(2)2 min末时Y的浓度
(3)化学反应方程式中n的值是
(4)2min末时,已用去的X占原来总物质的量分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】(1)在某一容积为2L的密闭容器中,某一反应中A、B、C、D四种气体的物质的量n(mol)随时间t(min)的变化曲线如图所示:
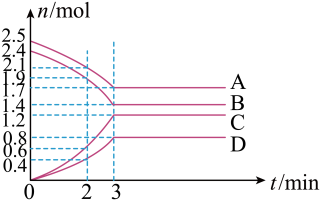
回答下列问题:
①该反应的化学方程式为___ 。
②前2min用A的浓度变化表示的化学反应速率为__ 。在2min时,图像发生改变的原因可能是__ (填字母)。
a.增大压强 b.降低温度 c.加入催化剂 d.增加A的物质的量
(2)在100℃时,将0.01mol的N2O4气体充入0.1L的密闭容器中发生反应,隔一定时间对该容器内的物质进行分析,得到如下表格:
试填空:
①该反应的化学方程式__ ,达到平衡时N2O4的转化率为__ 。
②在0~20s内,四氧化二氮的平均反应速率为__ 。

回答下列问题:
①该反应的化学方程式为
②前2min用A的浓度变化表示的化学反应速率为
a.增大压强 b.降低温度 c.加入催化剂 d.增加A的物质的量
(2)在100℃时,将0.01mol的N2O4气体充入0.1L的密闭容器中发生反应,隔一定时间对该容器内的物质进行分析,得到如下表格:
| 时间/s 浓度/mol·L-1 | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4)/mol·L-1 | 0.100 | 0.070 | 0.050 | a | b | c |
| c(NO2)/mol·L-1 | 0.000 | 0.060 | d | 0.120 | 0.120 | 0.120 |
试填空:
①该反应的化学方程式
②在0~20s内,四氧化二氮的平均反应速率为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】完成下列问题
(Ⅰ)某探究小组用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用HNO3浓度为1.00 mol/L、2.00 mol/L,大理石有细颗粒和粗颗粒两种规格,实验温度为25℃、35℃,每次实验HNO3的用量为25.0 mL。大理石用量为10.00 g。
(1)请完成以下实验设计表,并在实验目的一栏中填空:
(Ⅱ)把2.5 mol A和2.5 mol B混合放入2 L密闭容器里,发生反应: 3A(g)+B(g) xC(g)+2D(g),经5s后反应达到平衡。在此5 s内C的平均反应速率为0.2 mol/(L·s),同时生成1 mol D。试求:
xC(g)+2D(g),经5s后反应达到平衡。在此5 s内C的平均反应速率为0.2 mol/(L·s),同时生成1 mol D。试求:
(2)达到平衡时B的转化率为___________ 。
(3)x的值为___________ 。
(Ⅰ)某探究小组用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用HNO3浓度为1.00 mol/L、2.00 mol/L,大理石有细颗粒和粗颗粒两种规格,实验温度为25℃、35℃,每次实验HNO3的用量为25.0 mL。大理石用量为10.00 g。
(1)请完成以下实验设计表,并在实验目的一栏中填空:
| 实验编号 | 温度/℃ | 大理石规格 | HNO3浓度(mol/L) | 实验目的 |
| ① | 25 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究浓度对反应速率的影响 |
| ② | 25 | 粗颗粒 | (Ⅱ)实验①和③探究温度对反应速率的影响; | |
| ③ | 粗颗粒 | 2.00 | (Ⅲ)实验①和④探究 | |
| ④ | 25 | 细颗粒 | 2.00 |
(Ⅱ)把2.5 mol A和2.5 mol B混合放入2 L密闭容器里,发生反应: 3A(g)+B(g)
 xC(g)+2D(g),经5s后反应达到平衡。在此5 s内C的平均反应速率为0.2 mol/(L·s),同时生成1 mol D。试求:
xC(g)+2D(g),经5s后反应达到平衡。在此5 s内C的平均反应速率为0.2 mol/(L·s),同时生成1 mol D。试求:(2)达到平衡时B的转化率为
(3)x的值为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】在一体积固定的密闭容器中加入反应物A、B,发生如下反应:A(g)+2B(g)=3C(g)。反应2 min后,A的浓度从开始时的1.0 mol·L-1降到0.8 mol·L-1。.已知反应开始时B的浓度是1.6 mol·L-1。求:
(1)2 min末B的浓度___________ mol/L。
(2)2 min内A的平均反应速率___________ mol/(Lmin)。
(3)2 min内C的平均反应速率___________ mol/(Lmin)。
(4)2 min末时物质B的转化率为___________ 。
(1)2 min末B的浓度
(2)2 min内A的平均反应速率
(3)2 min内C的平均反应速率
(4)2 min末时物质B的转化率为
您最近一年使用:0次
【推荐3】在汽车排气系统中安装三元催化转化器,可发生下列反应:2NO(g)+2CO(g)  2CO2(g)+N2(g)。在某恒容密闭容器中通入等物质的量的CO和NO,在不同温度(T)下发生上述反应时,c(CO)随时间(t)的变化曲线如图所示:
2CO2(g)+N2(g)。在某恒容密闭容器中通入等物质的量的CO和NO,在不同温度(T)下发生上述反应时,c(CO)随时间(t)的变化曲线如图所示:

(1)温度为 时,反应开始19s内的平均反应速率:v(N2)=
时,反应开始19s内的平均反应速率:v(N2)=___________
(2)温度为 时,平衡常数K=
时,平衡常数K=___________ (填计算结果的数值)
(3)温度为 时,反应达到平衡时
时,反应达到平衡时 的转化率为
的转化率为___________ 。
 2CO2(g)+N2(g)。在某恒容密闭容器中通入等物质的量的CO和NO,在不同温度(T)下发生上述反应时,c(CO)随时间(t)的变化曲线如图所示:
2CO2(g)+N2(g)。在某恒容密闭容器中通入等物质的量的CO和NO,在不同温度(T)下发生上述反应时,c(CO)随时间(t)的变化曲线如图所示:
(1)温度为
 时,反应开始19s内的平均反应速率:v(N2)=
时,反应开始19s内的平均反应速率:v(N2)=(2)温度为
 时,平衡常数K=
时,平衡常数K=(3)温度为
 时,反应达到平衡时
时,反应达到平衡时 的转化率为
的转化率为
您最近一年使用:0次



