元素周期表短周期的一部分如图所示。回答下列问题:
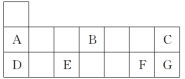
(1)A的元素符号为__________ 。
(2)B位于第二周期第__________ 族,DC为__________ (填“离子”或“共价”)化合物。
(3)G的最高价氧化物的化学式为__________ 。
(4)A、B、D原子半径由大到小的顺序为______________ (填化学式,下同),C、F、G最简单氢化物热稳定性由弱到强的顺序为__________ 。
(5)E的单质与D的最高价氧化物对应的水化物反应的离子方程式为___________________ 。

(1)A的元素符号为
(2)B位于第二周期第
(3)G的最高价氧化物的化学式为
(4)A、B、D原子半径由大到小的顺序为
(5)E的单质与D的最高价氧化物对应的水化物反应的离子方程式为
更新时间:2021-03-09 21:37:05
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】在表中用实线画出周期表的外框,写明族序数和周期序数,并在相应的空格内写出1~20号元素的元素符号,用虚线画出过渡元素外框___ 。


您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】与氯元素同族的短周期元素的原子,其核外能量最高的电子所处的电子亚层是________ ;碘元素在元素周期表中的位置是___________ ;液溴的保存通常采取的方法是__________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】原子结构与元素周期表存在着内在联系。根据已学知识,请你回答下列问题:
(1)指出31号元素镓(Ga)在元素周期表中的位置:___ 。
(2)写出原子序数最小的第Ⅷ族元素原子的核外的价电子排布图:____ 。其正三价离子的未成对电子数为____
(3)写出3p轨道上有2个未成对电子的元素的符号:____ 。
(4)日常生活中广泛使用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为3d54s1,该元素的名称为___ 。
(5)基态原子的4s能级中只有1个电子的元素共有___ 种
(6)元素基态原子的M层全充满,N层有且只有一个未成对电子,其基态原子的电子排布式为___ ,属于____ 区元素;[Cu(NH3)4]SO4中所含的化学键有___ ,,[Cu(NH3)4]SO4的外界离子的空间构型为____ 。
(1)指出31号元素镓(Ga)在元素周期表中的位置:
(2)写出原子序数最小的第Ⅷ族元素原子的核外的价电子排布图:
(3)写出3p轨道上有2个未成对电子的元素的符号:
(4)日常生活中广泛使用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为3d54s1,该元素的名称为
(5)基态原子的4s能级中只有1个电子的元素共有
(6)元素基态原子的M层全充满,N层有且只有一个未成对电子,其基态原子的电子排布式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。

下列______ (填写编号)组元素的单质可能都是电的良导体。
①a、c、h ②b、g、k ③c、h、l ④d、e、f

下列
①a、c、h ②b、g、k ③c、h、l ④d、e、f
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】X、Y、Z、L、M五种元素的原子序数依次增大,X的阴离子与Y的内层电子数相等,Y原子的最外层电子数是次外层电子数的两倍,Z、L是空气中含量最多的两种元素,M是地壳中含量最高的金属元素。回答下列问题:
(1)X与L形成的常见阴离子的电子式为____________________ 。
(2)Z、X两元素按原子数目比1:3和2:4构成分子A和B,用电子式表示A的形成过程______ ,B的结构式_______________________ 。
(3)硒是人体必须的微量元素,与L同一主族,硒原子比L原子多两个电子层,则硒在周期表的位置为_______________ ,其最高价氧化物水化物的化学式为_____________ 。
(1)X与L形成的常见阴离子的电子式为
(2)Z、X两元素按原子数目比1:3和2:4构成分子A和B,用电子式表示A的形成过程
(3)硒是人体必须的微量元素,与L同一主族,硒原子比L原子多两个电子层,则硒在周期表的位置为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】下表是元素周期表的一部分,针对表中的①~⑩种元素,请用化学用语回答下列问题:
(1)在③~⑦元素中,原子半径最大的是__________ (填元素符号);
(2)⑦元素的最高价氧化物对应的水化物与其氢化物能生成盐M,M中含有的化学键类型有__________________ ;
(3)写出元素①和⑧的单质在加热条件下反应生成的化合物的电子式:_________ 。
(4)③、⑤、⑦、⑧所形成的离子,其半径由小到大的顺序是________ (填离子符号)
(5)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是_____________ (填物质化学式);呈两性的氢氧化物是_________ (填物质化学式),该化合物与NaOH溶液反应的离子方程式为___________ 。
(6)用电子式表示元素③与⑨形成化合物的过程_____________________________ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑥ | ⑦ | ⑧ | |||||
| 3 | ① | ③ | ⑤ | ⑨ | ⑩ | |||
| 4 | ② | ④ |
(1)在③~⑦元素中,原子半径最大的是
(2)⑦元素的最高价氧化物对应的水化物与其氢化物能生成盐M,M中含有的化学键类型有
(3)写出元素①和⑧的单质在加热条件下反应生成的化合物的电子式:
(4)③、⑤、⑦、⑧所形成的离子,其半径由小到大的顺序是
(5)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是
(6)用电子式表示元素③与⑨形成化合物的过程
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】工业上最早在19世纪中叶便已生产的过氧化氢,目前成为社会需求量迅速增长的化学品,因为它有较强的氧化性,通常用于污水处理中,氧化除去水中的杂质。在过氧化氢分子中,有1个过氧键:-O-O-,每个氧原子再连接一个氢原子。纯的过氧化氢为蓝色的粘稠状液体,沸点是152.1℃,冰点是-0.89℃。
(1)过氧化氢的电子式为___________ ;
(2)过氧化氢是___________ 化合物(离子或共价);
(3)在低于-0.89℃时,过氧化氢是一种蓝色___________ 态物质,组成它的基本微粒是___________ 。
A.H2O2 B.H和O C.H2和O2 D.H和O2
(1)过氧化氢的电子式为
(2)过氧化氢是
(3)在低于-0.89℃时,过氧化氢是一种蓝色
A.H2O2 B.H和O C.H2和O2 D.H和O2
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】回答下列问题:
(1) 微粒中质子数是
微粒中质子数是_______ ,中子数_______ ,核外电子数是_______ 。
(2)它与钠元素形成的化合物的电子式_______ ,物质类型_______ (“离子化合物”/“共价化合物”)。
(3)硫与氢元素形成的化合物是_______ (共价化合物或离子化合物)。
(1)
 微粒中质子数是
微粒中质子数是(2)它与钠元素形成的化合物的电子式
(3)硫与氢元素形成的化合物是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】Ⅰ.用化学用语回答下列问题:
(1)写出二氧化碳分子的电子式:_____________ ;
(2)写出氮气分子的结构式____________ 。
Ⅱ.下列物质:①N2 ②CO2 ③NH3 ④Na2O ⑤Na2O2 ⑥NaOH ⑦CaBr2 ⑧H2O2 ⑨NH4Cl ⑩HBr。
(3)含有极性键和非极性键的是_______ ;
含有非极性键的离子化合物是_____ 。(填序号,下同)
Ⅲ.下列变化中:①干冰气化;②硝酸钾熔化;③KHSO4熔融;④硫酸溶于水;⑤蔗糖溶于水;⑥HI分解;⑦碘升华;⑧溴蒸气被木炭吸附。
(4)未破坏化学键的是_____________ ;
(5)仅离子键被破坏的是_____________ ;
(6)仅共价键被破坏的是_____________ 。
Ⅳ.下列物质:①1H、2H、3H ;②H2O、D2O、T2O;③O2、O3;④14N、14C
(7)互为同位素的是:______ ;
(8)互为同素异形体的是:______ ;
氢的三种原子1H、2H、3H 与氯的两种原子35Cl、37Cl相互结合为氯化氢,可得分子中相对分子质量不同的有________ 种。
(1)写出二氧化碳分子的电子式:
(2)写出氮气分子的结构式
Ⅱ.下列物质:①N2 ②CO2 ③NH3 ④Na2O ⑤Na2O2 ⑥NaOH ⑦CaBr2 ⑧H2O2 ⑨NH4Cl ⑩HBr。
(3)含有极性键和非极性键的是
含有非极性键的离子化合物是
Ⅲ.下列变化中:①干冰气化;②硝酸钾熔化;③KHSO4熔融;④硫酸溶于水;⑤蔗糖溶于水;⑥HI分解;⑦碘升华;⑧溴蒸气被木炭吸附。
(4)未破坏化学键的是
(5)仅离子键被破坏的是
(6)仅共价键被破坏的是
Ⅳ.下列物质:①1H、2H、3H ;②H2O、D2O、T2O;③O2、O3;④14N、14C
(7)互为同位素的是:
(8)互为同素异形体的是:
氢的三种原子1H、2H、3H 与氯的两种原子35Cl、37Cl相互结合为氯化氢,可得分子中相对分子质量不同的有
您最近一年使用:0次



