X、Y、Z、W为原子序数依次增大的前四周期元素,基态原子中,X为元素周期表中半径最小的原子,Z原子最外层电子数为次外层电子数的三倍,W原子的价电子排布为3d104s1,X、Y、Z、W形成的阳离子如图所示,下列说法正确的是
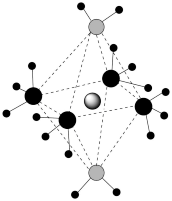

| A.原子半径:Z>Y>X |
| B.气态氢化物的稳定性:Y>Z |
| C.加热时该离子首先失去的组分是X2Z |
| D.两种配体中的键角:X2Z>YX3 |
2021·山东潍坊·一模 查看更多[15]
黑龙江省哈尔滨市第四中学校2022-2023学年高二下学期期中考试化学试题辽宁省大连市第一中学2022-2023学年高二下学期4月学情反馈化学试题专题4 分子空间结构与物质性质 第一~二单元综合拔高练(已下线)必刷卷03-2022年高考化学考前信息必刷卷(山东专用)(已下线)押全国卷理综第10题 元素周期表 元素周期律-备战2022年高考化学临考题号押题(课标全国卷)山东省滕州市第一中学2021-2022学年高三上学期12月份阶段检测化学试题(已下线)提升卷02-【新高考新题型】2022年高考化学选择题标准化练习20卷(山东专用)(已下线)专题06 物质结构 元素周期律-备战2022年高考化学真题及地市好题专项集训【山东专用】(已下线)押全国卷理综第10题 元素周期表元素周期律-备战2021年高考化学临考题号押题(课标全国卷)(已下线)押山东卷第03题 元素周期律、元素周期表-备战2021年高考化学临考题号押题(山东卷)黑龙江省哈尔滨市第六中学2020-2021学年高二4月月考化学试题河北省石家庄市第二中学2020-2021学年高二4月月考化学试题(已下线)小题14 元素周期表、律(根据物质结构角度的元素推断)——备战2021年高考化学经典小题考前必刷(全国通用)(已下线)重点6 物质结构与元素周期律-2021年高考化学【热点·重点·难点】专练(山东专用)山东省潍坊市2021届高三第一次模拟考试化学试题
更新时间:2021-03-11 21:30:41
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法正确的是
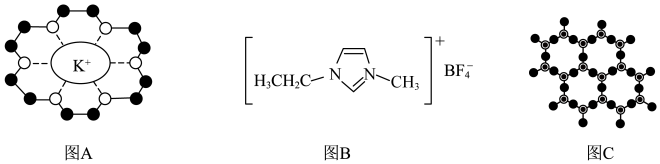
A.图A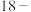 冠 冠 中O原子电负性大带负电荷,通过离子键与 中O原子电负性大带负电荷,通过离子键与 作用,体现了超分子“分子识别"的特征 作用,体现了超分子“分子识别"的特征 |
B.图B物质较 摩尔质量更大,比 摩尔质量更大,比 具有更高的熔沸点 具有更高的熔沸点 |
C.图B中, 该物质含有 该物质含有 键数目为 键数目为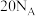 |
D.图C中,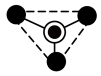 表示硅氧四面体,该结构是无限延伸层状多硅酸根,则化学式为 表示硅氧四面体,该结构是无限延伸层状多硅酸根,则化学式为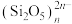 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知X、Y、Z、W为原子序数递增的短周期主族元素。Y的最高价氧化物的水化物是强酸,Z元素的基态原子中有2个未成对电子,基态W原子的价电子排布式为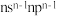 ,X与W为同主族元素。基态R原子的M能层全充满,且其核外有且仅有1个未成对电子。请回答下列问题:
,X与W为同主族元素。基态R原子的M能层全充满,且其核外有且仅有1个未成对电子。请回答下列问题:
(1)固态 的晶胞中,每个
的晶胞中,每个 分子周围等距且紧邻的
分子周围等距且紧邻的 分子有
分子有___________ 个。
(2)元素X、Y、Z是构成邻苯二甲酸酐(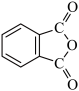 )和邻苯二甲酰亚胺(
)和邻苯二甲酰亚胺(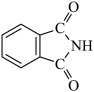 )的原子,后者熔点高于前者,主要原因是
)的原子,后者熔点高于前者,主要原因是___________ 。
(3)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态的Y原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的Y原子,其价电子自旋磁量子数的代数和为___________ 。
(4)下列有关的叙述中错误的是___________ 。
a.单质W属于共价晶体
b.Y的含氧酸根的空间构型为平面三角形
c.硅的电负性处于碳和磷之间,因此其是一种“类金属”
d.基态W原子的核外电子占据的最高能级轨道为3p轨道
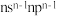 ,X与W为同主族元素。基态R原子的M能层全充满,且其核外有且仅有1个未成对电子。请回答下列问题:
,X与W为同主族元素。基态R原子的M能层全充满,且其核外有且仅有1个未成对电子。请回答下列问题:(1)固态
 的晶胞中,每个
的晶胞中,每个 分子周围等距且紧邻的
分子周围等距且紧邻的 分子有
分子有(2)元素X、Y、Z是构成邻苯二甲酸酐(
 )和邻苯二甲酰亚胺(
)和邻苯二甲酰亚胺( )的原子,后者熔点高于前者,主要原因是
)的原子,后者熔点高于前者,主要原因是(3)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用
 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态的Y原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的Y原子,其价电子自旋磁量子数的代数和为(4)下列有关的叙述中错误的是
a.单质W属于共价晶体
b.Y的含氧酸根的空间构型为平面三角形
c.硅的电负性处于碳和磷之间,因此其是一种“类金属”
d.基态W原子的核外电子占据的最高能级轨道为3p轨道
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】化学工业为新冠疫情防控提供了强有力的物质支撑。科学家利用原子序数依次增大的四种短周期元素X、Y、W和Z“组合”成一种高效、贮运稳定的消毒漂白剂,其分子结构示意图如下,Z原子的L层电子数比W原子的L层电子数多2个。下列说法正确的
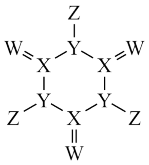

| A.原子半径:W>Y>X |
| B.Y和Z的氧化物对应的水化物均为强酸 |
| C.简单氢化物的沸点:W>Y |
| D.简单氢化物的还原性:X<Z |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】短周期主族元素W、X、Y、Z的原子序数依次增大,X的原子半径是所有短周期主族元素中最大的,W的核外电子数与X、Z的最外层电子数之和相等,Y的原子序数是Z的最外层电子数的2倍,由W、X、Y三种元素形成的化合物M的结构如图所示。下列叙述正确的是
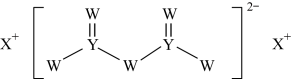

| A.元素非金属性强弱的顺序为W>Y>Z |
| B.化合物M中W不都满足8电子稳定结构 |
| C.W分别与X、Y、Z形成的二元化合物均只有一种 |
| D.Y单质的熔点高于X单质 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D、E均为短周期元素,A、B、C位于同一周期相邻位置,它们分别与D形成的分子中都有10个电子,且A和C的原子序数之比为3∶4,E原子半径是短周期元素原子半径最大的。则下列叙述正确的是
| A.E和C能形成不止一种化合物,且不同化合物化学键类型完全相同 |
| B.由B、D组成的物质是电解质 |
| C.由A、B、C、D四种元素形成的化合物一定不属于离子化合物 |
| D.A和C能形成共价化合物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】水合肼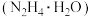 是一种无色透明发烟液体,具有强碱性和吸湿性,工业上常用作抗氧化剂。实验室利用反应
是一种无色透明发烟液体,具有强碱性和吸湿性,工业上常用作抗氧化剂。实验室利用反应 制备水合肼。下列有关说法正确的是
制备水合肼。下列有关说法正确的是
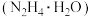 是一种无色透明发烟液体,具有强碱性和吸湿性,工业上常用作抗氧化剂。实验室利用反应
是一种无色透明发烟液体,具有强碱性和吸湿性,工业上常用作抗氧化剂。实验室利用反应 制备水合肼。下列有关说法正确的是
制备水合肼。下列有关说法正确的是| A.氯离子核外电子有18种空间运动状态 |
B.以上相关元素第一电离能关系: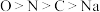 |
C.该反应中C原子均为 杂化,N原子均为 杂化,N原子均为 杂化 杂化 |
D. 中 中 键角小于 键角小于 中 中 键角 键角 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的有几项
①键长:碳碳三键>碳碳双键>碳碳单键 ②酸性:CF3COOH>CCl3COOH>CH3COOH
③沸点:正戊烷>异戊烷>新戊烷 ④熔点:SiO2>NaCl>C60
⑤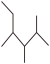 的名称为3,4-二甲基-2-乙基戊烷 ⑥键角:CH4>NH3>PH3
的名称为3,4-二甲基-2-乙基戊烷 ⑥键角:CH4>NH3>PH3
⑦HF比HCl沸点高的原因是HF分子内存在氢键
⑧甲苯与液溴在光照条件下可生成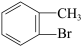 ⑨正己烷和2,2-二甲基丁烷互为同系物
⑨正己烷和2,2-二甲基丁烷互为同系物
⑩单烯烃和氢气加成后得到饱和烃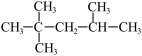 ,则该单烯烃可能有2种结构
,则该单烯烃可能有2种结构
⑪主族元素的电负性越大,其元素原子的第一电离能一定越大
⑫在任何情况下,都是σ键比π键强度大
①键长:碳碳三键>碳碳双键>碳碳单键 ②酸性:CF3COOH>CCl3COOH>CH3COOH
③沸点:正戊烷>异戊烷>新戊烷 ④熔点:SiO2>NaCl>C60
⑤
 的名称为3,4-二甲基-2-乙基戊烷 ⑥键角:CH4>NH3>PH3
的名称为3,4-二甲基-2-乙基戊烷 ⑥键角:CH4>NH3>PH3⑦HF比HCl沸点高的原因是HF分子内存在氢键
⑧甲苯与液溴在光照条件下可生成
 ⑨正己烷和2,2-二甲基丁烷互为同系物
⑨正己烷和2,2-二甲基丁烷互为同系物⑩单烯烃和氢气加成后得到饱和烃
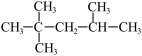 ,则该单烯烃可能有2种结构
,则该单烯烃可能有2种结构⑪主族元素的电负性越大,其元素原子的第一电离能一定越大
⑫在任何情况下,都是σ键比π键强度大
| A.5项 | B.6项 | C.4项 | D.8项 |
您最近一年使用:0次
【推荐3】五种前四周期的元素X、Y、Z、Q、T。已知X元素基态原子的M层有6种运动状态不同的电子;Y原子的价电子构型为3d84s2,基态Z原子的L层p能级有一个空轨道;Q原子的L电子层的p能级只有一对成对电子;基态T原子的M电子层上p轨道半充满。下列说法错误的是
| A.Y、Q及氢三种元素形成的某化合物,能用于制作可充电电池的电极材料 |
| B.若X、T、Z的最高价的氧化物对应的水化物分别为u、v、w,则酸性为:u>v>w。理由是含氧酸酸性与非羟基氧原子数有关 |
| C.X、Y、T三种元素第一电离能的大小次序是:X>T>Y |
| D.化合物ZQ2、ZX2均是由极性键构成的非极性分子 |
您最近一年使用:0次



