(1)在水的电离平衡中,c(H+)和c(OH-)的关系如图所示。A点水的离子积为1.0×10-14,B点水的离子积为_______ 。

(2)下列说法正确的是_______ (填字母)。
a. 图中A、B、D三点处Kw的大小关系:B>A>D
b. AB线上任意点的溶液均显中性
c. B点溶液的pH=6,显酸性
d. 图中温度T1>T2
(3)T2时,若盐酸中c(H+)=5×10-4mol·L-1,则由水电离产生的c(H+)=_______ 。

(2)下列说法正确的是
a. 图中A、B、D三点处Kw的大小关系:B>A>D
b. AB线上任意点的溶液均显中性
c. B点溶液的pH=6,显酸性
d. 图中温度T1>T2
(3)T2时,若盐酸中c(H+)=5×10-4mol·L-1,则由水电离产生的c(H+)=
20-21高二·浙江·阶段练习 查看更多[1]
(已下线)【浙江新东方】高中化学20210304-003
更新时间:2021-03-14 21:32:42
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】(1)某温度(t℃)时,水的离子积为Kw=1×10-13,则该温度____________ 25℃(选填 “>”“<”“=”),其理由是____________________________________ 。
(2)若保持温度不变,向少量水中加入____________ g的NaOH固体,并加入水至1L,才能使溶液中水电离产生的H+、OH-的浓度乘积为c(H+)水·c (OH-)水=10-26。
(3)若保持温度不变,向水中通入HCl气体,恰好使溶液中的c(H+)/c(OH-)=109,此时水电离出的的c (OH-)=____________ 。
(4)若将此温度下pH=11的NaOH溶液aL与pH=1的稀硫酸bL混合(设混合后溶液体积的微小变化忽略不计),试通过计算填写以下不同情况时两溶液的体积比。
①若所得混合溶液为中性,则a:b =____________________________________ 。
②若所得混合液的pH=3,则a:b=____________________________________ 。
③若a:b=101:9,则混合后溶液的pH=____________________________________ 。
(2)若保持温度不变,向少量水中加入
(3)若保持温度不变,向水中通入HCl气体,恰好使溶液中的c(H+)/c(OH-)=109,此时水电离出的的c (OH-)=
(4)若将此温度下pH=11的NaOH溶液aL与pH=1的稀硫酸bL混合(设混合后溶液体积的微小变化忽略不计),试通过计算填写以下不同情况时两溶液的体积比。
①若所得混合溶液为中性,则a:b =
②若所得混合液的pH=3,则a:b=
③若a:b=101:9,则混合后溶液的pH=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】常温下,0.1mol·L 溶液中,
溶液中,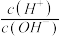 =
=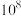 。现取0.1mol·L
。现取0.1mol·L 溶液与PH=13的
溶液与PH=13的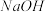 溶液等体积混合(忽略混合后溶液体积的变化)。试回答下列问题:
溶液等体积混合(忽略混合后溶液体积的变化)。试回答下列问题:
(1)混合溶液呈_______ 性(“酸”﹑“中”或“碱”),理由(用离子方程式表示)________ .
(2)混合溶液中由水电离出的
___________ 0.1mol·L 溶液中由水电离出的
溶液中由水电离出的 (填“大于”﹑“小于”或“等于”)。
(填“大于”﹑“小于”或“等于”)。
(3)若混合后溶液的pH=a,则 -
- =
=_________ mol·L (用含a的代数式表示)。
(用含a的代数式表示)。
 溶液中,
溶液中,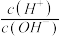 =
=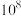 。现取0.1mol·L
。现取0.1mol·L 溶液与PH=13的
溶液与PH=13的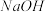 溶液等体积混合(忽略混合后溶液体积的变化)。试回答下列问题:
溶液等体积混合(忽略混合后溶液体积的变化)。试回答下列问题:(1)混合溶液呈
(2)混合溶液中由水电离出的

 溶液中由水电离出的
溶液中由水电离出的 (填“大于”﹑“小于”或“等于”)。
(填“大于”﹑“小于”或“等于”)。(3)若混合后溶液的pH=a,则
 -
- =
= (用含a的代数式表示)。
(用含a的代数式表示)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】完成下列各题:
(1)磷的一种化合物叫亚磷酸( )。已知:
)。已知:
(i)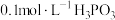 溶液的
溶液的 ;
;
(ii) 与NaOH反应只生成
与NaOH反应只生成 和
和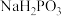 ;
;
(iii) 和碘水反应,碘水棕黄色褪去,再加
和碘水反应,碘水棕黄色褪去,再加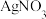 溶液有黄色沉淀生成。
溶液有黄色沉淀生成。
①关于 的说法:a.强酸;b.弱酸;c.二元酸;d.三元酸;e.氧化性酸;f.还原性酸,其中正确的是
的说法:a.强酸;b.弱酸;c.二元酸;d.三元酸;e.氧化性酸;f.还原性酸,其中正确的是______ 。(填序号)
A.bdf B.ade C.bcf D. bce
②Na2HPO3为__________ (填“正盐”或“酸式盐”)
(2)常温下,氨水的pH>7,用离子方程式解释其原因:_____________________________ 。
(3)25℃时, 溶液和盐酸的物质的量浓度相同。
溶液和盐酸的物质的量浓度相同。
①加水稀释至相同的倍数,此时 溶液的pH
溶液的pH______ (填“大于”“小于”或“等于”)盐酸的pH。
②加水稀释至相同的pH,此时加入 溶液中水的体积
溶液中水的体积______ (填“大于”“小于”或“等于”)加入盐酸中水的体积。
(4)常温下, 溶液中
溶液中
______ (用含 和
和 的代数式表示)。
的代数式表示)。
(5)25℃时,现有 的HCl溶液100mL,要使它的
的HCl溶液100mL,要使它的 ,如果加入蒸馏水,需加水
,如果加入蒸馏水,需加水______ mL;如果加入 的HCl溶液,需加入此HCl溶液
的HCl溶液,需加入此HCl溶液______ mL(假定溶液体积有加和性,下同)。
(6)某温度下,纯水中的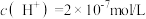 。若温度不变,滴入稀硫酸使
。若温度不变,滴入稀硫酸使 ,则由水电离出的
,则由水电离出的 为
为______ mol/L。
(1)磷的一种化合物叫亚磷酸(
 )。已知:
)。已知:(i)
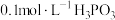 溶液的
溶液的 ;
;(ii)
 与NaOH反应只生成
与NaOH反应只生成 和
和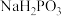 ;
;(iii)
 和碘水反应,碘水棕黄色褪去,再加
和碘水反应,碘水棕黄色褪去,再加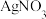 溶液有黄色沉淀生成。
溶液有黄色沉淀生成。①关于
 的说法:a.强酸;b.弱酸;c.二元酸;d.三元酸;e.氧化性酸;f.还原性酸,其中正确的是
的说法:a.强酸;b.弱酸;c.二元酸;d.三元酸;e.氧化性酸;f.还原性酸,其中正确的是A.bdf B.ade C.bcf D. bce
②Na2HPO3为
(2)常温下,氨水的pH>7,用离子方程式解释其原因:
(3)25℃时,
 溶液和盐酸的物质的量浓度相同。
溶液和盐酸的物质的量浓度相同。①加水稀释至相同的倍数,此时
 溶液的pH
溶液的pH②加水稀释至相同的pH,此时加入
 溶液中水的体积
溶液中水的体积(4)常温下,
 溶液中
溶液中
 和
和 的代数式表示)。
的代数式表示)。(5)25℃时,现有
 的HCl溶液100mL,要使它的
的HCl溶液100mL,要使它的 ,如果加入蒸馏水,需加水
,如果加入蒸馏水,需加水 的HCl溶液,需加入此HCl溶液
的HCl溶液,需加入此HCl溶液(6)某温度下,纯水中的
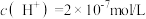 。若温度不变,滴入稀硫酸使
。若温度不变,滴入稀硫酸使 ,则由水电离出的
,则由水电离出的 为
为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】计算25℃时
(1)
 的
的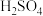 加水稀释至
加水稀释至 ,
,
_____ 。
(2) 的氢氧化钠溶液,
的氢氧化钠溶液,
______ 。
(3) 0.005 mol·L-1的硫酸溶液的pH=________ ,水电离出的c(H+)= ________ mol·L-1。
(4)某温度下,纯水的c(H+)=1×10-8 mol·L-1,则此时纯水的c(OH-)为________ 。 此时温度________ (填“高于”、“低于”或“等于”)25 ℃。
(1)

 的
的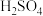 加水稀释至
加水稀释至 ,
,
(2)
 的氢氧化钠溶液,
的氢氧化钠溶液,
(3) 0.005 mol·L-1的硫酸溶液的pH=
(4)某温度下,纯水的c(H+)=1×10-8 mol·L-1,则此时纯水的c(OH-)为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】水的电离平衡曲线如图所示,若A点、B点分别表示25℃和100℃时水的电离达平衡时的离子浓度。则表示25℃的是________ (填“A”或“B”)。100℃时,在1mol∙L﹣1的NaOH溶液中,由水电离出的c(H+)=________ mol∙L﹣1。 100℃时,5×10﹣5 mol∙L﹣1的H2SO4溶液与pH=9的Ba(OH)2溶液混合后pH=7,则混合前H2SO4溶液与Ba(OH)2溶液的体积比为________ 。


您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】现有常温条件下浓度均为0.1 mol•L-1的甲、乙、丙、丁四种溶液,甲为NaOH溶液,乙为HCl溶液,丙为CH3COOH溶液,丁为氨水,已知Ka(CH3COOH)=Kb(NH3•H2O)试回答下列问题:
(1)甲、丁种溶液中由水电离出的c(OH−)的大小关系为甲___ 丁(填“大于”“小于”或“等于”)。
(2)将一定体积的甲与乙混合,所得溶液pH=12,则二者的体积比为v甲∶v乙=___ 。
(3)某同学用甲滴定丙溶液、乙滴定丁溶液,得到如图所示两条滴定曲线,请完成有关问题:

①乙溶液滴定丁溶液最适合的指示剂是___ ;甲溶液滴定丙溶液,选用酚酞为指示剂,则达到滴定终点的标志是___ 。
②计算滴定至b点时,c(CH3COOH)+c(CH3COO-)=___ mol•L-1
③向氨水中滴加盐酸至a点,溶液中离子浓度从大到小的顺序为___ ,若加盐酸vmL时,溶液恰好呈中性,用含v的代数式表示出Kb=___ (不考虑溶液混合体积变化)。
(1)甲、丁种溶液中由水电离出的c(OH−)的大小关系为甲
(2)将一定体积的甲与乙混合,所得溶液pH=12,则二者的体积比为v甲∶v乙=
(3)某同学用甲滴定丙溶液、乙滴定丁溶液,得到如图所示两条滴定曲线,请完成有关问题:

①乙溶液滴定丁溶液最适合的指示剂是
②计算滴定至b点时,c(CH3COOH)+c(CH3COO-)=
③向氨水中滴加盐酸至a点,溶液中离子浓度从大到小的顺序为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】(1)某温度(t℃)时,水的离子积为Kw=1×10-13,则该温度____________ 25℃(选填 “>”“<”“=”),其理由是____________________________________ 。
(2)若保持温度不变,向少量水中加入____________ g的NaOH固体,并加入水至1L,才能使溶液中水电离产生的H+、OH-的浓度乘积为c(H+)水·c (OH-)水=10-26。
(3)若保持温度不变,向水中通入HCl气体,恰好使溶液中的c(H+)/c(OH-)=109,此时水电离出的的c (OH-)=____________ 。
(4)若将此温度下pH=11的NaOH溶液aL与pH=1的稀硫酸bL混合(设混合后溶液体积的微小变化忽略不计),试通过计算填写以下不同情况时两溶液的体积比。
①若所得混合溶液为中性,则a:b =____________________________________ 。
②若所得混合液的pH=3,则a:b=____________________________________ 。
③若a:b=101:9,则混合后溶液的pH=____________________________________ 。
(2)若保持温度不变,向少量水中加入
(3)若保持温度不变,向水中通入HCl气体,恰好使溶液中的c(H+)/c(OH-)=109,此时水电离出的的c (OH-)=
(4)若将此温度下pH=11的NaOH溶液aL与pH=1的稀硫酸bL混合(设混合后溶液体积的微小变化忽略不计),试通过计算填写以下不同情况时两溶液的体积比。
①若所得混合溶液为中性,则a:b =
②若所得混合液的pH=3,则a:b=
③若a:b=101:9,则混合后溶液的pH=
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】(1)在常温下的0.05 mol·L-1硫酸溶液中,c(H+)=_______ mol·L-1,水电离出的c(H+)=___________ mol·L-1,水电离出的c(OH-)=_________ mol·L-1。
(2)某温度下,纯水的c(H+)=2×10-7 mol·L-1,则此时c(OH-)为_____________ mol·L-1。若温度不变,滴入稀盐酸使c(H+)=5×10-4 mol·L-1,则溶液中c(OH-)为_______________ mol·L-1,此时温度_______ (填“高于”、“低于”或“等于”)25 ℃。
(2)某温度下,纯水的c(H+)=2×10-7 mol·L-1,则此时c(OH-)为
您最近一年使用:0次




